Глава 9. БИОМЕМБРАНЫ И БИОЭНЕРГЕТИКА
ОСНОВНЫЕ ПРИНЦИПЫ ОРГАНИЗАЦИИ БИОМЕМБРАН
Все клетки отграничены друг от друга и от окружающей среды с помощью специальной оболочки – клеточной мембраны. Со времен К. Негели, описавшего в 1855 г. структуру мембран, окружающих живые клетки, представления об устройстве и функциях мембран существенно обогатились. Клеточная мембрана во многом определяет свойства, поведение и даже форму клетки. Мембраны прокариот и эукариот различаются между собой по составу и свойствам. Растительные и животные клетки также отличаются друг от друга как по набору органелл, так и по свойствам мембран (рис. 9.1).
Состав и строение биологических мембран. Биологические мембраны состоят из белков и липидов. Углеводы присутствуют лишь в качестве составных частей сложных белков (гликопротеинов) и сложных липидов (гликолипидов). Нуклеиновые кислоты в небольшом количестве бывают ассоциированы с мембранами, но в состав мембранных структур не включаются. Вода составляет 20% от мембранного материала, а отношение белок/липид в зависимости от вида мембран колеблется от 0,25 (клетки миелиновой оболочки) до 3,0 (митохондриальные мембраны).
Липиды мембран представлены четырьмя основными группами: фосфо-липидами (основная доля), сфинголипидами, гликолипидами и стероидами. Фосфолипиды – это сложные эфиры фосфатидной кислоты. Основными фосфолипидами являются фосфатидилэтаноламин, фосфатидилсерин, фос-фатидилинозит и фосфатидилхолин. В состав фосфолипидов входят также дифосфатидилглицерины (кардиолипин), плазмалогены (1-О-алкенил-2-О ацилфосфолипиды) и диольные фосфолипиды. Сфинголипиды, которые являются производными церамида и монофосфорных эфиров различных спиртов, представлены в основном сфингомиелином. Гликолипиды – глико-зильные производные церамида – представлены как нейтральными церебро-зидами, так и их кислыми сульфоэфирами – сульфатидами. Производные церамида и нейраминовой кислоты – ганглиозиды – часто выделяют в отдельную группу липидов – гликосфинголипиды. Стероиды представлены холестерином (в мембранах животных клеток), ситостерином (в растительных клетках) и тетрахименином (обнаружен у тетрахимены).
Несмотря на различия в составе, все мембранные липиды построены по единому плану и легко смешиваются друг с другом, образуя монослойные или бислойные структуры (рис. 9.2). В этих структурах реализуется 2 типа взаимодействий: ионные взаимодействия полярных «голов» и гидрофобные взаимодействия жирнокислотных цепей. Благодаря этому мицеллы и липо-сомы, создаваемые протяженными бислойными структурами, достаточно стабильны в водном окружении.
В наружных (плазматических) мембранах животных клеток обнаруживается большое количество холестерина (около 21 моль%), меньше – фосфатидилэтаноламина и еще меньше фосфатидилхолина. Для внутриклеточных мембран основным компонентом является фосфатидилхолин, и соотношение фосфатидилхолин/фосфатидилэтаноламин в них всегда больше 1.
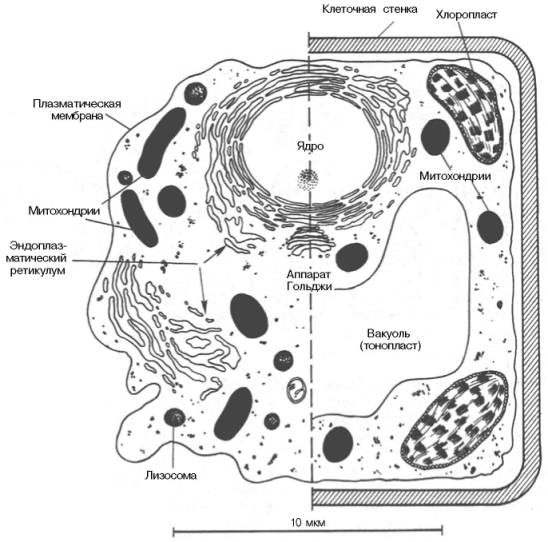
Рис. 9.1. Схематическое изображение животной (слева) и растительной (справа) клетки.
Соотношение основных классов липидов мембран нейронов у различных животных почти не подвержено изменениям. По-видимому, это соотношение сформировалось на самых ранних стадиях эволюции и обеспечивает как стабильность липидного бислоя, так и возможность включения в него белковых молекул. В то же время жирнокислотные компоненты мембранных липидов сильно подвержены эволюционной и сезонной изменчивости.
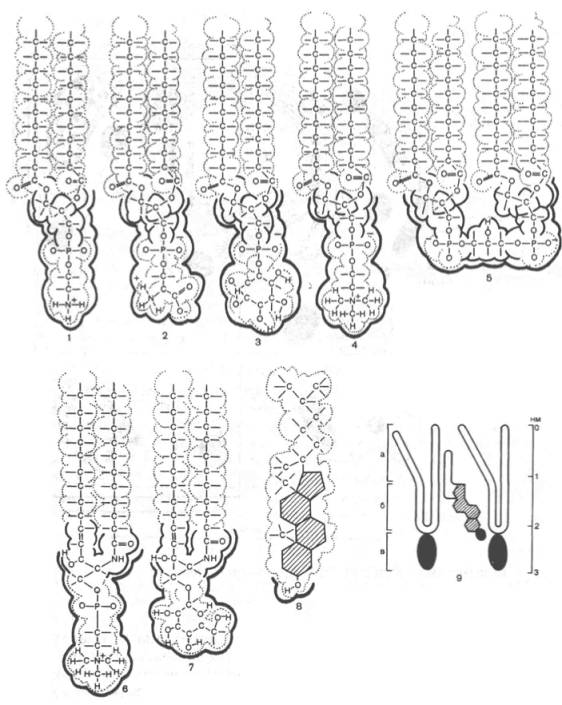
Рис. 9.2. Химические формулы распространенных липидов биологических мембран. 1 - фосфатидилэтаноламин; 2 - фосфатидилсерин; 3 - фосфатидилинозит; 4 - фосфатидилхолин; 5 - кардиолипин; 6 - сфингомиелин; 7 - цереброзид; 8 - холестерин; 9 - расположение молекулы холестерина между двумя молекулами фосфолипидов: а - наименее упорядоченная область бислоя, б - область, упорядочиваемая холестерином, в - область полярных «голов». Красным отмечены полярные области молекул.
Жирные
кислоты, составляющие «хвост» липидных молекул, представлены насыщенными [от
лауриновой (С12) до лигноцериновой (С24)] и ненасыщенными
(мононенасыщенные пальмитоолеиновая и олеиновая; полиненасыщенные линолевая,
линоленовая, арахидоновая) кислотами. У высших растений преобладают
пальмитиновая, олеиновая и линолевая кислоты, а стеариновая почти не
обнаруживается; в ряде случаев выявляются оксикислоты. В мембранах животных
клеток, кроме пальмитиновой и олеиновой, много стеариновой кислоты и больше
высокомолекулярных жирных кислот (содержат
20–24 углеродных
фрагмента). Жирные кислоты, как правило,
имеют четное число атомов углерода, но у цереброзидов и ган-глиозидов
встречаются и нечетные углеводородные остовы. У бактерий полиненасыщенные
жирные кислоты практически отсутствуют, но часто имеются разветвленные окси- и
циклопропансодержащие кислоты. Для мембран термоацидофильных, галофильных и
метанообразующих архебак-терий характерно
наличие нетипичных липидов, содержащих изопреноидные цепи,
метальные концы которых соединены друг с другом ковалент-ными связями. Такие
«шпильки» обеспечивают повышенную прочность липидного бислоя. (Подробнее о
жирных кислотах см. главу 11.)
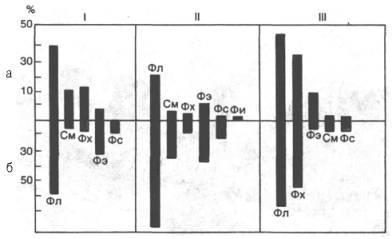
Рис. 9.3. Распределение липидов между наружной (а) и
внутренней (б) сторонами бислоя в мембранах эритроцитов (I), вируса гриппа (II) и саркоплазматического
ретикулума кролика (III). Фл - общие
фосфолипиды; Фх - фосфатидилхолин; Фэ - фосфатидилэтаноламин; Фс -
фосфати-дилсерин; См - сфингомиелин; Фи - фосфатидилинозит.
Липиды в составе бислоя распределяются асимметрично. Это свойство диктуется особенностями строения их молекул: фосфатидилхолину, фосфат-идилсерину, сфингомиелину присуща цилиндрическая форма, фосфатидил-этаноламину – форма конуса, а лизофосфолипидам (получаются в результате отщепления от молекулы одной жирнокислотной цепи) – форма перевернутого конуса. Природные мембраны также обладают исходной асимметрией (рис. 9.3).
Белки взаимодействуют с мембранным бислоем, в результате чего они либо ассоциируются с поверхностью мембраны – периферические белки, либо пересекают бислой один или несколько раз, прочно интегрируясь в него,– это интегральные белки. Интеграция оказывается возможной, если в первичной структуре белка имеются достаточно протяженные участки, содержащие гидрофобные аминокислотные последовательности. В таком случае белковые молекулы способны самопроизвольно встраиваться в би-слой. При ассоциации рибосом с мембранными структурами встраивание гидрофобных белков в мембрану осуществляется синхронно с их синтезом при участии специальных механизмов, потребляющих энергию АТФ.
Участки белка, которые обращены во внеклеточную среду, могут подвергаться гликозилированию. В мембранах растений и бактерий полисахара играют самостоятельную роль, образуя наружную оболочку. В клетках животных, в которых наружный слой включает углеводы, имеется внутренний цитоскелет, состоящий из актина и других легко полимеризующихся белков; он имеет регулярную связь с мембранными белками и выполняет формообразующую и опорную функцию (рис. 9.4).
Фазовое состояние мембранных липидов. Мембранные липиды могут находиться в нескольких фазовых состояниях, т. е. они обладают мезомор-физмом. Два основных ламеллярных состояния, характерных для мембранных липидов в клеточных системах: кристаллическое и жидкокристаллическое – различаются плотностью упаковки и подвижностью находящихся в бислое белковых молекул. При более плотной упаковке ацильные цепи липидов расположены под углом, близким к 90°, и все С—С-связи находятся в транс-конформации (максимально вытянуты). Фазовый переход приводит к увеличению подвижности ацильных цепей в бислое, увеличению угла их наклона и уменьшению плотности упаковки. Латеральная подвижность мембранных белков после фазового перехода возрастает, увеличивается вероятность образования их ассоциатов.
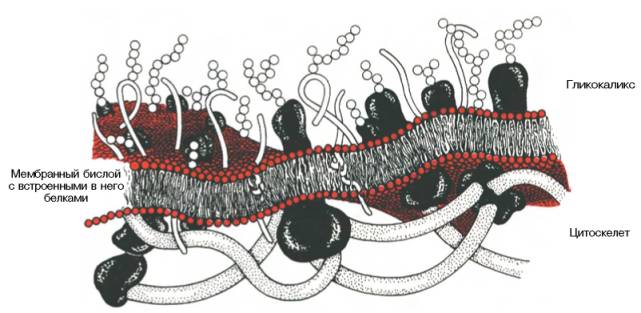
Рис. 9.4. Схематическое изображение клеточной мембраны.
В липидном бислое могут также образовываться гексагональные структуры (вывернутые мицеллы). При их образовании в мембране возникают дефекты регулярной упаковки, что позволяет проникать через мембрану крупным молекулам, а также обеспечивает обмен компонентами монослоев в бислойной мембране.
Фазовые переходы мембранных липидов могут быть вызваны изменением температуры среды. Значение температуры, при котором наблюдается фазовый переход, называется критической температурой фазового перехода, или разделения фаз, если различные участки мембраны вследствие гетерогенности липидного состава по-разному отвечают на изменения температуры. Ионы Са2+, изменение числа ненасыщенных жирнокислотных цепей мембранных фосфолипидов и некоторые другие факторы также могут индуцировать фазовые переходы в бислое. Обычно критическая температура фазовых переходов приближена к температуре тела гомойотермных животных (или к температуре среды обитания пойкилотермных животных). Таким образом, достаточно незначительного изменения условий, чтобы изменить упаковку мембраны.
Специфические свойства биологических мембран. Благодаря указанным особенностям биологические мембраны имеют присущие им характерные черты. Они образуют протяженные бислойные структуры малой толщины (6–10 нм), объединяющие белковые и липидные компоненты с различными свойствами.
Целостная структура мембраны создается за счет гидрофобных и электростатических взаимодействий, а не за счет ковалентных связей между составляющими ее молекулами белков и липидов. Гидрофобный липидный бислой представляет естественную преграду для проникновения полярных молекул. Мембраны асимметричны по своему исходному строению, что обеспечивает градиент кривизны и спонтанное образование замкнутых структур.
Мембранный бислой обладает относительно малой микровязкостью. Другими словами, мембраны рыхло упакованы, что позволяет отдельным компонентам проявлять высокую подвижность в латеральном направлении.
Наружные мембраны клеток отличаются от внутренних по липидному составу (последние почти не содержат стеринов, имеют соотношение ФХ/ФЭ > 1) и обладают специфическим набором ферментов и рецепторов. Как правило, белки плазматических мембран со стороны внеклеточной среды обильно гликозилированы. Внутриклеточные мембраны содержат мало гликопротеинов и гликолипидов и характеризуются меньшей микровязкостью. Благодаря этому они могут образовывать органеллы малого размера. Мембранные белки выполняют различные специфические функции: рецепторные, транспортные, ферментативные, энергопреобразующие и т.д. (см. далее).
Функции биологических мембран. Как отмечалось, клеточные мембраны отграничивают содержимое клетки (или клеточной органеллы) от окружающей среды. Благодаря наличию специальных рецепторов они воспринимают сигналы из внешней среды (например, молекулы гормонов, называемые первичными мессенджерами, или посредниками), в ответ на которые образуются вторичные мессенджеры, высвобождающиеся внутрь клетки. Так осуществляется преобразование сигналов, изменяющих клеточный метаболизм в соответствии с изменяющимися условиями среды (см. главу 8).
Мембранные рецепторы выполняют функции узнавания (иммунокомпе-тентная система), адгезии (обеспечение межклеточных контактов, формирование тканей), регуляции активности ионных каналов (электрическая возбудимость, создание мембранного потенциала). Мембранные ферменты в составе бислоя приобретают большую стабильность и способность к осуществлению реакций, которые в гидрофильном окружении протекали бы с весьма малой скоростью. Липидное окружение предоставляет таким белкам «привилегированные» условия функционирования, но и накладывает ограничения на поведение белковых ассоциатов: последнее сильно зависит от плотности упаковки (микровязкости) мембран. Поэтому факторы, влияющие на липидный состав и свойства клеточной мембраны, оказывают регулирующее влияние на функции мембранных белков.
Мембранные белки часто образуют олигомерные ансамбли, взаимодействия между которыми (или длительность их существования в бислое) оказывается под контролем их мембранного окружения. Изменения микровязкости мембран в таком случае позволяют контролировать активность этих надмолекулярных структур.
Транспортная функция является одной из важных функций клеточных мембран (рис. 9.5). Мембрана создает существенные ограничения для проникновения различных веществ, однако она не является полностью непроницаемой: небольшие нейтральные молекулы могут проникать через бислой в области структурных дефектов. Этот процесс осуществляется по градиенту концентрации переносимого вещества - из области, где его содержание высоко, в область с более низким содержанием. Такой процесс называется простой диффузией, он осуществляется неизбирательно и с низкой скоростью.
При облегченной диффузии вещества также переносятся в направлении их концентрационного градиента, но с использованием специальных структур - переносчиков или каналов, увеличивающих скорость и специфичность переноса. Известны высокоспецифические транслоказы - белковые молекулы, переносящие аденило-вые нуклеотиды через внутреннюю мембрану митохондрий: Nа+/Са2+-обменник -белок, входящий в состав плазматических мембран многих клеток; низкомолекулярный пептид бактериального происхождения валиномицин - специфический переносчик для ионов К+.
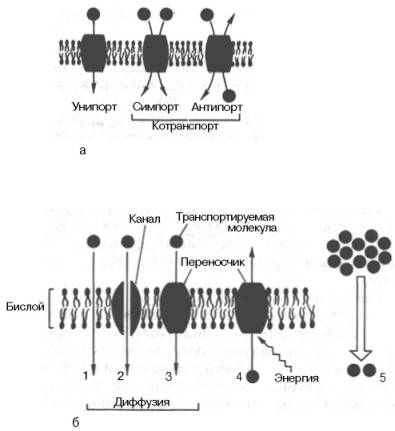
Рис. 9.5. Перенос веществ через мембрану. а - виды переноса; б - пассивный и активный транспорт: 1 - пассивная диффузия; 2 - диффузия с помощью канала; 3 - диффузия с помощью переносчика; 4 - активный транспорт; 5 - вторично-активный транспорт.
Облегченная диффузия, осуществляемая с помощью каналов, не обладает высокой специфичностью (специфичность определяется лишь размерами канала), но протекает с большей скоростью, а процесс переноса не достигает насыщения в широком диапазоне концентраций переносимого вещества. Функционирование каналов в меньшей степени зависит от фазового состояния мембраны, чем функционирование переносчиков. Все эти примеры относятся к пассивному транспорту через мембрану.
Активный транспорт веществ осуществляется такими же механизмами, но протекает против концентрационного градиента и для своего осуществления должен быть сопряжен с энергодающим процессом. Основным источником энергии для активного транспорта является АТФ. Поэтому, как правило, эти системы представляют собой АТФазы. Примером систем активного транспорта ионов является Na+/K+-АТФаза плазматических мембран животных клеток, которая «выкачивает» из клетки ионы натрия в обмен на ионы калия, затрачивая на выполнение этой работы АТФ в стехиометрии 3Nа+/2К+/1АТФ. Са2+-АТФаза осуществляет активный транспорт кальция через мембрану со стехиометрией 2Са2+/1АТФ.
В так называемых сопрягающих мембранах имеются протонные насосы, работающие как Н+-АТФазы. В результате их функционирования на мембране
возникает разность концентраций протонов (ΔрН) и разность электрических потенциалов, в совокупности образующие протонный электрохимический потенциал, обозначаемый ΔμН+ (см. далее). За счет работы Н+-АТФазы создается кислая среда в некоторых органеллах клетки (например, лизосомах, хромаффинных клетках надпочечников). В митохондриальной мембране Н+-АТФаза работает в обратном направлении, используя ΔμН+, создаваемый в дыхательной цепи, для образования АТФ.
Наконец, в клетках широко представлен вторично-активный транспорт, в процессе которого градиент одного вещества используется для транспорта другого. С помощью вторично-активного транспорта клетки аккумулируют сахара, аминокислоты и выводят некоторые продукты метаболизма, используя градиент Na+, создаваемый в ходе работы Na+/К+-АТФазы (см. рис. 9.5).
Предыдущая страница |
Следующая страница
СОДЕРЖАНИЕ