Простая связь
Простая связь, ординарная связь, одинарная связь, химическая ковалентная связь, осуществляемая парой электронов (с антипараллельной ориентацией спинов), движущихся в поле 2 атомных ядер. Например, в молекулах H2, Cl2 и HCl имеется по одной ковалентной связи, образованной взаимодействием неспаренных электронов (находившихся на атомных орбиталях 1s—1s, 3р—3р и 1s—3р соответственно). Поскольку эти молекулы двухатомны, химические связи в них двухцентровые. Для указанных молекул можно написать следующие электронные и структурные формулы: Н: Н и Н—Н, Cl: Cl и Cl—Cl, H: Cl и Н—Cl [две точки и валентный штрих (чёрточка) обозначают пару электронов, общую для обоих соединившихся атомов].
Аналогичное описание справедливо для молекул всех насыщенных соединений, у которых число пар валентных электронов равно числу возможных двухцентровых взаимодействий. В таких соединениях все химические связи являются простыми связями (с кратностью, равной единице). Пара электронов простой связи в равной степени может иметь и донорно-акцепторное происхождение (см. Донорно-акцепторная связь). Поэтому, например, изоэлектронные молекула CH4 и ионы 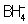 и
и 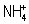 могут быть описаны однотипной структурной формулой
могут быть описаны однотипной структурной формулой
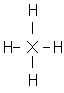
(где Х = В-, С и N+ соответственно).
В химических соединениях, в которых среднее число электронов, связывающих каждую пару атомных ядер, не равно двум, могут возникнуть химические связи самой различной кратности — как меньше единицы (соединения с дефицитом электронов), так и больше единицы (соединения с кратными связями). В этих случаях описание электронного строения молекул обычно требует привлечения наиболее общего метода квантовой химии — молекулярных орбиталей метода.
Е. М. Шусторович.
