Эбулиоскопия
ЭБУЛИОСКОПИЯ, физ.-хим. метод исследования жидких р-ров нелетучих в-в, основанный на измерении повышения т-ры кипения р-ра по сравнению с т-рой кипения чистого р-рителя. Для разб. р-ров это повышение определяется из соотношения:
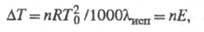
где п - число молей растворенного в-ва; R - газовая постоянная; Т0 и - соотв. т-ра кипения и уд. теплота испарения чистого р-рителя. Величина Е = RT20 /1000
- соотв. т-ра кипения и уд. теплота испарения чистого р-рителя. Величина Е = RT20 /1000 наз. эбулиоскопич. постоянной.
наз. эбулиоскопич. постоянной.
Для р-ров электролитов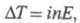 где i = 1 + (v - 1)
где i = 1 + (v - 1)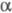 ;
;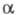 - степень диссоциации; v - число ионов, на к-рые распадается молекула электролита.
- степень диссоциации; v - число ионов, на к-рые распадается молекула электролита.
Эбулиоскопию используют для определения мол. массы растворенного в-ва, степени диссоциации слабых электролитов. Эбулиоскопия требует очень точных определений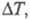 к-рые осложняются склонностью р-ров к перегреву, изменением концентрации в результате испарения р-рителя и др. Вследствие этого эбулиоскопия получила меньшее распространение, чем криоскопия.
к-рые осложняются склонностью р-ров к перегреву, изменением концентрации в результате испарения р-рителя и др. Вследствие этого эбулиоскопия получила меньшее распространение, чем криоскопия.

Дополнения к описанию эбулиоскопии: