Бария гидроксид
БАРИЯ ГИДРОКСИД Ва(ОН)2, бесцв. кристаллы. При т-рах от -273 до 246°С устойчива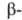 модификация; при 246-408 °С-
модификация; при 246-408 °С-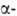 модификация (в обоих случаях решетка ромбическая);
модификация (в обоих случаях решетка ромбическая);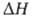 перехода
перехода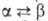 3,6 кДж/моль. Т. пл. 408 °С; Сp° 98,00 Дж/(моль*К);
3,6 кДж/моль. Т. пл. 408 °С; Сp° 98,00 Дж/(моль*К);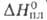 16 кДж/моль;
16 кДж/моль;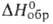 - 941,60 кДж/моль; So298 108,50 Дж/(моль*К). При нагр. разлагается на ВаО и Н2О, ок. 800°С полностью разлагается до ВаО; ур-ния температурной зависимости давления пара: над твердым бария гидроксидом lgp(na)= 14,892-184964/19,1557; над жидким lg р (Па) = 9,847-118767/19,155 Т. Р-римость в воде (г в 100 г): 1,65 (20°С), 3,76 (40°C), 17,65 (60°С). Насыщ. водный р-р наз. баритовой водой. Бария гидроксид гигроскопичен. Не раств. в спирте. В расплаве Ва(ОН)2 растворяется ВаО. Бария гидроксид-сильное основание; водные р-ры поглощают СО2 из воздуха. При обычных уловиях бария гидроксид существует в виде октагидра та с т. пл 78°С, плотн. 2,18 г/см3; давление пара при 78°С 30,3 кПа; ур-ние температурной зависимости давления диссоциации: lg р (Па) = 13,238 - 58230/19,1557: При 130°С полностью обезвоживается; при упаривании кипящих водных р-ров бария гидроксида в отсутствие СО2 образуется моногидрат. Получают октагидрат действием горячей воды на ВаО, нагреванием BaS в токе влажного СО2 и перегретого пара, взаимод. р-ров ВаС12 и NaOH при кипении.
- 941,60 кДж/моль; So298 108,50 Дж/(моль*К). При нагр. разлагается на ВаО и Н2О, ок. 800°С полностью разлагается до ВаО; ур-ния температурной зависимости давления пара: над твердым бария гидроксидом lgp(na)= 14,892-184964/19,1557; над жидким lg р (Па) = 9,847-118767/19,155 Т. Р-римость в воде (г в 100 г): 1,65 (20°С), 3,76 (40°C), 17,65 (60°С). Насыщ. водный р-р наз. баритовой водой. Бария гидроксид гигроскопичен. Не раств. в спирте. В расплаве Ва(ОН)2 растворяется ВаО. Бария гидроксид-сильное основание; водные р-ры поглощают СО2 из воздуха. При обычных уловиях бария гидроксид существует в виде октагидра та с т. пл 78°С, плотн. 2,18 г/см3; давление пара при 78°С 30,3 кПа; ур-ние температурной зависимости давления диссоциации: lg р (Па) = 13,238 - 58230/19,1557: При 130°С полностью обезвоживается; при упаривании кипящих водных р-ров бария гидроксида в отсутствие СО2 образуется моногидрат. Получают октагидрат действием горячей воды на ВаО, нагреванием BaS в токе влажного СО2 и перегретого пара, взаимод. р-ров ВаС12 и NaOH при кипении.
Применяют бария гидроксид как реактив на SO42- и CO32-, для очистки растит. масел и животных жиров, как компонент смазок, для удаления SO42- из пром. р-ров, получения солей Ва, а также гидроксидов Cs, Rb из их сульфатов или карбонатов. Бария гидроксид токсичен; ПДК 0,5 мг/м3.
Литература
АхметовТ.Г, Химия и технология соединений бария, М., 1974; АхметовТ.Г., ЛисинаН.В., Аналитические методы контроля производства бариевых и сульфитных солей, М., 1974. Т. Г. Ахметов.
