Свинца сульфаты
СВИНЦА СУЛЬФАТЫ. Сульфат свинца(II) PbSO4-бесцв. кристаллы; до 878 °С существует a-PbSO4 с ромбич. решеткой (а = 0,8480 нм, b = 0,5938 нм, с - 0,6958 нм, z = 4, пространств, группа Рпта), выше 878 °С-моноклинная форма p-PbSO4; DH полиморфного перехода 17,0 кДж/моль; т.пл. 1170°С, выше т-ры плавления разлагается с образованием SO2, O2, оксисульфатов Рb и затем РbО; плотн. 6,35 г/см3; 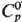 103,29 Дж/(моль·К);
103,29 Дж/(моль·К); 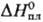 40,2 кДж/моль,
40,2 кДж/моль, 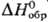 —921,20 кДж/моль;
—921,20 кДж/моль;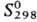 148,71 ДжДмоль·К); показатели преломления: больший Ng 1,8937, средний Nm 1,8826, меньший Np 1,8771. Р-римость (г в 100 г): в воде-0,0045 (25°С), 0,0057 (50°С); в р-ре 5% Н2О-95% H2SO4-0,080 (25 °С). Раств. в водных р-рах ацетата и тартрата NH4, щелочей, горячей H2SO4, не раств. в этаноле. Углем и Н2 восстанавливается до PbS. Реагирует с PbS с образованием Рb и SO2, эта р-ция (наряду с другими) протекает при выплавке Рb из сульфидных руд. Образует основные сульфаты (3РbО · PbSO4 · Н2О, РbО · PbSO4 и др.), двойные сульфаты [K2Pb(SO4)2 и др.]. В природе встречается минерал англезит a-PbSO4.
148,71 ДжДмоль·К); показатели преломления: больший Ng 1,8937, средний Nm 1,8826, меньший Np 1,8771. Р-римость (г в 100 г): в воде-0,0045 (25°С), 0,0057 (50°С); в р-ре 5% Н2О-95% H2SO4-0,080 (25 °С). Раств. в водных р-рах ацетата и тартрата NH4, щелочей, горячей H2SO4, не раств. в этаноле. Углем и Н2 восстанавливается до PbS. Реагирует с PbS с образованием Рb и SO2, эта р-ция (наряду с другими) протекает при выплавке Рb из сульфидных руд. Образует основные сульфаты (3РbО · PbSO4 · Н2О, РbО · PbSO4 и др.), двойные сульфаты [K2Pb(SO4)2 и др.]. В природе встречается минерал англезит a-PbSO4.
Получают PbSO4 осаждением из р-ров солей Pb(II) ионами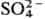 , окислением PbS, напр. H2О2. Применяют PbSO4 для заполнения ячеек пластин в свинцовых аккумуляторах, как компонент лаков и пигментов; РbО · PbSO4 и 3РbОx xPbSO4·H2O-добавки к цинковым и свинцовым белилам (для повышения устойчивости покрытий). Известен гидросульфат Pb(HSO4)2,
, окислением PbS, напр. H2О2. Применяют PbSO4 для заполнения ячеек пластин в свинцовых аккумуляторах, как компонент лаков и пигментов; РbО · PbSO4 и 3РbОx xPbSO4·H2O-добавки к цинковым и свинцовым белилам (для повышения устойчивости покрытий). Известен гидросульфат Pb(HSO4)2,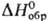 -1825,1 кДж/моль.
-1825,1 кДж/моль.
Сульфат свинца(IV) Рb(SО4)2-желтоватые кристаллы; разлагается при нагр.; гидролизуется водой с образованием Pb(OH)2SO4 и затем РbО2·xН2О; плохо раств. в горячей конц. H2SO4; образует двойные сульфаты M2Pb(SO4)3; сильный окислитель; получают в виде осадка при электролизе 80%-ной H2SO4 со свинцовыми электродами.
Свинца сульфаты токсичны; ПДК 0,01 мг/м3 (в пересчете на Рb).
И. Н. Один.
