Скорость реакции
СКОРОСТЬ РЕАКЦИИ, скорость хим. превращения исходных в-в в продукты р-ции. В случае гомог. элементарной р-ции vAA + vBB : vVV + vZZ, где VA, VB, vV и VZ-сте-хиометрич. коэф. реагентов А и В и продуктов V и Z соотв., в замкнутом постоянном объеме V реагент А исчезает со скоростью uА = — d[А]/dt(t-время), а продукт Z появляется со скоростью uZ = d[Z]/dt. Скорость реакции определяется выражением:
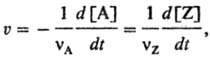
т. е. не зависит от того, по какому реагенту или продукту ее измеряют. Если в ходе р-ции изменяется объем V системы, v измеряют по изменению концентрации одного из в-в:
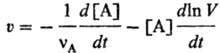
При постоянном объеме за протеканием р-ции можно следить, измеряя число молей nА прореагировавшего в-ва и определяя глубину протекания р-ции Dx = DnА/vА; в этом случае
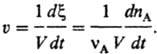
Для сложной р-ции (т.е. состоящей из ряда отдельно не наблюдаемых элементарных стадий) описание скорости реакции исходит из непосредственно определяемых хим. анализом или к.-л. другим способом изменений кол-в в-в. Наиб. просто скорость реакции, протекающей стационарно, определяют в проточном безградиентном реакторе, в к-ром концентрации в-в и т-ра одинаковы по всему реакц. пространству (напр., благодаря перемешиванию или рециркуляции). В указанных условиях скорость реакции по в-ву Вm (m-номер в-ва) определяется выражением uBm = nBm/tV, где nBm-число молей в-ва Вm, образовавшегося за время г в реакц. объеме V, если р-ция гомогенна, или на пов-сти площадью f, если она гетерогенна (если Вm- исходное в-во, nBm < 0). В общем случае скорость реакции uBm различна в разных участках пространства и изменяется со временем, для ее определения пользуются соотношением:
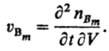
Скорости образования (расходования) всех в-в, участвующих в р-ции, взаимосвязаны. Если р-ция описывается одним хим. ур-нием 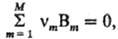 к-рое представляет собой выражение закона сохранения в-ва (М-общее число реагентов и продуктов), скорость реакции по каждому в-ву uBm пропорциональна его стехиометрич. коэф. vm (положительному для исходных в-в):
к-рое представляет собой выражение закона сохранения в-ва (М-общее число реагентов и продуктов), скорость реакции по каждому в-ву uBm пропорциональна его стехиометрич. коэф. vm (положительному для исходных в-в):
uBm=vmu
Одинаковое для всех участвующих в р-ции в-в отношение uBm/vm=u есть, по определению, скорость реакции.
Если стехиометрия р-ции описывается неск. хим. ур-ниями, к-рые линейно независимы, т.е. любое др. хим. ур-ние является их линейной комбинацией, эти ур-ния полностью задают стехиометрию р-ции, их можно считать базисными. Число Q базисных ур-ний связано с числом М всех в-в в системе и числом с независимых компонентов, изменения масс к-рых выражают все возможные изменения в составе системы (см. Многокомпонентные системы) соотношением:
Q = М - с.
Природой р-ции однозначно определено только число Q базисных ур-ний, выбор их м. б. сделан по-разному (Q следует отличать от числа P базисных маршрутов сложной р-ции-понятия, относящегося к механизму, а не к стехиометрии р-ции; всегда P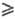 Q). Пусть р-ция описывается Q базисными хим. ур-ниями где
Q). Пусть р-ция описывается Q базисными хим. ур-ниями где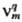 -стехиометрич. коэффициент в-ва Вm в
-стехиометрич. коэффициент в-ва Вm в 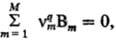 ур-нии номер q (положит., отрицат. или равный нулю).
ур-нии номер q (положит., отрицат. или равный нулю).
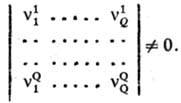
Скорость реакции может быть охарактеризована скоростями образования т. наз. ключевых в-в B1, B2, ..., BQ, для к-рых определитель, составленный из соответствующих стехиометрич. коэф., отличен от нуля:
Скорости образования всех в-в, участвующих в р-ции,-линейные ф-ции стехиометрич. коэффициентов 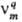 :
:
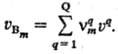
Зная uq, посредством этой системы ур-ний получаем скорости образования остальных (М — Q)в-в. Величины u(q) естественно считать скорость реакции по соответствующим хим. ур-ниям. Но следует при этом учитывать, что они имеют определенное значение лишь применительно ко всей данной совокупности базисных хим. ур-ний р-ции.
Для практич. целей скорости образования в-в при гетерог. катализе обычно относят не к единице пов-сти катализатора, а к массе или к объему слоя каталитич. зерен.
Приведенные определения отвечают общепринятому в хим. кинетике пониманию скорости реакции как интенсивной величины. Иногда, по преимуществу в литературе по хим. термодинамике, используют предложенное де Донде определение скорости реакции, согласно к-рому она служит экстенсивной величиной. Для р-ции, описываемой одним хим. ур-нием, скорость реакции
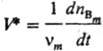
Экстенсивную величину V* удобнее называть производительностью (реактора, зерна катализатора, в зависимости от рассматриваемой зоны р-ции). Тогда скорость реакции v -плотность производительности или, в случае гетерог. р-ции, поверхностная плотность производительности. М. И. Темкин.
