Амфотерность
АМФОТЕРНОСТЬ (от греч. amphoteros-и тот и другой), способность хим. соед. проявлять кислотные или основные св-ва в зависимости от природы второго компонента, участвующего в кислотно-основном взаимодействии. Одно и то же в-во, реагируя с сильной к-той, имеет тенденцию проявлять основные св-ва, а при р-ции с сильным основанием-кислотные. Так, при взаимод. C6H5NH2 с НС1 образуется катион С6Н5NН+3, а при р-ции с KNH2 - анион C6H5NH-. Типичные амфотерные соединения-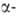 аминокислоты, нек-рые гидроксиды, напр. А1(ОН)3, Fe(OH)3; к амфотерным электролитам, или амфолитам, относятся соединения, способные присоединять или отщеплять протоны, превращаясь соотв. в катионы или анионы.
аминокислоты, нек-рые гидроксиды, напр. А1(ОН)3, Fe(OH)3; к амфотерным электролитам, или амфолитам, относятся соединения, способные присоединять или отщеплять протоны, превращаясь соотв. в катионы или анионы.
*Подобраны с помощью LLM, верифицированы, но возможны неточности.
Ещё по теме
Амфотерность — определение и примеры
Аммония фторид — характеристики и свойства
Аммоний в химии — свойства и реакции
Кислоты и основания — свойства и роль в природе
Аммония гексафторалюминат — основные характеристики
Коллоидные ПАВ и их свойства
Активность
Свойства аминокислот и их кислотно-основные характеристики
Гидросульфат аммония — основные характеристики
Аммония гидроортофосфат — характеристики и свойства
Кислоты и основания в химии — теории и применение
Аммония хлорид — характеристики и применение

Дополнения к описанию амфотерности: