Озониды неорганические
ОЗОНИДЫ НЕОРГАНИЧЕСКИЕ, ярко-красные твердые соед. общей ф-лы М(О3)n, где п заряд катиона М. Ион О-3 имеет симметричную треугольную конфигурацию; в молекуле RbO3 длина связи О—О 0,134 нм, угол ООО 114°, в молекуле [(CH3)4N]O3 длина связи О—О 0,1286 нм, угол ООО 119,5°. Все озониды парамагнитны, термически малостабильны. Стабильность наиб. устойчивых озонидов убывает в ряду [(CH4)3N]O3 > CsO3 > RbO3 > КО3 (см. табл.). Озониды щел.-зем. металлов распадаются в интервале от - 30 до О °С. Озонид лития, известный только в виде аммиаката [Li(NH3)4]O3, неустойчив уже при -78 °С; NH4O3 устойчив ниже -126°С. Озониды магния, серебра и др. металлов идентифицированы методом матричной изоляции в твердом Аг или N2. Первичные продукты распада озонидов-супероксиды, р-ция МО3 МО2 + 1/2 О2 экзотермична.
МО2 + 1/2 О2 экзотермична.
Озониды гигроскопичны и бурно реагируют с водой с образованием О2 и щелочного р-ра Н2О2; при этом промежуточно образуются своб. радикалы ОН* в высокой концентрации. С парами воды р-ция идет медленнее - при 50%-ной влажности и 24 °С КО3 полностью гидролизустся за 30 ч. В присут. водяных паров КО3 количественно реагирует с СО2, образуя К2СО3 и выделяя кислород. Озониды-активные окислители; взаимод. с большинством орг. р-рителей. В инертных и неполярных средах, напр. хладонах, озониды не раств.; хорошо раств. в жидком NH3, на чем основан метод их выделения и очистки.
Получают озониды действием О3 на гидроксиды или супероксиды металлов в среде хладона или в кипящем слое. Тонкий слой озонидов, образовавшийся на пов-сти кристаллов исходного в-ва, экстрагируют жидким NH3, после чего р-ритель упаривают. Озониды щелочных металлов могли бы быть эффективными ср-вами регенерации О2 и высокоемкими кислородоносителями, но из-за низкой их термич. стабильности и трудной доступности практич. применения не нашли.
СВОЙСТВА ОЗОНИДОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ
| Показатель | NaO3 | К03 | RbO3 | Cs03 | ||
| Сингония | Тетрагон. | Тетрагон. | Моноклинная | Моноклинная* | ||
| Пространств. группа | 14/ттт | I4/тст | Р21/с | Р21/c | ||
| Рентгеновская плотн., г/см3 | | 2,16 | 3,08 | 3,65 | ||
| | -193 | -261 | -264 | -271 | ||
| Т. разл., °С | -10 | 60 | 70 | 80 | ||
| Энтальпия р-ции МO3 кДж/моль | -67 | -22 | -15 | -15 | ||
| Р-римость в жидком NH3, г в 100 г | - | 14,8 (-35°С) | 4,3 (-82°С) | | ||
* Устойчива ниже 8°С, выше 8 °С - кубическая.
Лит.: Токарева С. А., "Успехи химии", 1971, т. 40, в. 2, с. 295-311.
В. Я. Росоловский.

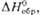 кДж/моль
кДж/моль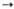 МO2 +
МO2 + 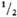 О2,
О2,