7.3. Реакции атмосферных ионов
Образующиеся молекулярные ионы обладают очень большой реакционной способностью, быстро реагируют с любыми другими частицами при столкновении, эти реакции также носят экзотермический характер. Но так как при высоком разряжении отдача избыточной энергии маловероятна, то более вероятна рекомбинация иона с электроном, сопровождающаяся диссоциацией:
N2+ + 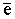 ® N (г) + N (г) ;
® N (г) + N (г) ;
O2+ + 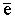 ® O (г) + O (г) ;
® O (г) + O (г) ;
NO+ + 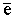 ® N (г) + O (г) .
® N (г) + O (г) .
Такие реакции называются реакциями диссоциативной рекомбинации. Атомарный азот в верхних слоях атмосферы образуется исключительно в результате такой реакции.
Перенос заряда. Когда молекулярный ион сталкивается с какой-либо нейтральной частицей, между ними может произойти перенос электрона: N2+ (г) + О2 (г) ® N2 (г) + О2+ (г). Это возможно, если Е1(O2)< E2(N2), то есть энергия ионизации молекулы, теряющей электрон, должна быть меньше энергии молекулы, приобретающей электрон (реакция должна быть экзотермическая).
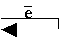
О+(г) + О2(г) ® О (г) + О2+ (г);
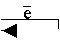
 О2+(г) + NО (г) ® О2 (г) + NО+ (г);
О2+(г) + NО (г) ® О2 (г) + NО+ (г);
|
 N2+(г) + NО (г) ® N2 (г) + NО+ (г) .
N2+(г) + NО (г) ® N2 (г) + NО+ (г) .
Реакции переноса заряда играют большую роль во многих областях химии, особенно в биохимии. Реакции переноса заряда не сопровождаются разрывом химических связей, осуществляется только перенос электрона от одной частицы к другой. Но существует класс реакций в атмосфере, в ходе которых частицы обмениваются атомами:
O+ (г) + N2 (г) ® N (г) + NО+ (г) ;
N2+ (г) + О (г) ® N (г) + NО+ (г) .
Эти реакции являются экзотермическими и протекают очень легко, при этом образуется молекулярный ион NО+ (г). Поскольку энергия ионизации NО самая низкая из всех частиц, находящихся в верхних слоях атмосферы, то NО+ (г)не может ничем нейтрализоваться и этот ион является преобладающим в данной области. Таким образом, молекулы N2, О2 и NО отфильтровывают большую часть опасного (жесткого) ультрафиолетового излучения на высоте около 100 км.
На высоте более 30 км фотодиссоциация кислорода остается (реакция 1). В мезосфере и стратосфере концентрация молекулярного кислорода превышает концентрацию атомарного кислорода, поэтому образующиеся атомы часто сталкиваются с молекулами О2, что приводит к образованию озона:
О (г) + О2(г) « О3* + 105 кДж/моль.
Эта реакция обратима и если частица О3* не отдает избыточную энергию при столкновении с другой (N2 и О2), то молекула распадется. Чем ниже к Земле, тем больше концентрация газов N2 и О2, тем чаще столкновение и стабилизация озона. Но опять же, чем ниже, тем меньше диссоциация О2 на атомы, так как отфильтровано излучение с длиной волны 242 нм. Максимальная скорость образования озона на высоте 50 км, так как мало атомов кислорода и, следовательно, мало озона.
Молекулы озона сами могут поглощать излучение, и сильнее всего озоном поглощаются фотоны с длиной волны 200 - 310 нм, что очень важно для нас. Это излучение другими частицами не поглощается в той мере, как озоном. При таком излучении все живое не может существовать. «Озоновый щит» играет важную роль в сохранении жизни на Земле.
Обобщенный процесс циклического образования и разложения озона:
О2 (г) + hn® О (г) + О (г) ;
О2 (г) +О (г) + М (г) ® О3 (г) + М* (г) + выделение тепла ;
О3 (г) + hn® О2 (г) + О (г) ;
О (г) + О (г) + М (г) ® О2 (г) + М* (г) + выделение тепла .
М* - любая частица в столкновении.
Результатом данного процесса является превращение ультрафиолетового излучения Солнца в тепловую энергию. Озоновый цикл обеспечивает повышение температуры в стратосфере (рис. 7.1). В этот цикл вовлекаются многие химические реакции; общим результатом является разложение озона, например:
О3(г) + NO(г) ® NО2(г) + О2(г)
NО2(г) + O(г) ® NО(г) + О2(г)
------------------------------------------
О3(г) + О(г) ® 2 О2(г)
NO является катализатором процесса. Когда в этот цикл вторгаются дополнительные порции оксида азота, значительно уменьшается концентрация озона. Так, при полете сверхзвуковых самолетов в двигателях достигается такая высокая температура, что становится возможной реакция: N2 (г) +O2 (г) ® 2 NО (г), в результате которой оксид азота выбрасывается в стратосферу, существенно снижая концентрацию озона.
Разрушение озона обусловлено также влиянием фторхлорметанов:
CFxCl4-–x (г)+ hn® CFxCl3–x (г)+ Cl(г), l = 190 – 225 нм.
За этим следует разложение CFxCl3–x и т.д. Расчеты показывают, что скорость образования атомарного хлора максимальна на высоте 30 км.
Cl(г) + О3 (г)® ClО(г) + О2 (г) (разрушение озона)
Оксид хлора, реагируя с атомарным кислородом, вновь дает атомарный хлор: ClО (г) + О (г) ® Cl (г)+ О2(г); снова Cl(г) + О3 (г)® ClО(г) + О2 (г)... обрыв цепи может происходить при взаимодействии хлора с молекулами водорода, метана, воды, пероксида водорода. В итоге имеем суммарную реакцию: О (г) + О3 (г) ® 2 О2(г).
Фреоны очень хорошо сохраняются в атмосфере, плохо растворимы в воде, не горят, имеют низкие температуры кипения, поэтому хорошо испаряются на воздухе. Из тропосферы часть фреонов может уходить с водой и, не гидролизуясь, скапливаться в океане, который становится своеобразным резервуаром фреонов.
Постоянно возникающий и разрушающийся слой озона вызывает явление, названное «озонным дождем». Концентрация озона должна быть максимальной на высоте 25 – 30 км. В атмосфере с увеличением высоты концентрация озона убывает из-за концентрации третьих частиц и кислорода. Разрушение озона в основном обусловливает азотный цикл, антропогенное загрязнение атмосферы:
· Ядерные взрывы. Разогрев до 6000 К и быстрое охлаждение (замораживание NO). 1 Мт при взрыве дает от 1000 до 12000 тонн оксидов азота (2,5·1032 молекул).
· Сверхзвуковые самолеты (18 г NO на 1 кг топлива). 1 млн тонн оксидов азота в год выбрасывают двигатели сверхзвуковых самолетов.
· Использование минеральных азотных удобрений.
· Сжигание топлива дает до 3 млн тонн оксидов азота в год.
В химии и фотохимии атмосферы участвуют пять основных азотсодержащих газов: N2, NH3, NO, NO2, N2O. В конденсированной фазе азот присутствует в форме иона аммония (NH4+) и нитратного иона (NO3–). Возможные взаимодействия можно описать следующей схемой:
2 NO + O2® 2 NO2 ;
NO2 + hn® NO + O ;
O + O2 + M ® O3 + M ;
O3 + NO ® NO2 + O2 ;
O + NO2® NO + O2 ;
O + NO2 + M ® NO3 + M ;
NO3 + NO ®2 NO2 ;
NO2 + O3® NO3 + O2 ;
O + NO + M ® NO2 + M ;
NO3 + NO2 + M ® N2O5 + M,
где М - третье вещество, принимающее избыток энергии. Цикл взаимодействий на основе соединений азота в тропосфере дополняется образованием азотной кислоты: 4 NO2 + 2 H2O + O2® 4 HNO3 или по реакции диспропорционирования 3 NO2 + H2O « 2 HNO3 + NO.
Атомарный кислород и озон способны вступать в реакции с различными органическими веществами, в результате чего получаются свободные радикалы. Так, для олефинов возможна следующая реакция:
O3 + R–CH=CH–R ® RCHO + RO* + HCO*,
где RO* и HCO* - свободные радикалы. Образующийся альдегид RCHO может подвергаться фотодиссоциации по реакции: RCHO + hn® R+HCO*. Кроме альдегидов фотохимически активны также кетоны, пероксиды и ацилнитраты, которые под воздействием солнечной радиации также образуют свободные радикалы. Последующая цепь взаимодействий может быть представлена схемой, где ROO* - пероксидный радикал:
ROO* + NO ® NO2 + RO* ;
ROO* + O2® O3 + RO* ;
RCO*2 + NO ® NO2 + RCO* ;
RCO* + O2® RCO*3 ;
RCO*2 + O2® CO2 + RO*2 ;
RCO*3 + NO2® RCO3NO2 ;
RO* + NO ® RONO ;
RH + RO*® ROH + R* ;
RH* + O ® OH– + R* .
Эта цепь превращений с участием свободных радикалов является основой для образования смога, содержащего ассоциации молекул альдегидов, кетонов, оксидантов и соединений типа пероксиацетилнитратов (ПАН).
Пероксиацетилнитрат: О
||
CH3 – C – O – O – NO2 - это газ, сильно раздражающий слизистую оболочку глаз и отрицательно действующий на ассимиляционный аппарат растений.
Другим веществом, также сильнодействующим на слизистую оболочку глаз, присутствующим в смоге, является пероксибензолнитрат (ПБН), имеющий следующую структуру: О
||
C6H5 – C – O – O – NO2.
Антропогенная деятельность и вулканические извержения приводят к накоплению в атмосфере SO2. Фотодиссоциация диоксида серы невозможна, так как длина волн, которые достигают нижних слоев атмосферы, где происходит накопление SO2, слишком велика, жесткое коротковолновое излучение уже отфильтровано. Однако фотодиссоциация NO2 и кислорода дает на данной высоте достаточное количество атомарного кислорода и озона (см. выше) и тогда возможен процесс: SO2 + О + М ® SO3 + М. Эффективность этой реакции возрастает по мере увеличения отношения концентрации SO2 к концентрации NO2. Окислению SO2 до SO3 могут способствовать следы металлов, проявляющих каталитическое действие на данную реакцию (например, марганец). Соединяясь с водой, оксид серы (VI) образует серную кислоту, которая с металлами или аммонием (NH4+) дает сульфаты.
Имеется мнение, что диоксид серы существует в атмосфере от нескольких часов до нескольких дней в зависимости от влажности и других условий. Однако установлено, что сернистый газ, поступающий в атмосферу с извержением вулканов, дает серную кислоту, циркулирующую вокруг Земли в стратосфере сроком до года и более. Так, вследствие извержения вулкана Эль-Чичон на юге Мексики 28 марта 1982 года, земной шар опоясал «язык» стратосферного аэрозольного облака, содержащий капельки серной кислоты размером от 0,04 мкм до 1,4 мкм, готовых выпасть в виде сернокислого дождя. Через месяц после извержения в стратосфере путешествовало почти 20 млн. тонн аэрозоля серной кислоты. Даже через год после извержения в апреле 1983 года около 8 млн. тонн серной кислоты еще находилось на околоземной орбите.
Переносу диоксида серы на дальние расстояния способствует строительство высоких дымовых труб. Это возможно и снижает степень локального загрязнения, но увеличивает время пребывания SO2 в воздушной среде и степень его превращения в серную кислоту и сульфаты. Таким образом, сернистый газ в сочетании с парами воды (туман) является главным компонентом так называемого сернистого смога (смог лондонского типа).
Кислотные дожди. В результате антропогенного загрязнения атмосферы сернистым газом и оксидами азота происходит, как показано выше, образование серной и азотной кислот, выпадающих на Землю вместе с осадками. Кислотность обычной дождевой воды за счет частичного растворения во влаге углекислого газа равна 5,6: рН = 5,6. Но известны случаи выпадения кислых дождей с рН = 2,3 (кислотность лимонного сока!). Такие осадки наносят существенный ущерб качеству воды в природных водоемах, качеству почвы, приводят к разрушению изделий из металлов, архитектурных сооружений, мрамора и бетона.
Ежегодно с осадками выпадают миллионы тонн кислот, что ведет к радикальному изменению химии природной среды. Частицы сульфатов размером 0,1 - 1 мкм, присутствующие в атмосфере, рассеивают свет, ухудшая видимость, что отрицательно воздействует на организм человека. В условиях повышенной влажности и гигроскопичности некоторых сульфатов: (NH4)2SO4, NH4HSO4 – рассеивание света возрастает.