Фенилфлуорон
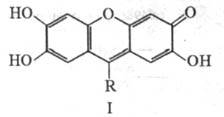
ФЕНИЛФЛУОРОН (2,6,7-тригидрокси-9-фенил-3(ЗH)-ксантенон; ф-ла I, R - фенил), мол. м. 320,30; красно-оранжевые кристаллы, не раств. в воде, раств. в водно-спиртовых р-рах к-т и щелочей, ДМФА. Амфотерен; pKa1 6,3, рКа2 10,2, pKa3 11,7; при рН 1,2 протонирован по карбонильной группе (рКа 2,1). В спектрах поглощения наблюдаются максимумы при следующих длинах волн l (в нм): 462-465 (рН 1,2); 462 и 490-492 (рН 4,8-5,2); 512-514 (рН 8,4-9,0); 532-538 (рН 11,4-12,0); 556-558 (рН
1,2 протонирован по карбонильной группе (рКа 2,1). В спектрах поглощения наблюдаются максимумы при следующих длинах волн l (в нм): 462-465 (рН 1,2); 462 и 490-492 (рН 4,8-5,2); 512-514 (рН 8,4-9,0); 532-538 (рН 11,4-12,0); 556-558 (рН 13,0). Получают фенилфлуорон конденсацией триацетоксигидрохинона (пирогаллола А) с бензальде-гидом в водно-этанольной среде в присут. H2SO4.
13,0). Получают фенилфлуорон конденсацией триацетоксигидрохинона (пирогаллола А) с бензальде-гидом в водно-этанольной среде в присут. H2SO4.
Фенилфлуорон- реагент для фотометрич. определения в водно-этаноль-ных р-рах Ge(IV) (1M HCL, l 530 нм, e 4,0-104), Sn(IV) (0,1М HCl, l 530 нм, e 3,5·104), Ti(IV) (rH 2-2,3, l 540 нм, e 7,4-104), Sb(III) (0,05М H2SO4, l 560 нм, e 3,4-104), Nb(V) (0,3М H2SO4, l 510 нм, e 3,1· 104), Mo(VI) (rH 1, l 578 нм, e 4,9-104). С ионами перечисленных металлов фенилфлуорон образует труднорастворимые в воде окрашенные комплексные соединения. В одно-этанольные р-ры последних стабилизируют защитными коллоидами (желатин, гуммиарабик, поливиниловый спирт). Чувствительность определения увеличивается (e достигает 105 и выше) при введении в эти р-ры ПАВ. Фенилфлуорон-неселективный реагент, поэтому обычно либо предварительно отделяют определяемый элемент, либо применяют маскирующие агенты.
Фенилфлуорон- типичный представитель тригидроксифлуоронов (ок-сиксантеновых красителей) - соединений общей ф-лы I. Они представляют собой красные кристаллы, плавятся с разложением; не раств. в воде, этаноле, раств. в водно-спиртовых р-рах к-т и щелочей. Слабые к-ты; в водно-спиртовых р-рах в зависимости от рН образуют 5 различно окрашенных форм. Аналоги фенилфлуорона: салицилфлуорон (I, R - 2-гидроксифенил), про-пилфлуорон (1, R - пропил), 2-нитрофенилфлуорон (I, R -2-нитрофенил), 2,4-дисульфофенилфлуорон (I, R - 2,4-дису-льфофенил). Применяются для фотометрич. определения Ti(IV), Zr(IV), Hf(IV), Sn(IV), V(IV), Nb(V), Ta(V), Вi(III), Mo(VI), W(VI), с к-рыми образуют комплексные соединения, стабилизированные в водных р-рах защитными коллоидами и ПАВ. Часто перечисленные металлы определяют в виде экстрагированных хлороформом разнолигандных комплексных соед., лигандами в к-рых кроме тригидроксифлуорона являются антипирин, диантипирилметан, N-бензоил-N-фе-нилгидроксиламин и его аналоги. Тригидроксифлуороны используют также для отделения, концентрирования (соосажде-нием) и последующего атомно-эмиссионного и рентгенофлуо-ресцентного определения микроколичеств Ge, РЗЭ, Та, Nb, Zr, Hf, Bi, W и др.
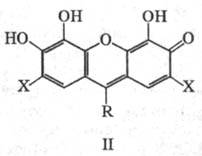
К тригидроксифлуоронам относят также соед. общей ф-лы II, обладающие аналогичными св-вами. Важнейшие представители: галлеин (II, X = H, R - 2-карбоксифенил), пирогалловый красный (П, X = H, R- 2-сульфофенил) и бромпирогалловый красный (II, X = Br, R - 2-сульфофенил). Они применяются в качестве комплексонометрич. индикаторов и для фотометрич. определения Ag(I), РЗЭ, Zr(IV), Sn(IV), Mo(VI) и др. .
Лит.: Назаренко В. А., Антонович В.П., Триоксифлуороны, M., 1973; Антонович В.П. [и др.], "Ж. аналит. химии", 1984, т. 39, в. 7, с. 1157-76; Антонович В.П. [и др.], "Ж. неорг. химии", 1986, т. 31, в. 6, с. 1422-26. В. П. Антонович.
