Электрохимический ряд напряжений
ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЙ, последовательность расположения электродов в порядке возрастания их стандартных электродных потенциалов (см. Стандартный потенциал). Металлич. электроды в водном р-ре электролита образуют след. электрохимический ряд напряжений: Li, К, Rb, Ba, Sr, Ca, Na, Се, Mg, Be, Al, Ti, Mn, V, Zn, Cr, Ga, Fe, Cd, In, Tl, Co, Ni, Sn, Pb, H2, Bi, Cu, Hg, Ag, Pt, O2, Au. Для сравнения включены водородный электрод (Pt, H2[l атм] | Н+ ), потенциал к-рого при давлении водорода 1,01 x 105 Па и термодинамич. активности а ионов Н+ в водном р-ре, равной 1, при всех т-рах принимается равным нулю (потенциалопределяющая р-ция Н+ + е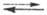 1/2Н2, где е - электрон) и кислородный электрод (потенциалопределяющая р-ция О2 + 2Н2О + 4е
1/2Н2, где е - электрон) и кислородный электрод (потенциалопределяющая р-ция О2 + 2Н2О + 4е 4ОН-).
4ОН-).
Металлы, потенциал к-рых менее положительный, чем у кислородного электрода, термодинамически неустойчивы в контакте с О2 (или воздухом) и водой. Поэтому электрохимический ряд напряжений служит для ориентировочных оценок скорости электрохим. коррозии в водных р-рах при обычных т-рах, а также для выбора безопасных контактных пар (гальванич. пар) разнородных металлов. Если металл электроотрицательнее, чем Н2, то может идти активный коррозионный процесс (см. Коррозия металлов, Коррозионностойкие материалы, Электрохимическая защита). Практич. реализация электродных процессов определяется наряду с термодинамич. также и кинетич. факторами (см. Электрохимическая кинетика).
Положение в электрохимическом ряду напряжений металлов, образующих ионы разного заряда, зависит от природы соответствующих ионов. Аналогичные ряды напряжений можно построить для неметаллич. и редокс-электродов (окислит.-восстановительных).
О. А. Петрий.
