Бутиллитий
БУТИЛЛИТИЙ C4H9Li, мол. м. 57,11. Практич. значение имеют н-бутиллитий и втор-бутиллитий - бесцв. вязкие жидкости, получаемые из измельченного металлич. Li и соотв. н- и втор-бутилхлоридов.
н-Бутиллитий: перегоняется ок. 80°С в вакууме (10-3-10-4 мм рт. ст.); не кристаллизуется до — 76 °С; d425 0,765: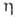 34,6 мПа*с (25°С);
34,6 мПа*с (25°С);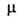 4,77*10-30 и 7,58*10-36 Кл*м (соотв. в бензоле и гексане); подобно др. литийорг. соединениям бурно реагирует с водой и О2 воздуха; в углеводородных р-рах сильно ассоциирован (степень ассоциации ~ 6); при комнатной т-ре в углеводородах стабилен, в эфирах распадается с образованием алкоксидов.
4,77*10-30 и 7,58*10-36 Кл*м (соотв. в бензоле и гексане); подобно др. литийорг. соединениям бурно реагирует с водой и О2 воздуха; в углеводородных р-рах сильно ассоциирован (степень ассоциации ~ 6); при комнатной т-ре в углеводородах стабилен, в эфирах распадается с образованием алкоксидов.
Синтезируют н-бутиллитий в гексане или гептане (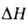 340-360 кДж/моль; выход почти количественный). Для повышения скорости р-ции увеличивают степень измельчения Li, удаляют с его пов-сти образующийся LiCl, используют смесь Li и Na. При высоком содержании Na в этой смеси идет р-ция Li + Na + RC1 -> RLi + NaCl, благодаря к-рой сводится к минимуму непроизводительный расход Li.
340-360 кДж/моль; выход почти количественный). Для повышения скорости р-ции увеличивают степень измельчения Li, удаляют с его пов-сти образующийся LiCl, используют смесь Li и Na. При высоком содержании Na в этой смеси идет р-ция Li + Na + RC1 -> RLi + NaCl, благодаря к-рой сводится к минимуму непроизводительный расход Li.
н-Бутиллитий - наиб. распространенный инициатор анионной полимеризации, применяемый (обычно в виде р-ров, образующихся при его получении) в произ-ве СК и нек-рых других синтетич. полимеров. Р-ры н-бутиллития хранят в закрытых сосудах из стекла или нержавеющей стали в вакууме или в аргоне.
втор-Бутиллитий: d425 0,783;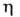 20,1 мПа*с (25,4°С); термически менее стабилен, чем н-бутиллитий (при комнатной т-ре постепенно распадается на LiH и смесь 1- и 2-бутенов), образует менее прочные ассоциаты (степень ассоциации ~4), благодаря чему обеспечивает большую скорость инициирования полимеризации, что важно для получения полимеров, более однородных по ММР, составу, размеру блоков и др. Используется в синтезе бутадиен-стирольных термоэластопластов, полимеров с узким ММР и др.
20,1 мПа*с (25,4°С); термически менее стабилен, чем н-бутиллитий (при комнатной т-ре постепенно распадается на LiH и смесь 1- и 2-бутенов), образует менее прочные ассоциаты (степень ассоциации ~4), благодаря чему обеспечивает большую скорость инициирования полимеризации, что важно для получения полимеров, более однородных по ММР, составу, размеру блоков и др. Используется в синтезе бутадиен-стирольных термоэластопластов, полимеров с узким ММР и др.
