Физические свойства предельных углеводородов (алканов)
Согласно теории химического строения, физические свойства веществ зависят от их состава и строения. На примере предельных углеводородов мы впервые встречаемся с изменениями физических свойств в одном гомологическом ряду.
Четыре первых члена гомологического ряда предельных углеводородов, начиная с метана, являются веществами газообразными. Сам метан является постоянным газом, сгущающимся в жидкость лишь при температуре —161,5° С. У последующих членов ряда температура кипения возрастает от гомолога к гомологу. Начиная с пентана и выше, нормальные углеводороды представляют собой жидкости, причем у средних гомологов с увеличением молекулярного веса температура кипения при переходе к следующему гомологу возрастает приблизительно на 25—30° С. Эта гомологическая разность температур кипения медленно уменьшается с увеличением молекулярного веса.
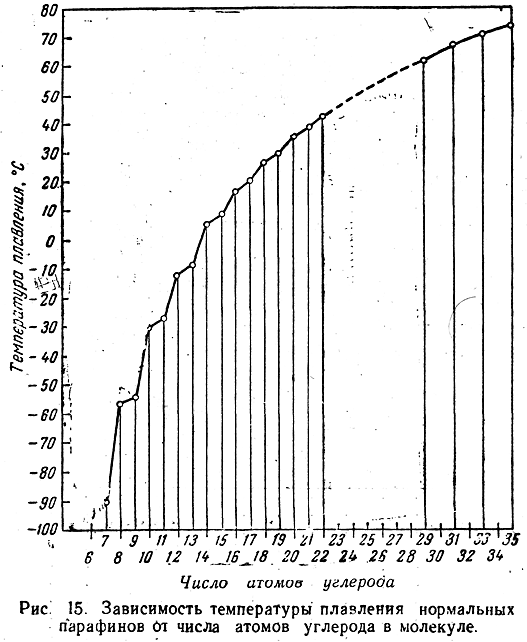
Закономерности в изменении температуры плавления нормальных углеводородов с нарастанием молекулярного веса (числа атомов углерода в молекуле) видны из рис. 15. Температура плавления нормальных углеводородов в гомологическом ряду увеличивается медленно..
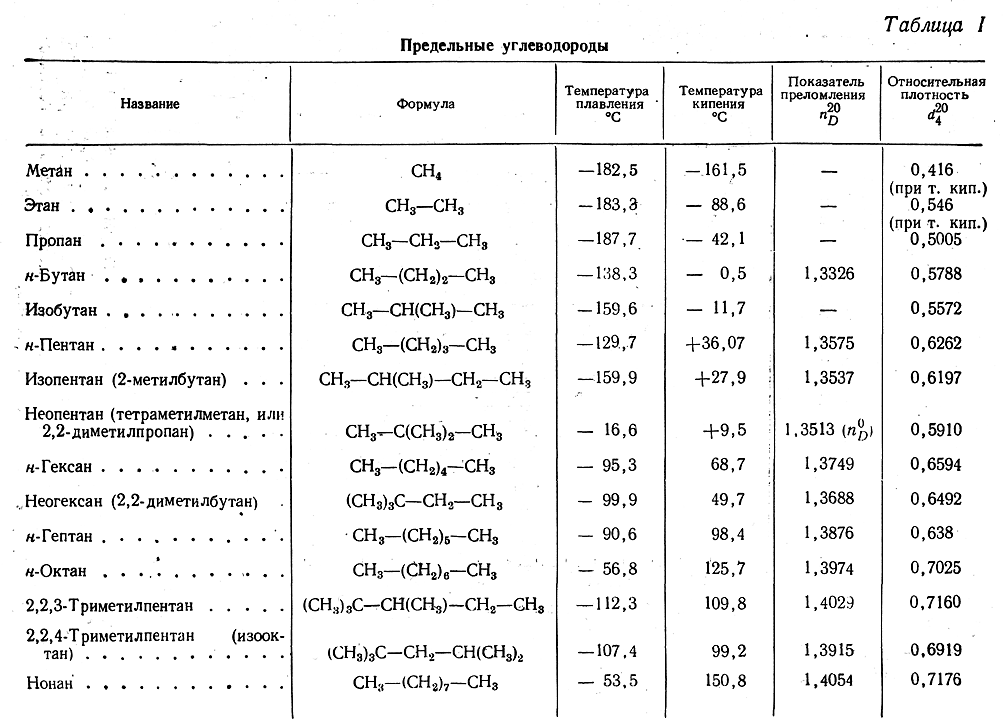

Относительная плотность углеводородов при их температурах кипения увеличивается сначала быстро, а затем все медленнее — от 0,416 у метана до величины несколько большей 0,78.
Начиная с углеводорода C16H34, высшие гомологи при обычной температуре — вещества твердые.
Правильности в изменении некоторых свойств выступают особенно четко, если эти свойства относить не к грамму, а к грамм-молекуле вещества. Так, молярный объем, получающийся при умножении молекулярного веса М на удельный объем 1/плотность
, т. е. величина M/d при переходе от каждого предыдущего гомолога к последующему правильно изменяется на величину, в среднем близкую к 17. Аналогично молярную теплоту горения предельных углеводородов можно вычислить, исходя из молярной теплоты горения метана, равной 212 ккал, прибавляя 158 ккал на каждую группу СН2.
Температуры кипения всех изоалканов ниже, чем у нормальных алканов, и притом тем ниже, чем более разветвлена углеродная цепь молекулы, как видно, например, из сравнения температур кипения трех изомерных пентанов. Наоборот, температура плавления оказывается самой высокой у изомеров с максимально разветвленной, в особенности симметрично разветвленной, углеродной цепью. Так, из всех изомерных октанов лишь гексаметилэтан (СН3)3С—С(СН3)3 является веществом твердым уже при обыкновенной температуре (т. пл. 100,7°С).


