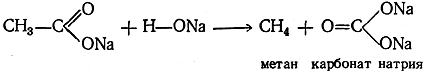Способы получения предельных углеводородов (алканов)
Как было уже сказано, каждый класс органических соединений характеризуется определенными особенностями строения. Мы знаем также, что от строения зависят физические и химические свойства веществ. Следовательно, вещества, принадлежащие к одному классу соединений, должны обладать многими общими или правильно изменяющимися при изменении состава физическими и химическими свойствами. Но не только физические свойства и химически-е реакции, т. е. настоящее и будущее веществ близкого строения, должны иметь много общего; в прошлом таких веществ, т. е. в способах их образования из веществ других классов, также должно быть много общего.
Общие способы получения предельных алифатических углеводородов можно разбить на три группы:
I. Получение из соединений, содержащих в молекуле столько же атомов углерода, сколько их имеется в получаемом углеводороде.
II. Получение из соединений с меньшим числом атомов углерода в молекуле; эти способы можно назвать синтетическими.
III. Получение из соединений с большим числом атомов углерода в молекуле; эти способы относятся к реакциям расщепления молекул.
I. Получение из соединений с тем же числом атомов углерода в молекуле:
1. Получение из производных введением водорода вместо заместителя. Получение углеводородов из соединений с тем же числом атомов углерода, но содержащих, кроме углерода и водорода, другие атомы или группы, т. е. получение углеводородов из их производных, очевидно, должно состоять в замене этих атомов или групп на атомы водорода (элиминирование заместителя). Иначе говоря, реакции этого рода можно рассматривать как реакции восстановления. Замена указанных атомов или групп на водород в различных органических веществах происходит с различной степенью трудности. Например, в таких металлоорганических соединениях, как цинкорганические или магнийорганические, атомы металла легко заменяются на атомы водорода уже при действии воды:
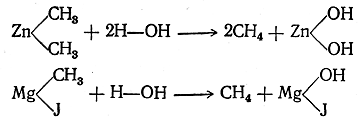
Для других органических соединений требуется действие сильных восстановителей.
Как показал Вертело (1868), особенно энергично восстанавливает органические вещества иодистоводородная кислота (при нагревании) вследствие ее способности диссоциировать на водород и иод:
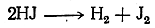
При этом водород в момент выделения (in statu nascendi) действует чрезвычайно энергично как восстановитель. Таким образом, можно различные вещества, даже столь трудно восстанавливающиеся, как органические кислоты, восстановить до углеводородов, согласно следующим примерным уравнениям:
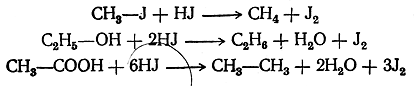
Газообразный водород является при обыкновенной температуре веществом инертным. Чтобы водород вступал в реакции восстановления, нужно действовать им в момент его выделения из соединений, пользуясь, например, цинком или амальгамой натрия и соляной кислотой или литийалюминийгидридом LiAlH. В этом случае реакции сводятся к прямому замещению различных атомов и остатков на водород, например:
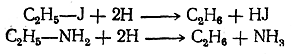
2. Получение из непредельных углеводородов. К реакциям восстановления относят и реакции получения предельных углеводородов из непредельных, т. е. содержащих двойные и тройные связи. Здесь речь идет о непосредственном присоединении атомов водорода (реакции гидрирования), например:

Эти реакции также протекают при действии таких восстановителей, как иодистоводородная кислота, но могут идти и с газообразным водородом. Однако в последнем случае, вследствие инертности водорода при обыкновенной температуре, приходится прибегать к помощи катализаторов.
Наиболее сильными катализаторами для реакции восстановления водородом являются металлы группы платины в мелко раздробленном состоянии, особенно сама платина, палладий и осмий. В присутствии этих металлов водород легко вступает в реакции даже при обычной температуре (С. А. Фокин; Вильштеттер).
Чрезвычайно важное значение имело открытие, сделанное французскими учеными Сабатье и Сандераном. Ими было найдено (1905), что очень активным катализатором для реакций присоединения водорода является мелко раздробленный никель при температуре выше 100 °С. Кроме металлического никеля, для этой цели теперь применяют также окись никеля, мелко раздробленную медь и ряд других катализаторов. Очень активным катализатором реакций восстановления водородом являет-
ся так называемый скелетный никелевый катализатор («никель Ренея»); он получается из сплава никеля с алюминием — в остатке после выщелачивания большей части алюминия рас-твором едкого натра.
3. Получение из кетонов. Большое значение имеет реакция Н. М. Кижнера, позволяющая получать углеводороды из соответствующих альдегидов и кетонов.
//. Получение из соединений с меньшим числом атомов углерода в молекуле:
1. Получение из галоидных алкилов. Одной из важнейших синтетических реакций получения предельных углеводородов является действие натрия на галоидные алкилы (реакция Вюрца). Механизм этой реакции подробно изучен П. П. Шорыгиным.
При действии натрия на галоидное соединение галоид отщепляется, а два углеводородных остатка соединяются, образуя молекулу углеводорода:
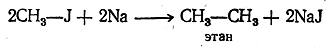
При этом можно взять два различных галоидных алкила:
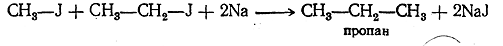
Аналогично галоидные алкилы реагируют и с некоторыми другими металлами.
Реакцию можно разделить на две фазы: а) образование металлоорганических соединений и б) действие на них галоидных соединений, приводящее к синтетическому образованию углеводородов, например:
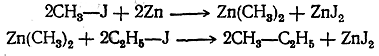
Реакция Вюрца имеет большое значение не только для синтеза углеводородов, но и для доказательства их строения, Подбирая галоидные соединения с соответствующими радикалами, можно получить углеводород любого строения, например.
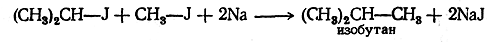
Обозначая одновалентные углеводородные остатки, или радикалы, буквой R, можно изобразить уравнение реакции Вюр-да в самой общей форме:
R — J + R'— J + 2Na-----> R — R' + 2NaJ
2. Электролиз солей одноосновных органических кислот (реакция Кольбе). В растворах соли одноосновных органических кислот распадаются на ионы:
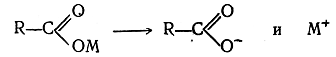
При электролизе ион металла, теряя на электроде заряд, действует на воду с выделением водорода и образованием едкой щелочи, а ион кислотного остатка, потеряв свой заряд, распадается на радикал R· и двуокись углерода СО2. Два радикала R· соединяются в молекулу R—R.
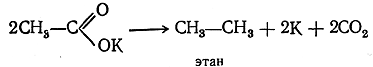
Согласно сказанному, при пропускании электрического тока через раствор уксуснокислого калия происходит реакция:
///. Получение из соединений с большим числом атомов углерода в молекуле (реакции расщепления):
Из реакций получения индивидуальных предельных углеводородов, происходящих с расщеплением углеродной цепи, важнейшей является сплавление солей одноосновных предельных кислот с едкими щелочами. Реакция идет по уравнению