Медь
МЕДЬ (лат. Cuprum-от назв. о. Кипр, где в древности добывали медную руду) Сu, хим. элемент I гр. периодич. системы, ат. н. 29, ат. м. 63,546. Прир. медь состоит из смеси двух стабильных изотопов 63Сu (69,09%) и 65Сu (30,91%). Поперечное сечение захвата тепловых нейтронов для прир. смеси 3,77.10-28 м2. Конфигурация внеш. электронной оболочки атома 3d104s1; степени окисления + 1, +2, редко +3, + 4; энергии ионизации Сu0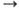 Сu+
Сu+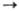 Сu2 +
Сu2 +  Сu3+ соотв. равны 7,7264, 20,2921, 36,83 эВ; сродство к электрону 1,8 эВ; электроотрицательность по Полингу 1,9; атомный радиус 0,128 нм, ионные радиусы (в скобках указаны координац. числа) Сu+ 0,060 нм (2), 0,074 нм (4), 0,091 нм (6), Сu2+ 0,071 нм (2), 0,079 нм (5), 0,087 нм (6); работа выхода электрона 4,36 эВ.
Сu3+ соотв. равны 7,7264, 20,2921, 36,83 эВ; сродство к электрону 1,8 эВ; электроотрицательность по Полингу 1,9; атомный радиус 0,128 нм, ионные радиусы (в скобках указаны координац. числа) Сu+ 0,060 нм (2), 0,074 нм (4), 0,091 нм (6), Сu2+ 0,071 нм (2), 0,079 нм (5), 0,087 нм (6); работа выхода электрона 4,36 эВ.
Содержание меди в земной коре (4,7.5,5).10-3% по массе. Для меди характерны месторождения гидротермального происхождения. В морской воде содержание меди 3.10-7% по массе, в речной —1.10-7%; ионы меди, поступающие в бассейны морей и океанов, сорбируются донными отложениями, поэтому содержание меди в них достигает 5,7.10-3%. Ионы меди участвуют во многих физиол. процессах, среднее содержание меди в живых организмах 2.10-4% по массе, в крови человека ок. 0,001 мг/л.
В земной коре медь встречается в осн. в виде соед. с S (св. 90% мировых запасов и добычи меди) и в виде кислородсодержащих соединений. Среди многочисл. минералов меди (более 250) наиб. важны: халькопирит CuFeS2, ковеллин CuS, халькозин Cu2S, борнит Cu5FeS4, куприт Сu2О, малахит CuCO3.Cu(OH)2, хризоколла CuSiO3.2H2O др. Редко встречается самородная медь. Медные руды по минера-логич. составу м. б. подразделены на сульфидные, оксидные и смешанные (30-40% Cu в форме оксидных минералов). По текстурным особенностям различают медные руды массивные, или сплошные (колчеданные, медно-никелевые, полиметаллич.), и прожилково-вкрапленные (медистые песчаники и сланцы). Медные руды полиметаллич., помимо меди, они содержат Fe, Zn, Pb, Ni, Au, Ag, Mo, Re, Se, Fe, платиновые металлы и др. Осн. мировые запасы меди (кроме СССР) сосредоточены в Сев. Америке (США, Канада, Мексика)-32%, Юж. Америке (Чили, Перу)-30%, Африке (Замбия, Заир)-15%. Мировые запасы медных руд (без СССР) составляют 847,6 млн. т, в т. ч. доказанные 447,4 млн. т.
Свойства. Медь-пластичный, розовато-красный металл с характерным металлич. блеском, тонкие пленки меди при просвечивании-зеленовато-голубого цвета. Кристаллич. решетка гранецентрированная кубич., а = 0,36150 нм, 2 = 4, пространств. группа FтЗт. Т. пл. 1083,4 0С, т. кип. 2567 °С; плотн. 8,92 г/см3, жидкой при 1100 0С-8,36 г/см3, при 200°С-8,32 г/см3, рентгеновская плотн. 8,9331 г/см3; C0р 24,44 ДжДмоль • К), ур-ние температурной зависимости в интервале 248-1356,9 К: С0р = 4,187(5,41 + 1,4.7.10-3 Т)ДжДмоль.К); DH0пл 13,02 кДж/моль, скрытая DHпл 205 кДж/молъ, DH0исп 304,8 кДж/моль; S0298 33,15 ДжДмоль.К); ур-ние температурной зависимости давления пара над жидкой медью: lgp(Па) = -17650/T + 1 l,27.l,273lg Т (1356,9-2870 К). Даже при 1900 К давление пара над медью не превышает 133,32 Па. Температурный коэф. линейного расширения 1,7.10-5 К-1 (273-323 К), ур-ние температурной зависимости линейного расширения: lt = l0(1 + 1,67.10-5t + + 3,8.10-9t2 + 1,5.10-12t3) м, где l0-длина образца при 25 °С; объемная усадка при кристаллизации-4,1%. Наиб. важные и широко используемые св-ва меди-ее высокая теплопроводность и малое электрич. сопротивление:

Температурный коэф. r 4,3-10~3 К-1 (273-373 К). Медь диамагнитна, уд. магн. восприимчивость -0,66.10-6. Для жидкой меди у (в мН/м): 1120 (1413 К), 1160 (1473 К), 1226 (1573 К); h (в мПа.с): 4,0 (1356,9 К), 8,6 (1373 К), 3,41 (1418 К).
Медь-мягкий, ковкий металл; твердость по Моосу 3,0; твердость по Бринеллю 370-420 МПа; sраст 220 МПа; относит. удлинение 60%, относит. уменьшение поперечного сечения 70%; модуль продольной упругости 112 ГПа; модуль сдвига 49,25 ГПа; коэф. Пуассона 0,34. После обработки давлением в связи с наклепом предел прочности меди возрастает до 400-450 МПа, уменьшаются на 1-3% удлинение и электрич. проводимость; последствия наклепа устраняются после отжига металла при 900-1000 К. Под действием нейтронного облучения (373 К, поток 5.1019 n/см2) предел текучести меди возрастает почти в 2,7 раза, сопротивление разрыву-в 1,26 раза, удлинение уменьшается в 1,35 раза. Небольшие примеси Bi, Pb вызывают красноломкость меди, S, О2 - хладноломкость, примеси Р, As, Al, Fe заметно уменьшают электрич. проводимость меди.
Медь растворяет Н2, к-рый существенно ухудшает ее мех. св-ва ("водородная болезнь"). Р-римость Н2 при 0,1 МПа (в см3 на 1 кг меди):
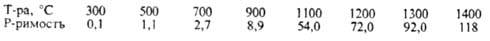
Стандартный электродный потенциал для р-ции Сu2+ + + 2е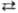 Сu равен 0,339 В, для р-ции Cu+ + e
Сu равен 0,339 В, для р-ции Cu+ + e Сu 0,515 В. Хим. активность меди невелика. В сухом воздухе при комнатной т-ре медь почти не окисляется. При нагр. тускнеет из-за образования пленки меди оксидов. Заметное взаимод. с О2 воздуха начинается ок. 200 °С по схеме: Сu
Сu 0,515 В. Хим. активность меди невелика. В сухом воздухе при комнатной т-ре медь почти не окисляется. При нагр. тускнеет из-за образования пленки меди оксидов. Заметное взаимод. с О2 воздуха начинается ок. 200 °С по схеме: Сu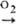 Сu2О
Сu2О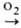 СuО. Сначала при т-ре до 377 °С образуется Сu2О, а выше 377 °С- двухслойная окалина, внутр. слой к-рой состоит из Сu2О, внешний-из СuО. Во влажном воздухе в присут. СО2 на пов-сти меди образуется зеленоватая пленка Cu(OH)2 x х СuСО3, в присут. SO2-пленка CuSO4 • 3Cu(OH)2, в среде H2S-черная пленка сульфида CuS.
СuО. Сначала при т-ре до 377 °С образуется Сu2О, а выше 377 °С- двухслойная окалина, внутр. слой к-рой состоит из Сu2О, внешний-из СuО. Во влажном воздухе в присут. СО2 на пов-сти меди образуется зеленоватая пленка Cu(OH)2 x х СuСО3, в присут. SO2-пленка CuSO4 • 3Cu(OH)2, в среде H2S-черная пленка сульфида CuS.
Медь не реагирует с Н2, N2, С, Si. При пропускании NH3 над раскаленной медью образуется Cu3N, в аналогичных условиях при контакте с парами S, Se, H2S, оксидами азота на пов-сти меди образуются соотв. сульфиды, селениды, оксиды. При сплавлении с S медь дает Cu2S, с Se и Те -соотв. селениды и теллуриды. Медь активно реагирует с галогенами, образуя соответствующие соли (см. Меди хлориды). С соляной к-той, разб. H2SO4, СН3СООН медь взаимод. только в присут. окислителей, образуя соответствующие соли Cu(II). В HNO3
Медь раств. с образованием Cu(NO3)2 и оксидов азота, в горячей конц. H2SO4-c образованием CuSO4 и SO2 ,в конц. р-рах цианидов - давая комплекс состава [Cu(CN)2]-.
Соли Cu(I) бесцв., практически не раств. в воде, легко окисляются; Cu(I) склонна к диспропорционированию: 2Cu+  Cu2+ + Сu0. Соли Cu(II), напротив, хорошо раств. в воде, в разб. р-рах полностью диссоциированы. Аквака-тионы [Сu(Н2О)4]2 + придают водному р-ру голубой цвет. При введении NaOH в р-ры солей Cu(II) сначала выпадает Сu(ОН)2 (см. Меди гидроксиды), а в очень конц. р-рах NaOH образуется Na2[Cu(OH)4]. В р-рах соед. Cu(II) при действии Na2CO3 или К2СО3 осаждаются основные карбонаты mCuCO3.Cu(OH)2 (см. Меди карбонаты), при избытке оса-дителя они раств. с образованием комплексов, напр. К2[Сu(СО3)2].ЗН2О. При обработке аммиачных р-ров солей меди ацетиленом получают карбид СuС2. Ионы меди количественно восстанавливаются до металла др. более электроотрицат. металлами.
Cu2+ + Сu0. Соли Cu(II), напротив, хорошо раств. в воде, в разб. р-рах полностью диссоциированы. Аквака-тионы [Сu(Н2О)4]2 + придают водному р-ру голубой цвет. При введении NaOH в р-ры солей Cu(II) сначала выпадает Сu(ОН)2 (см. Меди гидроксиды), а в очень конц. р-рах NaOH образуется Na2[Cu(OH)4]. В р-рах соед. Cu(II) при действии Na2CO3 или К2СО3 осаждаются основные карбонаты mCuCO3.Cu(OH)2 (см. Меди карбонаты), при избытке оса-дителя они раств. с образованием комплексов, напр. К2[Сu(СО3)2].ЗН2О. При обработке аммиачных р-ров солей меди ацетиленом получают карбид СuС2. Ионы меди количественно восстанавливаются до металла др. более электроотрицат. металлами.
Соли Cu(I) и Cu(II) с рядом молекул и ионов (NH3, CN-, Сl- и др.) образуют устойчивые комплексные соед., напр. (NH4)2[CuBr3], K3[Cu(CN)4], K2[CuCl4], аммиакаты; коор-динац. числа для Сu(I)-2, 3, 4, для Сu(II)-3, 4, 6. Путем образования комплексных соед. можно перевести в р-р многие нерастворимые соли меди. Известны соед. Cu(III)- неустойчивые, сильные окислители, примеры-KCuO2, K3[CuF6]. Наиб. важным соед. меди посвящены отдельные статьи, см., напр., Меди ацетаты, Меди нитрат, Меди сульфат, Медь-органические соединения.
Получение. Осн. сырье для получения меди-сульфидные, реже-смешанные руды. Большое значение приобретает переработка вторичного сырья, из к-рого в ряде развитых стран получают до 30-60% производимой меди. В связи с невысоким содержанием меди в рудах (0,5-1,2%) и их много-компонентностью руды подвергают флотационному обогащению, получая попутно, помимо медного, и др. концентраты, напр. цинковый, никелевый, молибденовый, пиритный, свинцовый. Содержание меди в медных концентратах достигает 18-45%.
Осн. кол-во меди (85-88%) получают по пирометаллургич. схемам, к-рые, как правило, включают след. последовательные стадии: обжиг концентрата, плавку, конвертирование, рафинирование. Обжиг проводят при переработке высокосернистых и полиметаллич. концентратов. При обжиге удаляют избыточное кол-во S в форме газов, содержащих 5-8% SO2 и используемых для произ-ва H2SO4, и переводят часть примесей (Fe, Zn, As, Pb и др.) в формы, переходящие при послед. плавке в шлак. Обжиг проводят в печах "кипящего слоя" с применением дутья, обогащенного О2 (24-26% О2), без затрат углеродистого топлива. Продукт обжига - огарок -плавят в печах отражательного типа, реже - электропечах. Богатые медью руды плавили в шахтных печах, в настоящее время этот способ имеет подчиненное значение. Перечисл. способы плавки связаны с расходом (10-18% от массы шихты) углеродистого топлива (прир. газ, мазут, кокс) или электроэнергии (350-450 кВт.ч на 1 т шихты).
В процессе плавки образуются 2 жидкие фазы-сплав сульфидов меди, Fe, цветных металлов (штейн; 22-45% Сu) и сплав оксидов металлов и силикатов (шлак; 0,4-0,7% Сu), к-рые не смешиваются друг с другом. Шлаки складируют или используют при произ-ве строит. материалов. Осваиваются автогенные процессы плавки, использующие тепло экзотермич. р-ций окисления сульфидов; концентраты обрабатывают в атмосфере О2, воздуха, обогащенного О2, или подогретого воздуха. Высокая производительность, получение богатых медью штейнов (до 75% Сu) и концентрированных по SO2 газов, миним. расход углеродистого топлива-достоинства, определяющие автогенные процессы как перспективное направление в развитии пирометаллургии меди. Важнейшие способы автогенной плавки-кислородно-факельная, взвешенная, отражательная, электроплавка, плавка в жидкой ванне, процессы "Норанда", "Мицубиси".
Расплав штейна (в осн. Cu2S • FeS) направляют на кон-вертирование - продувку сжатым воздухом с целью количеств. окисления FeS и его ошлакования в присут. кварцевого флюса (первая стадия процесса), окисления Cu2S и макс. удаления S и большинства примесей (вторая стадия):
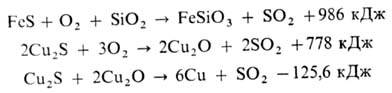
При конвертировании используют тепло экзотермических р-ций окисления, конечный продукт-черновая медь (98,5-99,3% Сu).
Черновую медь рафинируют огневым, а затем электрохим. способом. Огневое рафинирование основано на большем, чем у меди, сродстве большинства металлов-примесей к кислороду, что позволяет при продувке расплава воздухом окислить и ошлаковать количественно Fe, S, Zn, Pb и, частично, Ni, As, Sb, Bi. Для удаления кислорода расплав меди обрабатывают восстановителем (прир. конверсир. газ, сырая древесина). Готовый металл (>=99,5% Сu) разливают в формы, удобные для проведения электролиза. Полученные отливки служат анодами. Электролитич. рафинирование проводят в сернокислых р-рах при наложении постоянного тока; в процессе электролиза осуществляется непрерывная циркуляция подогреваемого (57-67°С) р-ра, медь осаждают на катодных основах, получаемых также электролизом в спец. матричных ваннах при условиях, обеспечивающих осаждение чистого металла. Для получения ровного катодного осадка требуемой текстуры в электролит вводят ПАВ. Катодную медь (>=99,94% Сu) переплавляют и разливают в формы, удобные для послед. обработки прокаткой, волочением. При растворении анодов ряд примесей (As, Fe, Ni, Sb) накапливается в электролите, поэтому часть его выводят из циркуляц. цикла (заменяя равным объемом р-ра H2SO4) и направляют на переработку для получения техн. сортов медного и никелевого купоросов. Нерастворимые включения анода образуют дисперсный продукт - шлам, в к-ром концентрируются благородные и редкие металлы. Этот продукт специально перерабатывают в шламовом цикле. Анодные остатки (выход их 15-18% от массы анода) возвращают на переплавку в цикл огневого рафинирования.
При пирометаллургич. переработке медного концентрата извлекают до 96-98% меди и благородных металлов, однако степень извлечения сопутствующих элементов (S, Zn, Ni, Pb) гораздо ниже, a Fe полностью теряется со шлаком.
Многие проблемы пирометаллургич. произ-ва меди (экологическая из-за повыш. тепло-, пыле- и газовыделения, взры-воопасность в случае контакта расплава штейна с водой и др.) устраняются при использовании гидрометаллургич. технологии. Она включает: селективное выщелачивание меди из сырья, чаще всего р-ром H2SO4 или NH3; очистку р-ра от примесей и извлечение сопутствующих ценных элементов (Zn, Co, Ni, Cd и др.); выделение меди. При переработке бедных р-ров (0,5-12,0 г/л меди) используют цементацию на железном скрапе и экстракцию с послед. электрохим. осаждением меди. Из богатых р-ров (30-40 г/л меди) медь извлекают чаще электролизом или автоклавным осаждением водородом (127-197 °С, давление Н2 1,5-2,5 МПа). В последнем случае медь получают в форме порошка (>=99,6% меди). Гидрометаллургич. схемы эффективны при извлечении меди из бедных руд методами подземного, кучного, чанового выщелачивания, в т. ч. с использованием биохим. окисления сульфидов; остатки от выщелачивания смешанных руд обогащают флотацией. Рациональна переработка полиметаллич. концентратов, вторичного сырья, особенно при небольшом объеме произ-ва. В этом случае весьма перспективно автоклавное выщелачивание при повыш. т-рах (137-197 °С) и давлении кислородсодержащего газа-окислителя (давление О2 0,2-1,0 МПа), обеспечивающее значит. интенсификацию процесса, получение более чистых р-ров и элементной S при окислении сульфидов. Гидрометаллургич. схемы позволяют более комплексно использовать сырье, проще обеспечить экологич. и пром. санитарию. Внедрение их сдерживается из-за недостаточной интенсивности, повыш. эксплуатац. затрат и др.
Определение. Соед. меди в смеси с содой и углем в пламени горелки образуют красный металлич. королек, р-римый в HNO3. Р-ры, содержащие ионы Сu2+ , при добавлении NH3 приобретают синюю окраску (чувствительность 0,007 мг/л); при добавлении K4[Fe(CN)6] выпадает красно-коричневый осадок (чувствительность 0,0001 мг/л); при взаимод. с Na2S или (NH4)2S образуется черный осадок CuS. Для количеств. определения меди используют гравиметрич., объемный, комплексонометрич., амперометрич., кондуктометрич., по-лярографич., потенциометрич., радиоактивац., эмиссионный, спектральный методы анализа. При повыш. содержании меди ее определяют объемным иодометрич. или более точным электрогравиметрич. методом. Для определения малых кол-в меди используют фотометрич. метод с дити-зоном, купфероном, диэтилдитиокарбаматом Na (чувствительность 0,02-0,002 мг/л), атомно-абсорбционный (кислородно-водородное пламя, l = 324,7 нм, чувствительность 0,01-0,0015 мг/л). При определении содержания меди в сточных водах дополнительно используют флуоресцентный (чувствительность 0,002 мг/л), спектральный (0,002-0,003 мг/л), хроматографич. (0,07 мг/л) методы анализа.
Применение. Широкое применение меди в пром-сти обусловлено рядом ее ценных св-в и прежде всего высокой электрич. проводимостью, пластичностью, теплопроводностью. Более 50% меди используется для изготовления проводов, кабелей, шин, токопроводящих частей электрич. установок. Из меди изготовляют теплообменную аппаратуру (вакуум-испарители, подогреватели, холодильники). Более 30% меди применяют в виде сплавов, важнейшие из к-рых - бронзы, латуни, мельхиор и др. (см. Меди сплавы). Медь и ее сплавы используют также для изготовления художеств. изделий. В виде фольги медь применяют в радиоэлектронике. Значит. кол-во меди(10-12%) применяют в виде разл. соед. в медицине (антисептич. и вяжущие ср-ва), для изготовления инсектофунгицидов, в качестве медных удобрений, пигментов, катализаторов, в гальванотехнике и т.д.
Мировое произ-во меди (без СССР) ок. 7,5 млн. т, в т.ч. из вторичного сырья-1,15 млн. т/год (1985). Осн. страны-производители рафинированной меди (1985): США (1,7 млн. т), Япония (1,1), Чили (0,9), Канада (0,8), Замбия (0,53), Заир (0,5).
Все соли меди ядовиты; раздражают слизистые, поражают желудочно-кишечный тракт, вызывают тошноту, рвоту, заболевание печени и др. При вдыхании пыли меди развивается хронич. отравление. ПДК для аэрозолей меди 1 мг/м3, питьевой воды 1,0 мг/л, для рыбных водоемов 0,01 мг/л, в сточных водах до биол. очистки 0,5 мг/л.
Медь известна человечеству с глубокой древности. Медь и ее сплавы сыграли заметную роль в развитии цивилизации.
Исп. литература для статьи «МЕДЬ»: Набойченко С. С., Смирнов В. И., Гидрометаллургия меди, М., 1974; Металлургия меди, никеля, кобальта, 2 изд., ч. 1, М., 1977; Онаев И. А., Жакибаев Б. К., Медь в истории цивилизации, А.-А., 1983; Ванюков А. В., Уткин Н. И., Комплексная переработка медного и никелевого сырья, М., 1988; Ванюков А. В. [и др.], Плавка в жидкой ванне, М., 1988; Подчайно-ва В.Н., Симонова Л.Н., Медь, М., 1990. С. С. Набойченко.
