Ионные радиусы
Ионные радиусы, условные характеристики ионов, используемые для приблизительной оценки межъядерных расстояний в ионных кристаллах. Значения ионных радиусов закономерно связаны с положением элементов в периодической системе Менделеева. Ионные радиусы широко используются в кристаллохимии, позволяя выявить закономерности строения кристаллов разных соединений, в геохимии при изучении явления замещения ионов в геохимических процессах и др.
Предложено несколько систем значений ионных радиусов. В основе этих систем обычно лежит следующее наблюдение: разность межъядерных расстояний А — Х и В — Х в ионных кристаллах состава АХ и ВХ, где А и В — металл, Х — неметалл, практически не меняется при замене Х на аналогичный ему другой неметалл (например, при замене хлора на бром), если координационные числа аналогичных ионов в сравниваемых солях одинаковы. Отсюда вытекает, что ионные радиусы обладают свойством аддитивности, т. е. что экспериментально определяемые межъядерные расстояния можно рассматривать как сумму соответствующих «радиусов» ионов. Разделение этой суммы на слагаемые всегда базируется на более или менее произвольных допущениях. Системы ионных радиусов, предложенные разными авторами, отличаются главным образом использованием различных исходных допущений.
В таблицах приводят ионные радиусы, отвечающие разным значениям окислительного числа (см. Валентность). При значениях его, отличных от +1, окислительное число не соответствует реальной степени ионизации атомов, и ионные радиусы приобретают ещё более условный смысл, так как связь может иметь в значительной мере ковалентный характер. Значения ионных радиусов (в 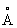 ) для некоторых элементов (по Н. В. Белову и Г. Б. Бокию): F— 1,33, Cl— 1,81, Br— 1,96, I— 2,20, O2— 1,36, Li+ 0,68, Na— 0,98, К+ 1,33, Rb+ 1,49, Cs+ 1,65, Be2+ 0,34, Mg2+ 0,74, Ca2+ 1,04, Sr2+ 1,20, Ba2+ 1,38, Sc3+ 0,83, Y3+ 0,97, La3+ 1,04.
) для некоторых элементов (по Н. В. Белову и Г. Б. Бокию): F— 1,33, Cl— 1,81, Br— 1,96, I— 2,20, O2— 1,36, Li+ 0,68, Na— 0,98, К+ 1,33, Rb+ 1,49, Cs+ 1,65, Be2+ 0,34, Mg2+ 0,74, Ca2+ 1,04, Sr2+ 1,20, Ba2+ 1,38, Sc3+ 0,83, Y3+ 0,97, La3+ 1,04.
В. Л. Киреев.
