Жёсткость воды
Жёсткость воды, совокупность свойств, обусловленных содержанием в воде ионов Са2+ и Mg2+. Суммарная концентрация ионов Ca2+ (кальциевая жёсткость воды) и Mg2+ (магниевая жёсткость воды) называется общей жёсткостью воды. Различают жёсткость воды карбонатную и некарбонатную. Карбонатная жёсткость воды соответствует той части ионов Ca2+ и Mg2+, которая эквивалентна содержащимся в воде гидрокарбонат-ионам
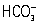
В СССР величину жёсткости природных вод выражают в миллиграмм-эквивалентах на 1 л (мг-экв/л), а жёсткость вод умягченных, обессоленных и т. п. — в микрограмм-эквивалентах на 1 кг (мкг-экв/кг). До 1952 в СССР жёсткость воды выражали в градусах жёсткости (1° соответствует 0,357 мкг-экв/л). Жёсткость природных вод колеблется в очень широких пределах — от 0,1—0,2 мг-экв/л в водах рек и озёр, расположенных в зонах тайги и тундры, до 80—100 мг-экв/л в некоторых подземных водах и водах морей и океанов. Повышенная жёсткость воды природных источников обусловлена преимущественно контактом воды с горными породами, содержащими карбонаты и сульфаты Ca и Mg. Использование жёсткой воды недопустимо в теплоэнергетике, производстве искусственного волокна и ряде др. отраслей. Жёсткость воды ведёт к усиленному образованию накипи в котлах и отопительных приборах, что ухудшает теплообмен. Жёсткость воды увеличивает расход мыла при стирке, т. к. часть его образует с ионами Ca2+ нерастворимый осадок. В жёсткой воде плохо развариваются овощи и мясо, т. к. ионы Ca2+ образуют с белками пищевых продуктов нерастворимые соединения; ухудшается вкус чая. Высокая жёсткость воды способствует образованию мочевых камней у человека. Допустимый предел жёсткости воды, используемой для централизованного водоснабжения, — 7 мг-экв/л; в исключительных случаях по согласованию с органами санитарного надзора может быть допущена большая жёсткость воды — до 14 мг-экв/л. При необходимости использования водоисточника с высокой жёсткостью воды применяют специальные методы умягчения воды (см. также Водоподготовка).
Лит.: Гигиеническое нормирование солевого состава питьевой воды, под ред. С. Н. Черкинского, М., 1963.
В. А. Клячко.
