Жесткость воды
ЖЕСТКОСТЬ ВОДЫ, совокупность св-в воды, обусловленная наличием в ней преим. катионов Са2+ (кальциевая жесткость воды) и Mg2+ (магниевая жесткость воды). Один из возможных их источников - горные породы (известняки, доломиты), к-рые растворяются в результате контакта с прир. водой. Сумма концентраций Са2+ и Mg2+ наз. общей жесткостью воды. Она складывается из карбонатной (временной, устраняется кипячением) и некарбонатной (постоянной) жесткости воды. Первая вызвана присутствием в воде гидрокарбонатов Са и Mg [при кипячении разлагаются на СаСО3 и Mg(OH)2 с выделением СО2], вторая - наличием сульфатов, хлоридов, силикатов, нитратов и фосфатов этих металлов. В СССР жесткость воды выражают в ммоль экв/л: карбонатная жесткость отвечает той части катионов Са2+ и Mg2+, которая эквивалентна содержащимся в воде анионам НСО3-, некарбонатная - анионам SO42-, NO3- и др. (1 ммоль экв/л соответствует 20,04 мг/л катионов Са2+ или 12,16 мг/л катионов Mg2+). В др. странах для выражения Ж в. часто используют т. наз. градусы жесткости. Напр., Г жесткости немецкий, соответствующий 0,01 г СаО в 1 л воды, равен 0,357 ммоль экв/л. Жесткость воды обычно определяют титрованием р-ром дигидрата динатриевой соли этилендиаминтетрауксусной к-ты (комплексон III, трилон Б) в щелочной среде. При титровании с использованием комплексонометрич. индикаторов находят: в присут. эриохрома черного Т (хромогеновый черный ЕТ) -общую жесткость воды (Жоб), в присут. мурексида (пурпурат аммония) - кальциевую жесткость воды (ЖСа ). Магниевую жесткость воды определяют из выражения: ЖMg = Жоб - ЖCa. Если содержание катионов Са2+ и Mg2+ в воде было найдено др. методами, общую жесткость воды можно вычислить по ф-ле: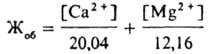
Жесткость воды колеблется в широких пределах: от 0,1-0,2 ммоль экв/л в реках и озерах, расположенных в зонах тайги и тундры, до 80-100 ммоль экв/л и более в подземных водах, морях и океанах. Различают воду мягкую (общая жесткость до 2 ммоль экв/л), средней жесткости (2-10 ммоль экв/л) и жесткую (более 10 ммоль экв/л). В поверхностных водоисточниках, где преобладает, как правило, карбонатная жесткость (70-80% от общей), а магниевая жесткость обычно не превышает 30%, реже 60% от общей, наиб. значения жесткость воды достигает в конце зимы, наименьшего - в период паводка. Так, в Волге (г. Горький) макс. жесткость воды бывает в марте (4,3 ммоль экв/л), минимальная - в мае (0,5 ммоль экв/л).
Литература
Руководство по химическому анализу поверхностных вод суши, под ред. А. Д. Семенова. Л., 1977; Унифицированные методы исследования качества вод. ч. 1. Методы химического анализа вод. кн. 1, 2, 3 изд.. М., 1977; Лурье Ю. Ю., Аналитическая химия промышленных сточных вод. М., 1984.
Синонимы/примеры:*
Карбонатная жесткость; Некарбонатная жесткость; Общая жесткость; Временная жесткость; Постоянная жесткость
*подобраны ИИ, возможны неточности
Ещё по теме
Жёсткость воды — понятие и влияние на жизнь человека
Тяжёлая вода — свойства и применение
Вода
Тяжёлая вода — свойства и применение
Вода как растворитель — уникальные свойства и роль в природе
Экологическая химия гидросферы
Гидролиз — понятие, механизмы и значение в химии и биологии
Тяжёлая вода — свойства и характеристики
Поверхностные явления и адсорбция — основные понятия и термины
Водоочистка — методы и технологии
Гигроскопичность материалов — свойства и применение
Гидрофобные взаимодействия и растворимость в воде
