Гидролиз
Гидролиз (от гидро... и греч. lýsis — разложение, распад), реакция ионного обмена между различными веществами и водой. В общем виде гидролиз можно представить уравнением:
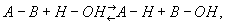
где А—В — гидролизующееся вещество, А—Н и В—ОН — продукты гидролиза.
Равновесие в процессе гидролиза солей подчиняется действующих масс закону. Если в результате гидролиза образуется нерастворимое или легколетучее вещество, гидролиз идёт практически до полного разложения исходной соли. В остальных случаях гидролиз солей проходит тем полнее, чем слабее соответствующая соли кислота или основание.
Если гидролизу подвергается соль, образованная слабой кислотой и сильным основанием, например KCN, раствор имеет щелочную реакцию; это объясняется тем, что анион слабой кислоты частично связывает образовавшиеся при диссоциации воды ионы Н+ и в растворе остаётся избыток ионов OH-:
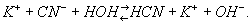
Раствор соли сильной кислоты и слабого основания, например NH4Cl, — кислый
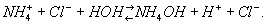
Если заряд катиона (или аниона) соли больше единицы, то гидролиз часто приводит к образованию кислых (или основных) солей в качестве продуктов первой ступени процесса, например:
CuCl2 ® Cu (OH) Cl ® Cu (OH)2.
Количественной характеристикой гидролиза солей может служить степень гидролиза (a), определяемая отношением концентрации гидролизованной части молекул к общей концентрации данной соли в растворе; в большинстве случаев она невелика. Так, в 0,1 молярных растворах ацетата натрия CH3COONa или хлорида аммония NH4CI при 25 °С a = 0,01%, а для ацетата аммония CH3COONH4 a = 0,5%. С повышением температуры и разбавлением раствора степень гидролиза увеличивается.
Гидролиз солей лежит в основе многих важных процессов в химической промышленности и лабораторной практике. Частичный гидролиз трёхкальциевого силиката является причиной выделения свободной извести при взаимодействии портландцемента с водой (см. Цемент). Благодаря гидролизу возможно существование буферных систем, способных поддерживать постоянную кислотность среды. Такие растворы имеют и очень важное физиологическое значение — постоянная концентрация ионов Н+ необходима для нормальной жизнедеятельности организма. С гидролизом солей связан ряд геологических изменений земной коры и образование минералов, формирование природных вод и почв.
Гидролиз органических соединений — расщепление органического соединения водой с образованием двух или более веществ. Обычно гидролиз осуществляется в присутствии кислот (кислотный гидролиз) или щелочей (щелочной гидролиз). Гидролитическому расщеплению чаще всего подвергаются связи атома углерода с другими атомами (галогенами, кислородом, азотом и др.). Так, щелочной гидролиз галогенидов служит методом получения (в том числе и промышленного) спиртов и фенолов, например:
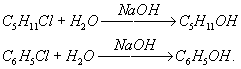
В зависимости от строения углеводородного радикала (R) и от условий реакции гидролиза галогенпроизводных может осуществляться как мономолекулярный (SN1) или бимолекулярный (SN2) процесс. В случае мономолекулярной реакции вначале происходит ионизация связи углерод — галоген, а затем образующийся ион карбония реагирует с водой; щёлочь, если она добавлена, не влияет на скорость гидролиза и служит только для нейтрализации выделяющейся галогеноводородной кислоты и смещения равновесия:
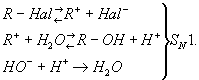
В случае бимолекулярной реакции скорость гидролиза прямо пропорциональна концентрации щёлочи:
R—Hal+ + HO- ® R—OH + Hal-SN2.
Исключительно важен гидролиз сложных эфиров (реакция, обратная этерификации):
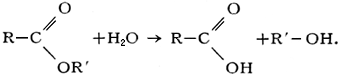
Кислотный гидролиз сложных эфиров является обратимым процессом:
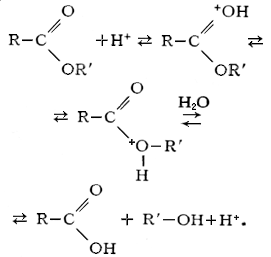
Щелочной гидролиз сложных эфиров необратим, поскольку он приводит к образованию спирта и соли кислоты:
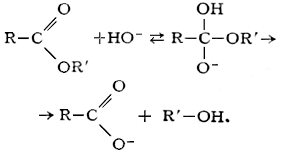
Этот процесс широко применяется в промышленности для получения спиртов и кислот, например при омылении жиров с целью получения глицерина и солей высших алифатических кислот (мыла).
Аналогично сложным эфирам гидролизуются амиды кислот:
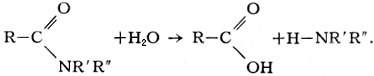
Случаи гидролиза углерод-углеродной связи сравнительно редки. К ним относятся, в частности, кетонное (действием кислот и разбавленных щелочей) и кислотное (действием концентрированной щёлочи) расщепление 1,3-дикарбонильных соединений, например ацетоуксусного эфира:
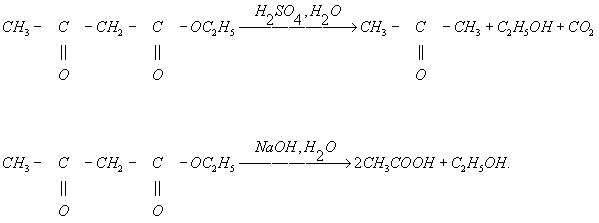
Термин «гидролиз» обычно применяется в органической химии также по отношению к некоторым процессам, которые более правильно было бы называть гидратацией; примером может служить превращение нитрилов кислот в амиды:
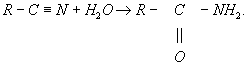
Гидролиз сложноэфирных, гликозидных (в углеводах) и амидных (в белках) связей играет огромную роль в жизнедеятельности любых организмов, например, в таких процессах, как усвоение пищи, передача нервных импульсов и т. п. Гидролиз в живом организме катализируется ферментами гидролазами. См. также Гидролиз растительных материалов.
Лит.: Киреев В. А., Курс физической химии, 2 изд., М., 1956; Реутов О. А., Теоретические проблемы органической химии, 2 изд., М., 1964.
