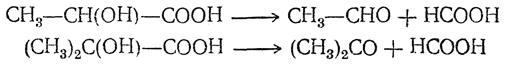Свойства
Простейшие оксикислоты — вязкие жидкости или кристаллические вещества; низшие оксикислоты смешиваются в любых соотношениях с водой. Оксикислоты являются более сильными кислотами, чем жирные предельные кислоты:

В оксикислотах гидроксильная и карбоксильная группы могут реагировать независимо друг от друга. Например, гликолевая кислота СН2(ОН)—СООН образует следующие простые и сложные эфиры:
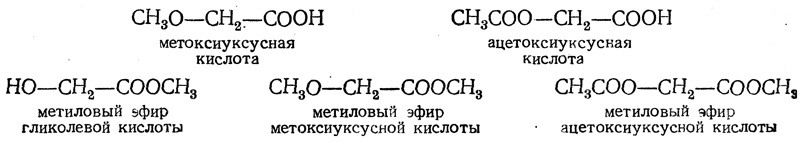
При действии на оксикислоты галоидных соединений фосфора может заместиться на галоид либо только кислотный гидроксил, причем получается галоидангидрид кислоты СН2ОН—СОСl, либо оба гидроксила с образованием галоидангидрида галоидкислоты СН2Сl—СОСl. При действии галоидоводородных кислот обменивается на галоид лишь спиртовый гидроксил, например:
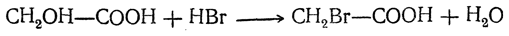
Концентрированная иодистоводородная кислота при нагревании восстанавливает гидроксил оксикислоты с образованием жирной кислоты, например:

Кроме реакций, свойственных гидроксилу и карбоксилу, для оксикислот характерны реакции, в которых сказывается взаимное влияние гидроксила и карбоксила, зависящее от расстояния между ними в молекуле. К таким реакциям, позволяющим различить α-, β-, γ- и δ-оксикислоты, относятся реакции, протекающие с выделением воды.
а) α-Оксикислоты при нагревании легко выделяют воду, причем в реакцию вступают две молекулы оксикислоты, образуя циклический сложный эфир (шестичленное кольцо). Получаемые соединения называются лактидами (для гликолевой кислоты — гликолид):
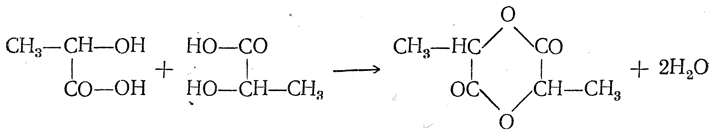
При кипячении с водой лактид омыляется с образованием двух молекул исходной кислоты.
б) β-Оксикислоты очень легко выделяют воду; при этом образуется этиленовая связь, например:
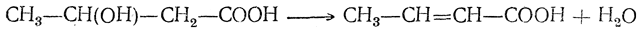
в) γ- и и δ-оксикислоты отщепляют воду с образованием соединений, называемых лактонами:
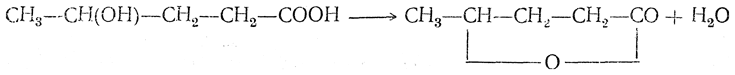
Эти соединения представляют собой циклические сложные эфиры, образуемые функциональными группами одной и той же молекулы («внутренний» сложный эфир). Так как реакция протекает с выделением воды, лактоны иногда называют «внутренними» ангидридами.
Характерной реакцией α-оксикислот является также расщепление их при кипячении с разбавленными минеральными кислотами на альдегиды (или кетоны) и муравьиную кислоту: