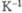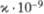Фосфор
ФОСФОР (от греч. phosphoros - светоносный; лат. Phosphorus) P, хим. элемент V гр. периодич. системы; ат. номер 15, ат. м. 30,97376. Имеет один устойчивый нуклид 31P. Эффективное сечение захвата тепловых нейтронов 18 · 10-30 м2. Конфигурация внеш. электронной оболочки атома 3s23p3; степени окисления -3, +3 и +5; энергия последоват. ионизации при переходе от Р° до P5+ (эВ): 10,486, 19,76, 30,163, 51,36, 65,02; сродство к электрону 0,6 эВ; электроотрицательность по По-лингу 2,10; атомный радиус 0,134 нм, ионные радиусы (в скобках указаны координац. числа) 0,186 нм для P3- , 0,044 нм (6) для P3+, 0,017 нм (4), 0,029 нм (5), 0,038 нм (6) для P5+.
Среднее содержание фосфора в земной коре 0,105% по массе, в воде морей и океанов 0,07 мг/л. Известно ок. 200 фосфорных минералов, все они представляют собой фосфаты. Из них важнейший - апатит, к-рый является основой фосфоритов. Практич. значение имеют также монацит CePO4, ксенотим YPO4, амблигонит LiAlPO4(F, ОН), трифилин Li(Fe, Mn)PO4, торбернит Cu(UO2)2(PO4)2· 12H2O, отунит Ca(UO2)2(PO4)2 x x 10H2O, вивианит Fe3(PO4)2· 8H2O, пироморфит Рb5(РО4)3С1, бирюза СuА16(РО4)4(ОН)8· 5Н2О.
Свойства. Известно св. 10 модификаций фосфора, из них важнейшие - белый, красный и черный фосфор (техн. белый фосфор наз. желтым фосфором). Единой системы обозначений модификаций фосфора нет. Некоторые св-ва важнейших модификаций сопоставлены в табл. Термодинамически устойчив при нормальных условиях кристаллич. черный фосфор (P I). Белый и красный фосфоры мета-стабильны, но вследствие малой скорости превращения могут практически неограниченное время сохраняться при нормальных условиях.
СВОЙСТВА ВАЖНЕЙШИХ МОДИФИКАЦИЙ ФОСФОРА
| Показатель | Белый Р Ш | Красный P II | Черный P I | ||
| Сингония | Кубич. | Моноклинная | Ромбич. | ||
| Параметры элементарной ячейки: | | | | ||
| а, нм | 1,851 | 1,02 | 0,33136 | ||
| b, нм | — | 0,936 | 0,4376 | ||
| с, нм | — | 2,51 | 1,0478 | ||
| | — | 118,8 | — | ||
| z | 224 | 84 | 8 | ||
| Пространств. группа | I43т | Р2/с | Стса | ||
| Плотн., г/см3 | 1,828 | 2,31 | 2,702 | ||
| T. пл., 0C | 44,14 | 593а | 1000а | ||
| T. возг., 0C | 287б | 429 | 453 | ||
| | 23,8 | 21,2 | 21,6 | ||
| | 0,66 | 25,96 | — | ||
| | 13,1в | 128,6 | 53,75 | ||
| | 0 | -17,4 | -39,35 | ||
| | 41,1 | 22,85 | 22,7 | ||
| Теплопроводность, Вт/(м · К) | 0,56 | — | — | ||
| Температурный коэф. линейного расширения, К-1 | 3,76·10-6 | — | — | ||
| | 15, 4 · 10-8 | 107-1012 | 0,015 | ||
| Температурный коэф. р, | 45, 6 · 10-3 | — | 7,7 -10-3 | ||
| Ширина запрещенной зоны, эВ | 2,1 | 1,55 | 0,33 | ||
| Магн. восприимчивость, | -0,86 | -0,67 | -0,27 | ||
а Под давлением. б Т-ра кипения. 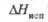
Белый фосфор (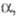 P III) образуется при конденсации паров и затвердевании расплава. Это белая прозрачная воскообразная масса (при охлаждении становится хрупкой) или прозрачные кристаллы, из-за высокой дисперсии света и большого показателя преломления похожие на алмазы. При -76,9 0C он превращается в
P III) образуется при конденсации паров и затвердевании расплава. Это белая прозрачная воскообразная масса (при охлаждении становится хрупкой) или прозрачные кристаллы, из-за высокой дисперсии света и большого показателя преломления похожие на алмазы. При -76,9 0C он превращается в 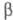 -модификацию белого фосфора (P IV) с плотн. 1,88 г/см3 с гексагон. [по др. данным, с ромбич. или кубич. (а = 0,734 нм)] кристаллич. решеткой;
-модификацию белого фосфора (P IV) с плотн. 1,88 г/см3 с гексагон. [по др. данным, с ромбич. или кубич. (а = 0,734 нм)] кристаллич. решеткой;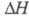 перехода
перехода 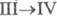 0,522 кДж/моль. В структуре белого фосфора содержатся тетраэд-рич. молекулы P4. В
0,522 кДж/моль. В структуре белого фосфора содержатся тетраэд-рич. молекулы P4. В 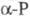 они могут свободно вращаться, в
они могут свободно вращаться, в 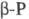 этого нет. Такие же молекулы наблюдаются в расплаве и парах фосфора. Только выше ~ 800 0C начинается диссоциация на молекулы P2. При конденсации таких паров при -190 0C образуется неустойчивая модификация - коричневый фосфор, состоящий, по-видимому, из молекул P2. Выше -100 0C он превращается в смесь белого и красного (P II) фосфора.
этого нет. Такие же молекулы наблюдаются в расплаве и парах фосфора. Только выше ~ 800 0C начинается диссоциация на молекулы P2. При конденсации таких паров при -190 0C образуется неустойчивая модификация - коричневый фосфор, состоящий, по-видимому, из молекул P2. Выше -100 0C он превращается в смесь белого и красного (P II) фосфора.
Зависимость давления пара белого фосфора от т-ры: для твердого lg p (мм рт. ст.) = 19,0925 - 35291,4/Т- 3,5 lg T (273-317 К); для жидкого lg p (мм рт. ст.) = 4,512-2660/Т+1,243 lg T (317,3-530 К). Расплав белого фосфора очень легко переохлаждается. Плотн. расплава 1,749 г/см3.
Нагревание (без доступа воздуха) выше ~ 180 0C разрушает систему связей групп P4, в результате чего начинается полимеризация, приводящая к превращению в красный фосфор. Описан целый ряд разновидностей красного фосфора, различающихся по цвету - от оранжевого и ярко-красного до коричневого и черно-фиолетового, по плотности (2,0-2,4 г/см3), т-ре плавления (585-610 0C) и т.п. При 250-300 0C образуется аморфный красный фосфор 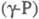 с плотн. 2,16 г/см3; при 360-450 0C -моноклинный красный фосфор (P П,
с плотн. 2,16 г/см3; при 360-450 0C -моноклинный красный фосфор (P П, 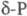 ); при ~ 500 0C - другая моноклинная модификация, также образующаяся при нагр, белого фосфора с Pb или Bi (т. наз. фосфор Гитторфа, фиолетовый фосфор) с параметрами решетки а = 0,924 нм, в = 0,921 нм, с = 2,23 нм,
); при ~ 500 0C - другая моноклинная модификация, также образующаяся при нагр, белого фосфора с Pb или Bi (т. наз. фосфор Гитторфа, фиолетовый фосфор) с параметрами решетки а = 0,924 нм, в = 0,921 нм, с = 2,23 нм, 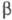 =107,4°. При длит. нагревании при ~ 600 0C образуется кубич. красный фосфор (пространств, группа РтЗт, а= 1,131 нм, z = 66, плотн. 2,35 г/см3). Описаны также трик-линный, тетрагон., гексагон. красный фосфор и др. Превращение фосфор белый
=107,4°. При длит. нагревании при ~ 600 0C образуется кубич. красный фосфор (пространств, группа РтЗт, а= 1,131 нм, z = 66, плотн. 2,35 г/см3). Описаны также трик-линный, тетрагон., гексагон. красный фосфор и др. Превращение фосфор белый  фосфор красный ускоряется при действии УФ облучения, а также в присут. примесей I2, S, Se и т.д. В структуре красного фосфора существуют связанные между собой бесконечные цепи из тетраэдров P4. В этой структуре м. б. выделены группировки P8 и P9. При испарении и плавлении красного фосфора (при атм. давлении он сублимируется и м. б. расплавлен при давлении 4,5 МПа) образуются молекулы P4. Ур-ние зависимости давления пара твердого красного фосфора от т-ры: lgp (мм рт. ст.) = 14,207 - 6300/Т+ 3,298Т+ 0,156 lg Т (298- 866 К).
фосфор красный ускоряется при действии УФ облучения, а также в присут. примесей I2, S, Se и т.д. В структуре красного фосфора существуют связанные между собой бесконечные цепи из тетраэдров P4. В этой структуре м. б. выделены группировки P8 и P9. При испарении и плавлении красного фосфора (при атм. давлении он сублимируется и м. б. расплавлен при давлении 4,5 МПа) образуются молекулы P4. Ур-ние зависимости давления пара твердого красного фосфора от т-ры: lgp (мм рт. ст.) = 14,207 - 6300/Т+ 3,298Т+ 0,156 lg Т (298- 866 К).
При давлении более 1,2 ГПa белый фосфор переходит в кристаллич. черный фосфор (P I, 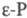 ). Для перехода красного фосфора требуется более высокое давление (2,5 ГПа), нагревание до ~ 200 0C облегчает переход. При меньших давлениях образуется аморфный черный фосфор (i-P) с плотн. 2,25 г/см3. Кристаллич. черный фосфор может быть получен и при атм. давлении -длит. нагреванием красного фосфора с ртутью при ~ 300 0C в присут. затравки. Черный фосфор графитоподобный, его структура состоит из слабо связанных между собой гофрированных слоев. При атм. давлении черный фосфор возгоняется без плавления, ур-ние зависимости давления пара от т-ры lg r (мм рт. ст.) = 13,36-7560/Т. Плавится он при ~ 1000 0C под давлением 1,8 ГПа, экстраполяция на атм. давление дает т. пл. 606 0C. При натр, черный фосфор при давлении собств. паров при 560-580 С превращается в красный.
). Для перехода красного фосфора требуется более высокое давление (2,5 ГПа), нагревание до ~ 200 0C облегчает переход. При меньших давлениях образуется аморфный черный фосфор (i-P) с плотн. 2,25 г/см3. Кристаллич. черный фосфор может быть получен и при атм. давлении -длит. нагреванием красного фосфора с ртутью при ~ 300 0C в присут. затравки. Черный фосфор графитоподобный, его структура состоит из слабо связанных между собой гофрированных слоев. При атм. давлении черный фосфор возгоняется без плавления, ур-ние зависимости давления пара от т-ры lg r (мм рт. ст.) = 13,36-7560/Т. Плавится он при ~ 1000 0C под давлением 1,8 ГПа, экстраполяция на атм. давление дает т. пл. 606 0C. При натр, черный фосфор при давлении собств. паров при 560-580 С превращается в красный.
При давлении 8,6 ГПа образуется фосфор V с ромбоэдрич. структурой типа 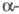 As с плотн. 3,56 г/см3 (пространств, группа R3m, z = 2, а = 0,3524 нм,
As с плотн. 3,56 г/см3 (пространств, группа R3m, z = 2, а = 0,3524 нм, 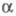 =57,25°). При 10 ГПа он переходит в модификацию VI с кубич. структурой типа NaCl (а = 0,2377 нм, z = 1) с плотн. 3,83 г/см3. Есть указания на существование при высоких давлениях и др. модификаций фосфора.
=57,25°). При 10 ГПа он переходит в модификацию VI с кубич. структурой типа NaCl (а = 0,2377 нм, z = 1) с плотн. 3,83 г/см3. Есть указания на существование при высоких давлениях и др. модификаций фосфора.
Белый и красный фосфор- диэлектрики, черный фосфор- полупроводник, модификации высокого давления, по-видимому, обладают металлич. св-вами. Сверхпроводимость наблюдается у модификаций P V и P VI ниже соотв. 4,7-6 К и 7,5-10 К (в зависимости от давления).
Белый фосфор очень активен. При переходе к красному и особенно черному фосфору хим. активность резко снижается. Белый фосфор на воздухе светится в темноте, с чем исторически связано его назв. (греч. phosphoros - светоносный). Свечение обусловлено окислением (с образованием низших оксидов) паров фосфора - белый фосфор обладает заметной летучестью даже при низких т-рах. Мелкодисперсный белый фосфор самовоспламеняется на воздухе, для компактного т. воспл. 34-50 0C. В воде он почти не раств. (3 · 10-4% при 15 0C), очень хорошо раств. в CS2 (89,8% при 10 0C), раств. в PCl3, POCl3, жидких SO2, NH3, мало раств. в этаноле (0,31%), диэтиловом эфире (1,04%), бензоле (3,2%), CCl4 (1,27%), глицерине (0,17%), уксусной к-те (~ 1%), ксилоле. Для красного и черного фосфора р-рители не найдены.
Красный фосфор при комнатной т-ре окисляется медленно, но нек-рые его образцы могут самовоспламеняться из-за присут. следов белого фосфора, а также наличия высокоактивного аморфного фосфора по границам зерен. T. воспл. красного фосфора 210 С (черного фосфора ок. 500 0C), но большие кол-ва красного фосфора при длит. хранении на воздухе могут загораться из-за повышения т-ры вследствие окисления.
При горении фосфора образуется оксид P4O10 (или P2O5, см. Фосфора оксиды). С парами воды фосфор реагирует под давлением при 600-900 0C в присут. катализаторов (Pt, Cu и др.) с вытеснением H2 и образованием H3PO4 (см. Фосфорная кислота). Р-ры неокисляющих минеральных к-т на фосфор не действуют, HNO3 окисляет его до H3PO4. При нагр. фосфора с р-рами щелочей выделяется фосфин PH3. Белый фосфор реагирует с р-рами солей электроположит. металлов (Cu, Pb, Ag и др.), вытесняя их из р-ров с образованием фосфидов. Красный и черный фосфоры этой способностью не обладают.
С водородом фосфор в обычных условиях не реагирует. Его гидриды (фосфины) получают косвенным путем. С фтором и белый и красный фосфоры реагируют со взрывом. Белый фосфор воспламеняется в атмосфере хлора и паров брома, красный реагирует спокойно. Р-ция с иодом у белого фосфора идет даже при охлаждении, тогда как у красного - при нагревании. Во всех случаях образуются разл. фосфора галогениды. При нагр. фосфора в атмосфере галогеноводородов образуются фосфин и соли фосфония.
Пары фосфора реагируют с азотом в электрич. разряде или на накаленной вольфрамовой нити с образованием смеси аморфных нитридов P3N5 и PN. Обычно нитрид P3N5 (оранжево-коричневого цвета с плотн. 2,6 г/см3) получают взаимод. P4S10 с NH3 при нагревании. При его термич. разложении при ~ 800 0C м. б. получен полимерный низший нитрид PNx переменного состава (х = 0,7 до 1,19). Нитриды фосфора инертны, холодная вода на них не действует, они не разлагаются при нагр. в р-рах HCl, разб. HNO3, р-рах щелочей, не реагируют с хлором, на воздухе начинают окисляться выше 250 0C. Нитрид P3N5 используют как газопоглотитель в лампах накаливания и в галогенных лампах, для легирования кремния в технологии полупроводниковых материалов.
Белый фосфор при сплавлении с серой при т-рах до ~ 100 0C образует систему эвтектич. типа с ограниченными твердыми р-рами, выше ~ 230 0C компоненты реагируют с образованием серии сульфидов. Тетрафосфора трисульфид P4S3 - лимонно-желтые кристаллы ромбич. сингонии (а = 1,063 нм, .b - 0,969 нм, с = 1,372 нм, z = 8, пространств. группа РптЬ); т. пл. 172 0C, т. кип. 407 0C; плотн. 2,03 г/см3; С0р 162,6 Дж/(моль·К); 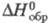 -130 кДж/моль;
-130 кДж/моль; 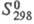 203,3 Дж/(моль·К); т. воспл. 80-89 0C; горячей водой медленно разлагается; хорошо раств. в CS2 (50% при 17 0C), раств. в бензоле (2,5%), толуоле (3%); получают взаимод. желгого или красного фосфора и серы выше 250 0C в атмосфере CO2; очищают перегонкой или перекристаллизацией из CS2; компонент зажигат. смеси для спичечных коробок. Тетрафосфора декасульфид P4S10 (или P2S5, пентасуль-фид) - серовато-желтые кристаллы триклинной сингонии (а = 0,907 нм, b = 0,918 нм, с = 0,919 нм,
203,3 Дж/(моль·К); т. воспл. 80-89 0C; горячей водой медленно разлагается; хорошо раств. в CS2 (50% при 17 0C), раств. в бензоле (2,5%), толуоле (3%); получают взаимод. желгого или красного фосфора и серы выше 250 0C в атмосфере CO2; очищают перегонкой или перекристаллизацией из CS2; компонент зажигат. смеси для спичечных коробок. Тетрафосфора декасульфид P4S10 (или P2S5, пентасуль-фид) - серовато-желтые кристаллы триклинной сингонии (а = 0,907 нм, b = 0,918 нм, с = 0,919 нм, 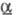 =92,4°,
=92,4°, 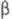 = 101,2°,
= 101,2°, 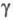 =110,5°, z = 2, пространств, группа Pl); т. пл. 288 0C, т.кип. 514 0C; плотн. 2,09 г/см3; С°р 296 Дж/(моль·К);
=110,5°, z = 2, пространств, группа Pl); т. пл. 288 0C, т.кип. 514 0C; плотн. 2,09 г/см3; С°р 296 Дж/(моль·К); 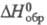 -364 кДж/моль; S0298 381,7 Дж/(моль·К); гигроскопичен, разлагается горячей водой; мало раств. в CS2; реагирует со спиртами и др. орг. р-рителями; получают аналогично P4S3; используют в синтезе флотореагентов, антикоррозионных добавок к смазочным маслам, инсектицидов и др. Известны также P4S5 и P4S7 и моносульфид PS (аморфный и кристаллический), а также селенид P4Se3 и теллурид Te3P2.
-364 кДж/моль; S0298 381,7 Дж/(моль·К); гигроскопичен, разлагается горячей водой; мало раств. в CS2; реагирует со спиртами и др. орг. р-рителями; получают аналогично P4S3; используют в синтезе флотореагентов, антикоррозионных добавок к смазочным маслам, инсектицидов и др. Известны также P4S5 и P4S7 и моносульфид PS (аморфный и кристаллический), а также селенид P4Se3 и теллурид Te3P2.
Пары фосфора реагируют с углеродом, только выше 2000 0C. Косвенным путем, напр. р-цией PCl3 с Mg2C2I2, можно получить карбид P2C6 - светло-желтая аморфная масса, не взаимод. с водой, р-рами к-т и щелочей, но загорается на воздухе при самом слабом нагревании. С CO2 фосфор реагирует выше 650 0C с образованием СО и паров низших оксидов фосфора. С СО не реагирует.
С кремнием пары фосфора взаимод. выше 1000 0C с образованием желто-коричневого силицида SiP, устойчивого до 1100 0C. Взаимод. гидридов PH3 и SiH4 получен Si2P голубовато-черного цвета. Силициды фосфора устойчивы на воздухе, гидролизу-ются горячей водой, разлагаются р-рами щелочей, а также минеральных к-т при нагревании. С бором, а также со всеми металлами, кроме Sb и Bi, фосфор реагирует при нагр. с образованием фосфидов.
Фосфор большей частью образует ковалентные связи как с одноименными атомами, так и с атомами др. элементов. Редкое исключение - частично ионные связи в нек-рых фосфидах. Обычно наблюдаются простые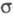 -связи. Часто образуются полимеры с такими связями (элементарный фосфор, оксиды, полифосфаты и др.). Важнейшим соед. фосфора посвящены отдельные статьи (см. Фосфора кислоты, Фосфаты неорганические, Фосфорорганические соединения и др.).
-связи. Часто образуются полимеры с такими связями (элементарный фосфор, оксиды, полифосфаты и др.). Важнейшим соед. фосфора посвящены отдельные статьи (см. Фосфора кислоты, Фосфаты неорганические, Фосфорорганические соединения и др.).
Получение. Фосфор получают восстановлением фосфоритов или апатита коксом в присут. SiO2 в электропечах при 1300-1500 0C по р-ции:
4Ca5(PO4)3F + 21SiO2 + 30C 3P4 + 20CaSiO3 + SiF4 + З0СО
3P4 + 20CaSiO3 + SiF4 + З0СО
Образующиеся пары фосфора конденсируются на охлаждаемой пов-сти в виде белого (желтого) фосфора и собираются под слоем нагретой воды (60 0C). В случае присутствия в шихте оксидов железа в качестве побочного продукта получается феррофос-фор - сплав фосфидов Fe2P и Fe3P.
Красный фосфор получают нагреванием белого без доступа воздуха в течение неск. часов при 375-400 0C.
Очищают белый фосфор отстаиванием или фильтрованием расплава, переплавкой под слоем разб. хромовой смеси, обработкой 10-20%-ным р-ром KOH при 90-100 0C, 50%-ной H2SO4 и деионизированной водой при 41-50 0C, сублимацией или перегонкой в вакууме либо перегонкой с водяным паром в атмосфере CO2, высокотемпературной обработкой паров (900-1200 0C) на кварцевой насадке, зонной плавкой. Кристаллы белого фосфора получают испарением р-рителя из его р-ров в CS2 или бензоле.
Красный фосфор очищают обработкой 3-5%-ными водными р-рами минеральных к-т при 70 0C, кипячением с 7%-ным р-ром щелочи, а затем кипячением с деионизированной водой. Фосфор высокой чистоты получают гидридным методом -термич. разложением очищенного ректификацией фосфина.
Определение. Известные р-ции обнаружения и определения фосфора в осн. относятся к ортофосфатным ионам. Для качеств, обнаружения преим. применяют р-цию образования при действии молибдата аммония в азотнокислой среде желтого осадка (или желтого окрашивания р-ра) фосфоромолибдата аммония. Действие молибдата аммония в присут. бензидина или нек-рых др. восстановителей дает синее окрашивание (используют в виде капельной р-ции на фосфор). Аналогичная р-ция применяется для проявления пятен разл. фосфатов в бумажной хроматографии.
Наиб. употребительный гравиметрич. способ определения фосфора (если он находится в низших степенях окисления, его предварительно окисляют) - вышеуказанная р-ция осаждения фосфоромолибдата аммония с послед. переосаждением в виде MgNH4РO4·6H2O и прокаливанием осадка до Mg2P4O7 (весовая форма).
Титриметрич. фосфоромолибдатный метод заключается в осаждении фосфоромолибдата аммония, растворении осадка в титрованном р-ре щелочи и титровании его избытка р-ром к-ты. Близок к нему гидрооксихинолинмолибдатный метод -осаждение фосфоромолибдата 8-гидроксихинолином с послед, растворением в щелочи и кислотным титрованием. Известны методы прямого титрования фосфатов солями разл. металлов (Ag, Pb, Bi, Ce и др.), а также методы осаждения нерастворимых фосфатов (Ag, Bi и т. п.) с послед. титримет-рич. определением металлов.
Наиб. употребляемые фотометрич. методы определения фосфора основаны на р-ции образования желтого фосфоромолибдено-вого комплекса или его восстановленной формы синего цвета.
Применяют разл. физ. методы определения фосфора: спектральные, атомно-адсорбционный, люминесцентный, ЯМР, радио-активационный и др. Для отделения фосфора от др. элементов чаще всего используют экстракционные методы. Для разделения разл. фосфатных анионов обычно применяют бумажную хро-матографию.
Применение. Осн. долю всего добываемого фосфора (~ 90%) используют для получения P2O5 и т. наз. термической фосфорной к-ты, применяемой в произ-ве разл. фосфорных удобрений и разнообразных фосфатов, в т. ч. для животноводства (минеральных подкормок). Используют фосфор также для получения разнообразных фосфорсодержащих неорг. и орг. соединений. Белый фосфор применяют в качестве дымообразующего и зажигат. ср-ва, для изготовления трассирующих боеприпасов.
Красный фосфор используют в спичечной пром-сти как осн. компонент обмазки зажигат. пов-сти спичечных коробков, как компонент термопластичных композиций, в произ-ве ламп накаливания - как газопоглотитель.
В металлургии фосфор применяют как раскислитель при получении нек-рых сплавов, напр. хромаля, как легирующую добавку (фосфористый чугун содержит до 0,8% P, нек-рые стали до 0,3% P, фосфористая бронза до 1,2% P), как компонент припоев и антифрикционных сплавов, магнитомягких сплавов, для фосфатирования пов-сти стальных изделий с целью увеличения их коррозионной стойкости, для получения ферромагн. пленок в элементах памяти вычислит. машин. Фосфор высокой чистоты используют для получения полупроводниковых фосфидов, в осн. типа АIПВ5.
Мировое произ-во фосфора (без стран СНГ) ок. 1 млн. т в год. Осн. производители - США, Германия, Нидерланды, Канада.
Белый фосфор очень ядовит - смертельная доза для человека 0,05-0,15 г. Симптомы острого отравления: желудочно-кишечные расстройства, сердечная недостаточность. При хро-нич. отравлении происходит изменение костей, в частности омертвение челюстей. Попадая на кожу, белый фосфор воспламеняется, давая тяжелые ожоги. ПДК в воздухе рабочей зоны 0,03 мг/м3. Хранят белый фосфор под слоем воды или незамерзающего р-ра (CaCl2 или NaCl, ZnCl2) в темноте.
Красный фосфор менее токсичен, но его пыль может вызывать хронич. отравление, а также пневмонию, поражение кожи. T. к. красный фосфор может воспламеняться, в частности, при трений и ударе, разбивать его слитки рекомендуется орудиями из тефлона. Черный фосфор не токсичен, может обрабатываться без особых предосторожностей.
Фосфор получил в 12 в. арабский алхимик Ахад Бехиль. В Европе фосфор впервые был получен X. Брандом в 1669.
Лит.: Везер В.-Дж., Фосфор и его соединения, пер. с англ., M., 1962; Астахов К. В., Фосфор, M., 1972; Аналитическая химия фосфора, M., 1974; Ершов В. А., Технология производства фосфора, Л., 1978; Технология фосфора, Л., 1979; Корбридж Д., Фосфор. Основы химии, биохимии, технологии, пер. с англ., M., 1982; Миллер Т.Н., Витола А. А., Неорганические соединения фосфора с азотом, Рига, 1986; Физико-химические и технологические основы процесса получения красного фосфора, M., 1987.
П. И. Федоров.

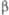 , град
, град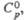 Дж/(моль· К)
Дж/(моль· К)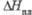 , кДж/моль
, кДж/моль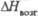 , кДж/моль
, кДж/моль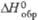 , кДж/моль
, кДж/моль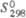 ,Дж/(моль· К)
,Дж/(моль· К) ,Ом· м
,Ом· м