Толуол
Толуол (от испанского tolú — толуанский бальзам, из которого впервые был получен толуол), метилбензол, бесцветная горючая жидкость, по запаху напоминающая бензол; tпл — 95 °С, tkип 110,6 °С, плотность 0,8669 г/см3 (20 °С), пределы взрываемости смеси с воздухом 1,27—7,0% толуола (по объёму), tвоспл 552 °С, tвсп 4,4 °С. Толуол смешивается с большинством органических растворителей; при 22 °С в 1кг воды растворяется 0,492 г толуола, в 1 кг толуола — 0,526 г воды.
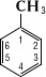 Толуол содержится в некоторых нефтях; в промышленности его выделяют главным образом из каменноугольной смолы и продуктов термической переработки нефтяных фракций. Толуол — важное химическое сырьё; для него характерны реакции электрофильного замещения в бензольном ядре и превращения метильной группы при сохранении ядра. Электрофильное замещение происходит легче, чем в бензоле, и направляется главным образом в пара- и орто-положения (4- и 2-, 6-). Так, нитрование толуола смесью HNO3 и H2SO4 последовательно даёт моно- и динитропроизводные, а затем 2, 4, 6-тринитротолуол (тол, или тротил).
Толуол содержится в некоторых нефтях; в промышленности его выделяют главным образом из каменноугольной смолы и продуктов термической переработки нефтяных фракций. Толуол — важное химическое сырьё; для него характерны реакции электрофильного замещения в бензольном ядре и превращения метильной группы при сохранении ядра. Электрофильное замещение происходит легче, чем в бензоле, и направляется главным образом в пара- и орто-положения (4- и 2-, 6-). Так, нитрование толуола смесью HNO3 и H2SO4 последовательно даёт моно- и динитропроизводные, а затем 2, 4, 6-тринитротолуол (тол, или тротил).
Превращения метильной группы происходят по радикальному механизму. Например, хлорирование при УФ-облучении и нагревании приводит к бензилхлориду C6H5CH2CI, хлористому бензилидену C6H5CHCl2 и бензотрихлориду C6H5CCI3; нитрование раствором HNO3 в уксусной кислоте даёт a-нитротолуол C6H5CH2NO2, окисление — бензиловый спирт C6H5CH2OH, бензойный альдегид C6H5CHO и бензойную кислоту C6H5COOH. Толуол применяется в производстве красителей, взрывчатых веществ, фармацевтических препаратов и различных полупродуктов; используется в качестве растворителя при получении пластмасс, лакокрасочных материалов, типографских красок, в резиновой промышленности и др.
Толуол менее токсичен, чем бензол. Предельно допустимая концентрация паров толуола в воздухе 0,05 мг/л.
Б. Л. Дяткин.
