Гидроксид-анион
ГИДРОКСИД-АНИОН ОН-. Существует в газовой фазе изолированно, находится в кристаллич, решетке гидроксидов и основных солей Наиб. активных металлов, образуется в водных р-рах вследствие диссоциации воды или (и) растворенных гидроксдцов. Для ОН- в газовой фазе: длина связи О—Н 0,096 нм; частота колебаний 3800 см-1; энергия ионизации 176,13 кДж/моль; Сop 29,14 Дж/(моль*К);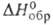 - 143,2 кДж/моль; S°29S 172,32 Дж/(моль*К). ионный радиус и поляризуемость ОН ~ в твердых гидроксидах велики, поэтому гидроксиды имеют рыхлую слоистую кристаллич. структуру с большой долей ковалентной составляющей связи металл—ОН. При гидролизе солей многовалентных металлов образуются не растворимые в воде полиядерные гидроксокомплексы, в к-рых имеются мостиковые связи, осуществляемые с помощью ОН-.
- 143,2 кДж/моль; S°29S 172,32 Дж/(моль*К). ионный радиус и поляризуемость ОН ~ в твердых гидроксидах велики, поэтому гидроксиды имеют рыхлую слоистую кристаллич. структуру с большой долей ковалентной составляющей связи металл—ОН. При гидролизе солей многовалентных металлов образуются не растворимые в воде полиядерные гидроксокомплексы, в к-рых имеются мостиковые связи, осуществляемые с помощью ОН-.
Для ОН- в бесконечно разб. водном р-ре: относительные парциальные моляльные теплоемкость и энтропия равны соотв. —139,7 и — 10,5 Дж/(моль*К);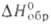 - 230,0 кДж/моль; абс. подвижность 17,8*10-8 м2/(с*В). Присутствие в водном р-ре ОН- в концентрациях выше 10-7 моль/л приводит к щелочной р-ции р-ра. Ион ОН-играет большую роль в хим. и биол. процессах в водных средах., п. м. Чукуров.
- 230,0 кДж/моль; абс. подвижность 17,8*10-8 м2/(с*В). Присутствие в водном р-ре ОН- в концентрациях выше 10-7 моль/л приводит к щелочной р-ции р-ра. Ион ОН-играет большую роль в хим. и биол. процессах в водных средах., п. м. Чукуров.

Дополнения к описанию гидроксид-аниона: