Дебая-Хюккеля теория
ДЕБАЯ - ХЮККЕЛЯ ТЕОРИЯ, статистич. теория разбавленных р-ров сильных электролитов, позволяющая рассчитать коэф. активности ионов. Основана на предположении о полной диссоциации электролита на ионы, к-рые распределены в р-рителе, рассматриваемом как непрерывная среда. Каждый ион действием своего электрич. заряда поляризует окружение и образует вокруг себя нек-рое преобладание ионов противоположного знака - т. наз. ионную атмосферу. В отсутствие внеш. электрич. поля ионная атмосфера имеет сферич. симметрию и ее заряд равен по величине и противоположен по знаку заряду создающего ее центр. иона. Потенциал j суммарного электрич. поля, создаваемого центр. ионом и его ионной атмосферой в точке, расположенной на расстоянии r от центр. иона, м.б. рассчитан, если ионную атмосферу описывать непрерывным распределением плотности r заряда около центр. иона. Для расчета используют ур-ние Пуассона (в системе СИ):n2j = -r/ee0,
где n2-оператор Лапласа, e - диэлектрич. проницаемость р-рителя, e0 - электрич. постоянная (диэлектрич. проницаемость вакуума). Для каждого i-го сорта ионов r описывается ф-цией распределения Больцмана; тогда в приближении, рассматривающем ионы как точечные заряды (первое приближение Дебая - Хюккеля теории), решение ур-ния Пуассона принимает вид:
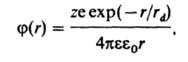
где z - зарядовое число центр. иона, rd - т. наз. дебаевский радиус экранирования (радиус ионной атмосферы). На расстояниях r > rd потенциал j становится пренебрежимо малым, т. е. ионная атмосфера экранирует электрич. поле центр. иона. Величина rd равна радиусу сферы, заряд к-рой равен заряду центр. иона и к-рая создает в месте нахождения центр. иона такой же потенциал, что и ионная атмосфера; значение rd выражается ф-лой:
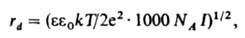
где k - постоянная Больцмана, Т - т-ра, NA - постоянная Авогадро, I - т. наз. ионная сила р-ра, зависящая от состава. Она определяется выражением:
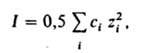
где сi - молярная концентрация i-го иона в моль/см3, zi - eгo зарядовое число; суммирование производится по всем типам ионов, присутствующих в р-ре. Дебая - Хюккеля теория дает возможность рассчитать средний ионный коэф. активности из выражения (предельный закон Дебая-Хюккеля):
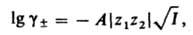
где коэф. А выражается ф-лой:
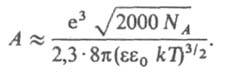
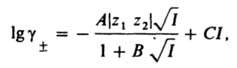
где В и С - эмпирич. постоянные. Ограниченность Дебая - Хюккеля теории обусловлена пренебрежением ассоциаций ионов, представлением о р-рителе как о непрерывной среде, характеризуемой только значением e, т. е. неучетом мол. структуры р-рителя и его взаимод. с ионами. Дебая - Хюккеля теория является основой теории электропроводности разбавл. р-ров сильных электролитов, разработанной Л. Онсагером. Она позволяет объяснить увеличение электропроводности р-ра при повышении напряженности постоянного электрич. поля (эффект Вина) и в высокочастотном поле (эффект Дебая-Фалькенхагена). В этих условиях ионная атмосфера, тормозящая движение ионов, не успевает образоваться (см. Электропроводность электролитов). Теория создана П. Дебаем и Э. Хюккелем в 1923.
Литература
