Ниренштайна реакция
НИРЕНШТАЙНА РЕАКЦИЯ (Клиббенса-Ниренштайна р-ция), получение жирно-ароматич. хлорметилкетонов взаи-мод. хлорангидридов карбоновых к-т с диазометаном:
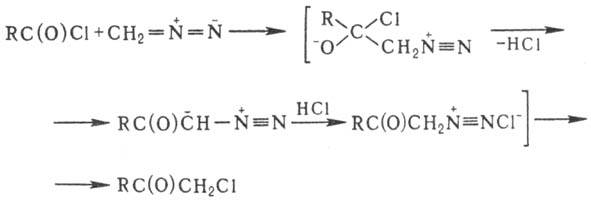
Р-цию осуществляют обычно при комнатной т-ре, прибавляя избыток р-ра диазометана к р-ру хлорангидрида в эфире или бензоле. Выходы хлорметилкетонов 65-95%. При обратном порядке прибавления реагентов образуются диа-зокетоны (см. Арндта-Айстерта реакция).
В Ниренштайна реакцию легко вступают хлорангидриды замещенных бензойной к-ты (содержащих в кольце, напр., нитро-, метокси-или ацилоксигруппы) или фенилуксусных к-т, напр.:
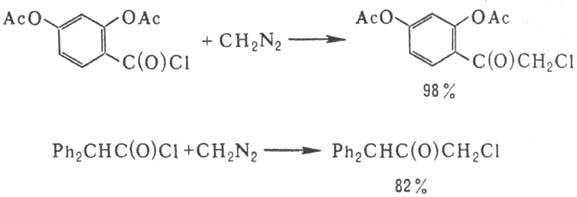
Побочный процесс - образование дигалоген-1,4-диокса-нов:
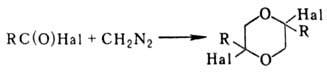
Эта р-ция становится преобладающей при использовании бромангидридов или стерически затрудненных хлорангидридов, напр. Ph3CC(O)Cl.
Ниренштайна реакция имеет препаративное значение; ее открыли в 1915 М. Ниренштайн и Д. Клиббене.
Лит.: Кнунянц И. Л., Кисель Я.М., Быховская Э. Г., "Изв. АН СССР, сер. хим.", 1956, № 3, с. 377-79; Miyahara Y., "J. Heterocycl. Chem.", 1979, v. 16, № б, р. 1147-51. К. В. Вацуро.
Комментарии*
Дополнения к описанию реакции Ниренштайна:
- Механизм реакции: Реакция протекает через образование промежуточного диазокетона, который под действием хлористого водорода (выделяющегося в ходе реакции) или добавленного хлорирующего агента (например, HCl) претерпевает перегруппировку и замещение с образованием целевого хлорметилкетона.
- Препаративное значение: Получаемые хлорметилкетоны являются ценными бифункциональными синтонами в органическом синтезе. Активированная метиленовая группа (-CH2Cl) может участвовать в нуклеофильном замещении (например, в реакции с аминами), а карбонильная группа — в различных карбонильных реакциях (восстановление, образование оснований Шиффа и т.д.). Это делает их полезными интермедиатами для синтеза гетероциклических соединений, фармацевтических субстанций и других сложных молекул.
- Современный контекст: Из-за высокой токсичности и взрывоопасности диазометана в лабораторной практике реакцию Ниренштайна часто стараются заменить более безопасными методами, например, использованием реагентов типа диазометана, иммобилизованных на полимерном носителе, или альтернативными синтетическими подходами к получению α-галогенкетонов.
*Подобраны с помощью LLM, верифицированы, но возможны неточности.


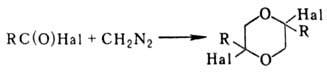

Дополнения к описанию реакции Ниренштайна: