Нитрозодифениламины
НИТРОЗОДИФЕНИЛАМИНЫ. Различают N- и С-нитрозодифениламины N-Н и т р о з о д и ф е н и л а м и н (ф-ла Г), мол.м. 198,14, кристаллы от желтого до коричневого цвета моноклинной сингонии (а = 1,708 нм, b = 0,8867 нм, с = 2,867нм, b 90,97°, пространств. группа С2/т): т. пл. 68 °С; m 10,37.10-30 Кл.м; DH0сгор - 6388 кДж/моль. В УФ спектре максимум поглощения при 295 нм; в ИК спектре характеристич. полоса 1340 см-1 (vNO). При нагр. раств. в воде, этаноле, бензоле; р-римость в 100 г ССl4 при 20 °С 34,1 г.
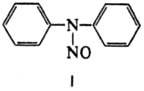
Соед. I типичный представитель N-нитрозосоединений (см. Нитрозамины). При нитровании превращ. в смесь 2- и 4-нитро-N-нитрозодифениламинов, восстановление его приводит к смеси дифениламина и N,N-дифенилгидразина. При обработке соляной к-той I претерпевает Фишера-Хеша перегруппировку с образованием 4-нитрозодифениламина. Получают соед. I нитрозированием дифениламина нитритом Na в смеси этанола с НСl при сильном охлаждении.
4-Н и т р о з о д и ф е н и л а м и н ONC6H4NHC6H5, сине-зеленые кристаллы, т.пл. 145,6-146,6 °С, lмакс 421 нм. Раств. в этаноле, уксусной к-те, не раств. в воде. По хим. св-вам -типичный представитель ароматич. С-нитрозосоединений (см. Нитрозосоединения). Гидрирование 4-нитрозодифениламина приводит к соответствующему аминодифениламину. Получают 4-нитрозодифениламин нитрозированием дифе-нила с послед. перегруппировкой образующегося соед. I (без его выделения).
С-Нитрозодифениламины-промежут. продукты в синтезе основных и катион-ных красителей феноксазинового ряда; 4-нитрозодифениламин применяют также в качестве реактива при колори-метрич. определении Pd. N-Нитрозодифениламины-источники получения С-нитрозодифениламинов и аминодифениламинов; их, как правило, не выделяют из реакц. смесей, а сразу же подвергают дальнейшей переработке; обладают канцерогенными св-вами.
Лит.: Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов, Л., 1980, с. 164. В. И. Рыбинов.
