Нитрозамины
НИТРОЗАМИНЫ (N-нитрозоамины), соед. общей ф-лы RR'NNO (R, R'= Alk, Ar). Первичные нитрозамины (R = Н) существуют лишь при т-ре ниже О °С. Известны также N-нитрозоамиды общей ф-лы RN(X)NO (X = CONH2, CO2Alk и др.).
Нитрозамины-жидкости или твердые в-ва желтого цвета (см. табл.), раств. в воде и мн. орг. р-рителях, при обычной т-ре устойчивы лишь огранич. время. Атомы в молекуле нитрозаминов расположены в одной плоскости. В N-нитрозодиметиламине длина связей N—N 0,134 нм, N—О 0,124 нм, угол NNO 119°. Большой барьер вращения вокруг связи N—N (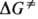 75-160 кДж/моль) позволяет разделять Е- и Z-изоме-ры. В ИК спектрах нитрозаминов присутствуют две характеристич. полосы при 1430-1530 (N=O) и ок. 1000 см-1 (N—N). В УФ спектре lмакc 360 нм (e
75-160 кДж/моль) позволяет разделять Е- и Z-изоме-ры. В ИК спектрах нитрозаминов присутствуют две характеристич. полосы при 1430-1530 (N=O) и ок. 1000 см-1 (N—N). В УФ спектре lмакc 360 нм (e 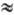 100) и 230-255 нм (e
100) и 230-255 нм (e 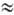 5000), отвечающие п
5000), отвечающие п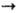 p* и p
p* и p p*-переходам соответственно. В спектрах ПМР сигнал a-Н-атома цис-изомера сдвинут в более сильное поле по сравнению с соответствующим сигналом транс-изомера на 0,2-0,6 м. д. В спектрах ЯМР на ядрах N хим. сдвиг dN ок. 200 м. д. (N=O) и —150м. д. (аминогруппа).
p*-переходам соответственно. В спектрах ПМР сигнал a-Н-атома цис-изомера сдвинут в более сильное поле по сравнению с соответствующим сигналом транс-изомера на 0,2-0,6 м. д. В спектрах ЯМР на ядрах N хим. сдвиг dN ок. 200 м. д. (N=O) и —150м. д. (аминогруппа).
СВОЙСТВА НЕКОТОРЫХ N-НИТРОЗАМИНОВ И N-НИТРОЗОАМИДОВ

Мн. восстановители (H2/Pt или H2/Pd, LiAlH4 и др.) превращают нитрозамины в несимметричные гидразины, в более жестких условиях (под действием Н2 над Ni-Ренея или амальгамы Na) происходит разрыв связи N—N и образуются вторичные амины. Дитионит Na дезоксигенирует нитрозамины, образуя диалкиламинонитрены 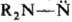 (см. Нитрены); HNO3 или CF3CO3H окисляют их в соответствующие N-нитрами-ны. Под действием ангидридов орг. к-т или НСl нитрозамины соотв. ацилируются или хлорируются с разрывом связи N—N. Сильные алкилирующие агенты взаимод. с нитрозаминами по атому кислорода группы NO, напр.:
(см. Нитрены); HNO3 или CF3CO3H окисляют их в соответствующие N-нитрами-ны. Под действием ангидридов орг. к-т или НСl нитрозамины соотв. ацилируются или хлорируются с разрывом связи N—N. Сильные алкилирующие агенты взаимод. с нитрозаминами по атому кислорода группы NO, напр.:
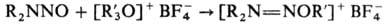
При парофазном фотолизе нитрозаминов разрывается связь N—N, при этом генерируется радикал 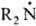 ; в жидкой фазе в присут. к-т нитрозамины фотолитически присоединяются к алкенам, напр.:
; в жидкой фазе в присут. к-т нитрозамины фотолитически присоединяются к алкенам, напр.:
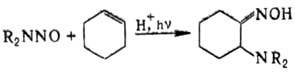
Ароматические нитрозамины в присут. к-т претерпевают внутримол. перегруппировку с образованием и-нитрозоариламинов. N-Нитрозоамиды под действием NH3 или оснований дают диазосоед., напр.:
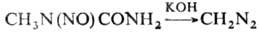
Общий метод синтеза нитрозаминов- нитрозирование вторичных аминов или амидов с помощью NaNO2 (в слабокислой среде), N2O3, N2O4, NO2BF4, N-нитрозо-3-карбазола и др. агентов. Нитрозамины получают также р-цией вторичных аминов с NaNO2 и СН3О или хлоралем, напр.:
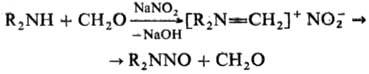
Иногда используют р-цию R2NCOCl с AgNO2 или восстановление N-нитроаминов Аl в щелочной среде.
Нитрозамины используют для извлечения вторичных аминов из смесей, в синтезе лек. препаратов и орг. красителей, в лаб. практике для получения диазоалканов.
Нитрозамины-высокотоксичные соед., они поражают печень, вызывают кровоизлияния, конвульсии, кому. Большинство нитрозаминов-сильные канцерогены, нек-рые из них оказывают действие уже при одноразовой экспозиции. Нитрозамины-сильные мутагены, легко метаболизируются, в организме действуют гл. обр. как алкилирующие агенты, N-нитрозо-N-метилмочевина обладает противоопухолевой активностью.
Лит.: Химия нитро- и нитрозогрупп, пер. с англ., т. 1, М., 1972, с. 100-19; т. 2, М., 1973, с. 156-210; Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 449-59; Костюковский Я.Л., МаламедД.Б., "Успехи химии", 1988, т. 57, в. 4, с. 625-55. С. Л. Иоффе.
