Аминов
АМИНОВ N-ОКСИДЫ (N-окиси аминов), производные третичных аминов и гетероароматич. соединений, содержащие семиполярную связь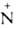 —О-. Большинство хорошо раств. в воде, ограниченно-в неполярных орг. р-рителях. Образуют с к-тами устойчивые кристаллич. соли
—О-. Большинство хорошо раств. в воде, ограниченно-в неполярных орг. р-рителях. Образуют с к-тами устойчивые кристаллич. соли
R3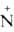 OHX-. Расположение четырех заместителей у атома азота тетраэдрическое.
OHX-. Расположение четырех заместителей у атома азота тетраэдрическое.
СВОЙСТВА N-ОКСИДОВ АМИНОВ
| Показатель Т. пл., °С | (СН3Ь 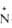 -O-212,0 -O-212,0 | С6Н5(СН3)2 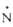 -O -O | С5Н5 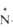 -O-65,6 -O-65,6 |
| Т. кип., °С | — | 154,0 | 100* |
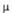 *10-30, Кл-м *10-30, Кл-м | 16,7 | 16,15 | 14,11 |
| рКа | 4,65 | 4,21 | 1,90 |
| Потенциал полуволны восстановления, В | -0,456 | -0,705 | - 1,278 |
| v( 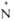 ->O-), см-1 ->O-), см-1 | 930-970 | — | 1230-1320 |
* При 1 мм рт. ст.
Аминов N-оксиды -более слабые основания, чем исходные амины. Их основные св-ва определяются отрицат. зарядом на кислороде, по к-рому происходит как присоединение протона, так и алкилирование. При действии арилгалогенидов образуются соли тетразамещенного гидроксиаммония, разлагающиеся при обработке щелочью:
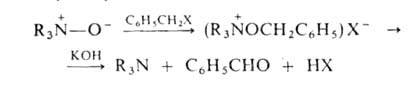
При ацилировании аминов N-оксидов происходят след. превращения:
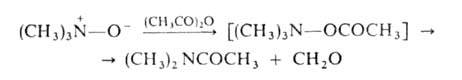
При нагр. алифатич. аминов N-оксид образуют замещенные гидроксиламины (перегруппировка Майзенхаймера) или олефины (перегруппировка Коупа), напр.:
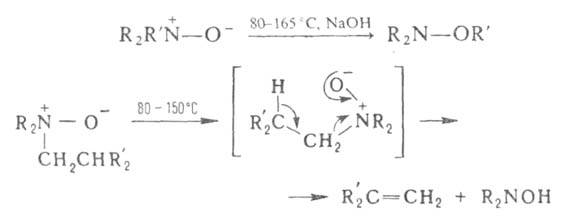
где R - Alk, Ar; R' = СН2С6Н5, СН(С6Н5)2, СН2СН=СН2.
Аминов N-оксиды восстанавливаются до аминов гидрированием на Ni или Pd, а также действием производных трехвалентного фосфора, напр. (С6Н5bР- В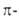 электронной системе цикла гетероциклич. аминов N-оксидов группа
электронной системе цикла гетероциклич. аминов N-оксидов группа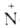 —О- может играть роль как донора, так и акцептора электронов. Поэтому аминов N-оксиды такого типа вступают в р-ции электроф. и нуклеоф. замещения легче, чем соответствующие амины. Ацилирование гетероциклич. аминов N-оксидов происходит след. образом:
—О- может играть роль как донора, так и акцептора электронов. Поэтому аминов N-оксиды такого типа вступают в р-ции электроф. и нуклеоф. замещения легче, чем соответствующие амины. Ацилирование гетероциклич. аминов N-оксидов происходит след. образом:
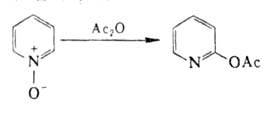
N-Оксиды пиридина и его гомологов, производных хинолина нитруются до 4-нитропроизводных. При р-ции с РОС13, РС15, SOC12 образуются 1- и 4-хлорпроизводные, с ангидридами и галогенангидридами к-т-2-ацилоксипроизводные с металлоорг. соед.-2-алкилпроизводные, с анионом CN- в присут. хлористого бензоила-4-цианпиридин.
Общий метод получения аминов N-оксидов -окисление третичных аминов действием Н2О2 в нейтральной (алифатич. амины) или кислой (ароматич. амины) средах, реже - озоном или надкислотами (азотистые гетероциклы). Применяется также исчерпывающее алкилирование гидроксиламина и его производных, циклизация нитро- и нитрозосоединений. Методы анализа аминов N-оксидов основаны на восстановлении группы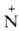 —О- (потенциометрия).
—О- (потенциометрия).
Алифатич. аминов N-оксиды -ПАВ в космети-ке и парфюмерии, коагулирующие и желатинизирующие агенты, ингибиторы полимеризации, р-рители целлюлозы. Нек-рые аминов N-оксиды обладают противомикробной и противогрибковой активностью.
Литература
Иоффе Д.В., ЭфросЛ.С, "Успехи химии", 1961, т. 30, в. 11. с. 1325-51; Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 247-51; Katritzky A.R., Lagowski J.M., Chemistry of the heterocyclic N-oxides, L.-N.Y.. 1971. Д.В.Иоффе.
