Нитрозосоединeния
НИТРОЗОСОЕДИНEНИЯ (С-нитрозосоединения), содержат в молекуле одну или неск. нитрозогрупп —N=O, связанных с атомами углерода. Известны также N- и О-нитрозосоединения (см. Нитрозамины и Нитриты органические). Обычно нитрозосоединения существуют в виде равновесной смеси мономера и димера (для последнего характерна геом. изомерия):
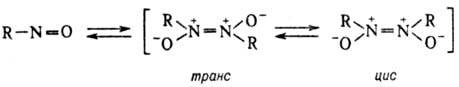
Назв. мономерных нитрозосоединений производят прибавлением префикса "нитрозо" к назв. соединения-основы.
В индивидуальном состоянии большинство нитрозосоединений находятся в виде димеров, однако введение электроноакцепторных заместителей в орг. остаток приводит к преобладанию мономеров (напр., трихлор- и трифторнитрозометаны). В димер-ных нитрозосоединениях транс-изомеры стабильнее цис-изомеров. В р-рах или при нагр. димерные нитрозосоединения диссоциируют, по крайней мере частично. Вицинальные ароматические нитрозосоединения или непредельные димерные нитрозосоединения димеризуются специфически, давая фуроксаны, а перфторалкильные нитрозосоединения при облучении димеризуются в соответствующие О-нитрозогидроксиламины, напр.:
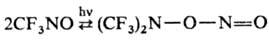
Нитрозогруппа в мономерных и димерных нитрозосоединений-плоская, напр. для нитрозометана длины связей 0,149 нм (С—М) и 0,122 нм (N—О), угол CNO 112,6°.
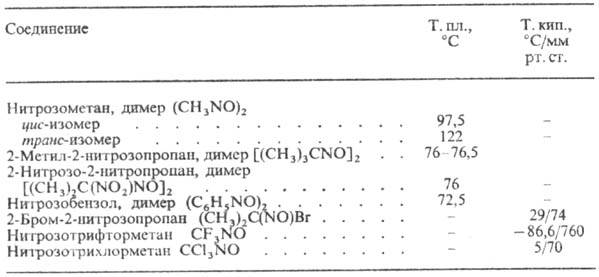
Физические свойства. Мономерные нитрозосоединения-газы или жидкости голубого или зеленого цвета, хорошо раств. во мн. орг. р-рителях, димерные нитрозосоединения-бесцв. кристаллы, раств., как правило, в полярных р-рителях. Св-ва нек-рых нитрозосоединений приведены в таблице.
В И К спектрах нитрозосоединений присутствуют интенсивные полосы, соответствующие валентным колебаниям группы NO: для мономерных алифатических и ароматических нитрозосоединений при 1540-1620 или 1500-1512 см-1 соотв.; для транс-димеров алифатических и ароматических нитрозосоединений при 1176-1290 и 1253-1299 см-1; у цис-димеров эти полосы смещены в область больших частот и проявляются в виде дублетов при 1323-1344 и 1330-1420 см-1 (алифатические нитрозосоединения) и 1389 и 1409 см-1 (ароматические нитрозосоединения).
СВОЙСТВА НЕКОТОРЫХ НИТРОЗОСОЕДИНЕНИЙ
В УФ спектрах мономерных нитрозосоединений наблюдаются три максимума: 630-790 нм (e 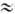 45-60, п
45-60, п p-переход), 270-290 нм (e
p-переход), 270-290 нм (e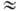 80, о
80, о p*-переход) и 220 нм (e
p*-переход) и 220 нм (e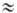 5.103, п
5.103, п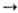 p*-пере-ход). Для транс-димеров lмакс 280-300 нм (e
p*-пере-ход). Для транс-димеров lмакс 280-300 нм (e 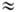 5.103 -— 12.103, p
5.103 -— 12.103, p p*-переход), а для цис-димеров этот максимум сдвинут в коротковолновую область на 10-15 нм.
p*-переход), а для цис-димеров этот максимум сдвинут в коротковолновую область на 10-15 нм.
В спектрах ПМР нитрозосоединений хим. сдвиги a-Н-атома близки к хим. сдвигам аналогичных протонов в соответствующих нитро-соед., причем они различны для мономеров и цис-, и транс-димеров нитрозосоединений, что позволяет оценить их количественно в равновесной смеси. В спектре ЯМР на ядрах N хим. сдвиги нитрозосоединений весьма характерны, хотя и проявляются в широком диапазоне в значительно более сильных полях, чем в соответствующих нитросоед. (5 от 300 до 550 м.д.).
Химические свойства. Особенность алифатических нитрозосоединений, содержащих a-Н-атом,-их необратимая изомеризация в оксимы:
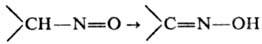
Р-ция катализируется основаниями, водой и полярными р-рителями. Окислители (О3, Н2О2, орг. перкислоты, О2 воздуха и др.) окисляют нитрозосоединения в соответствующие нитросоединения. Восстановление нитрозосоединений в зависимости от восстановителя приводит к гидроксиламинам [NaBH4, арсенат (III) и т. п.] или к аминам (металл в к-те, Н2 над Ni-Ренея и др.), причем процесс осложняется конденсацией нитрозосоединений с промежуточными и конечными продуктами соотв. в азокси- и азосоединения. При действии производных Р(III) происходит дезоксигенирование нитрозосоединений с образованием нитренов 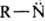 , к-рые далее конденсируются с исходным нитрозосоединением или вступают во взаимод. с р-рителем.
, к-рые далее конденсируются с исходным нитрозосоединением или вступают во взаимод. с р-рителем.
Нитрозосоединения взаимод. с N,N-дигалогенаминами в присут. солей Сu+ с образованием азоксисоед. RN(O)=NR'. Для нитрозосоединений характерны р-ции по кратным связям. Так, с олефинами возможны три типа превращений: а) 1,2-присоединение с образованием оксазетидинов; б) 1,4-присоединение (диеновый синтез) с образованием дигидрооксазинов; в) конденсация двух молекул нитрозосоединений с одной молекулой олефина, приводящая к дигидро-1,3-диокса-2,4-диазинам:
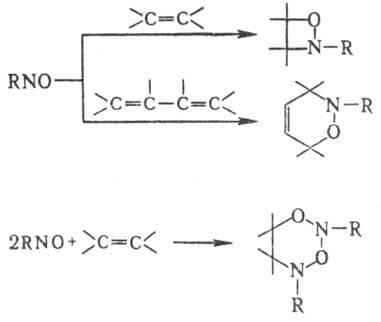
Направление р-ции зависит от природы нитрозосоединения и олефина.
С илидами серы нитрозосоединения взаимод. по схеме переилидирования, давая нитроны, а с илидами фосфора - по типу р-ции Витти-га, образуя азометины:
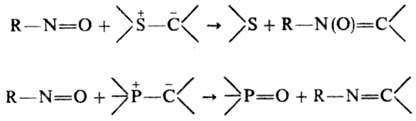
Ароматические нитрозосоединения реагируют с соед. с активной метиле-новой группой в присут. основных катализаторов, образуя N-ариламины или нитроны:
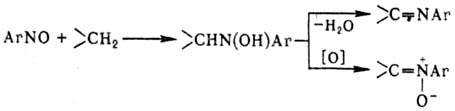
Нитрозосоединения присоединяют HN3 по связи N=O и нек-рые др. к-ты, а также реактивы Гриньяра.
Третичные и ароматические нитрозосоединения с активными радикалами R. образуют стабильные нитроксильные радикалы, напр.:
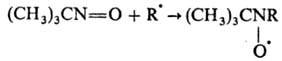
Это св-во позволяет использовать нитрозосоединения в спиновых ловушек методе.
Получение. Общий способ получения нитрозосоединений-окисление первичных аминов к-той Каро (выход нитрозосоединений 30-70%) или гидро-ксиламинов орг. перкислотами, Наl2, HgO и др. Можно использовать окисление орг. перкислотами азометинов, нитронов (окислителем м. б. также О3) и диметилсульфид-иминов (в неполярном р-рителе), напр.:
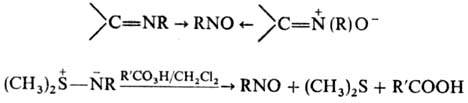
Нитрозосоединения получают также введением нитрозогруппы в молекулу орг. соед. путем замещения атома водорода (нитрозирование). Для синтеза функционально замещенных алифатических нитрозосоединений используют нитрозирование соед., содержащих активирующие группы [COR, NO2, CN, C(R)=NH] у нитро-зируемого атома углерода; нитрозирующие агенты-N2O3 или NaNO2/H2SO4. Нитрозирование этими же реагентами вторичных нитросоед.- общий способ получения псевдонит-ролов RR'C(NO)NO2. Для получения алифатических нитрозосоединений можно использовать радикальное нитрозирование углеводородов, а также действие NO на алхилиодиды (в синтезе перфторалкилнитрозосоед.), напр.:
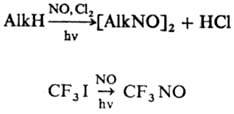
При действии на кетоксимы галогенов образуются a-хлор-нитрозосоед., в присут. N2O4 — псевдонитролы, при действии тетраацетата Pb-a-ацетоксинитрозосоед., напр.:
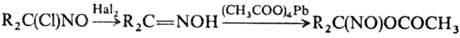
Вицинальные хлор- или нитрозамещенные нитрозосоединения получают с хорошим выходом присоединением соотв. NOCl или N2O3 к олефинам. При действии этих же реагентов на Ag-соли или ангидриды карбоновых к-т карбоксильная группа заменяется на группу NO, напр.:
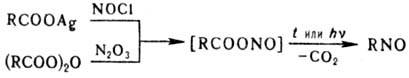
Однако этот метод синтеза нитрозосоединений менее распространен.
Нек-рые нитрозосоединения можно получить действием NOCl на ртутьорг. производные, напр.:
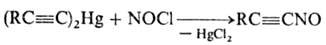
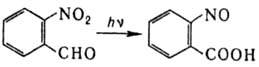
Специфич. методы синтеза ароматических нитрозосоединений-нитрозирование ароматич. аминов или фенолов действием NaNO2/ H2SO4 с образованием соотв. пара- и орто-замещенных продуктов. Для получения ароматических нитрозосоединений иногда используют внутримол. диспропорционирование, напр.:
Анализ и применение. Для обнаружения нитрозосоединений используют их взаимод. с фенолом (резорцином) и конц. H2SO4, приводящее к появлению темно-красного окрашивания, переходящего в темно-голубое после добавления водного р-ра NaOH (р-ция Либермана), или появление интенсивного голубого окрашивания при обработке нитрозосоединений смесью H2SO4 с дифениламином. Количественно нитрозосоединения определяют волюмометрически по выделению азота после обработки нитрозосоединений фенилгидразином.
Нитрозосоединения применяют как полупродукты в синтезе гетероциклич. соед., аминокислот и др. Нитрозофенолы используют для получения красителей и лек. препаратов, фторсодержащие и нек-рые др. Нитрозосоединения-в синтезе эластомеров (см. Фторкаучуки)и для отверждения полимерных композиций, напр. в произ-ве термостойких каучуков.
Нек-рые нитрозосоединения обладают мутагенной и канцерогенной активностью, а также вызывают кожные заболевания.
Лит.: Химия нитро- и нитрозогрупп, пер. с англ., т. 1, М., 1972, с. 100-19, 158-224; т. 2, М., 1973, с. 176-220; Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 372-99; Беляев Е. Ю., Гидаспов Б. В., Ароматические нитрозо-соединения, Л., 1989. С. Л. Иоффе.
