Физические и химические свойства
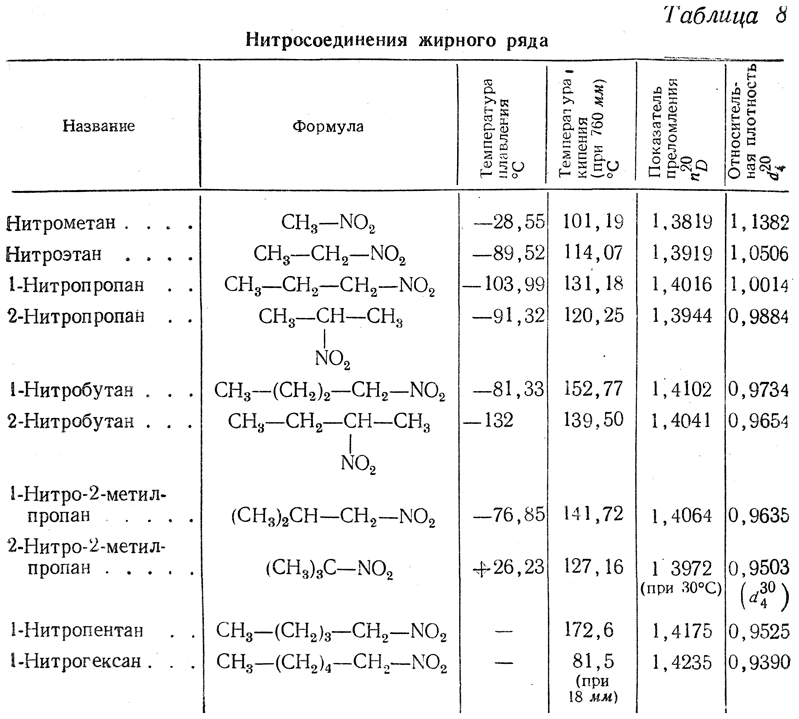
Низшие гомологи нитросоединений — жидкости, не имеющие неприятного запаха, нерастворимые в воде, смешивающиеся со спиртом и эфиром. Нитрометан кипит при 101° С; у последующих гомологов температуры кипения повышаются, обнаруживая правильности, общие для всех гомологических рядов. Плотности низших нитросоединений больше единицы; с увеличением молекулярного веса плотности нитросоединений уменьшаются.
Химические свойства.
1. Действие щелочей и обра зование изонитросоединений.
Нитросоединения ряда метана — вполне нейтральные вещества. Однако первичные и вторичные нитросоединения при взбалтывании с растворами едких щелочей медленно растворяются в них, образуя растворимые в воде вещества, обладающие всеми свойствами нейтральных солей. Эти вещества представляют собой собственно не соли нитросоединений, а соли изомерных им изонитросоединений, являющихся сильными кислотами.
Взаимодействие нитросоединений с щелочами протекает следующим образом:
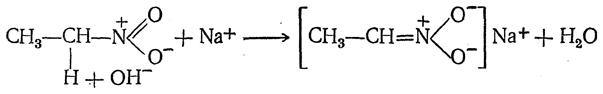
Изомеризация нейтральных нитросоединений в кислые изонитросоединения подтверждается тем, что при действии сильной кислоты на соль изонитросоединения (I) нерастворимое в воде нитросоединение (III) получается не сразу; сначала выделяется хорошо растворимое в воде изонитросоединение (II), лишь постепенно превращающееся в нитросоединение (III):
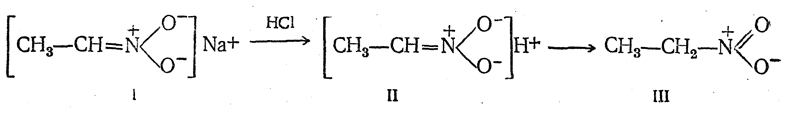
Простейшие изонитросоединения не удалось выделить в чистом виде, так как их превращение в истинные нитросоединения происходит очень быстро, хотя и не мгновенно. Некоторые более сложные изонитросоединения были получены и в чистом виде.
Случаи, подобные превращениям нитросоединений, когда нейтральные вещества со щелочами дают соли изомерных им сильных кислот, а также когда нейтральные вещества с кислотами дают соли сильных оснований, нередки среди органических веществ и относятся к области явлений таутомерии.
Нейтральным веществам, ведущим себя подобным образом, Ганч дал названия псевдокислот и соответственно псевдооснований.
2. Действие концентрированных минеральных кислот. При действии концентрированных минеральных кислот нитросоединения превращаются в карбоновые кислоты, отщепляя гидроксиламин. Это превращение происходит по следующей схеме:
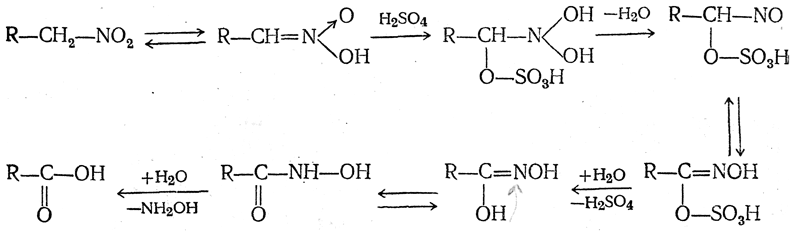
3. Действие азотистой кислоты. Весьма характерной реакцией, позволяющей различить первичные, вторичные и третичные нитросоединения, является их взаимодействие с азотистой кислотой.
а) Первичные нитросоединения (и нитрометан) реагируют с азотистой кислотой, выделяя молекулу воды и образуя так называемые нитроловые кислоты:
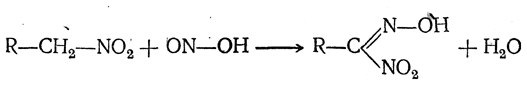
Щелочные соли нитроловых кислот окрашены в ярко-красный цвет, являющийся при этой реакции признаком первичного нитросоединения.
б) Вторичные нитросоединения с азотистой кислотой также выделяют воду, давая соединения, называемые псевдонитролами:
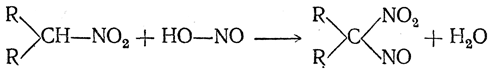
Эти вещества в кристаллическом состоянии бесцветны, но в расплавленном состоянии и в растворах (в эфире, хлороформе и пр.) обладают интенсивной бирюзовой окраской.
в) Третичные нитросоединения не реагируют с азотистой кислотой.
Эти реакции играют важную роль при установлении строения углеводородных радикалов не только у нитросоединений, но и у галоидных алкилов, спиртов и других веществ, которые легко превратить в нитросоединения.
4. Действие галоидов на щелочные растворы нитросоединений. Этим способом можно заместить во вторичных нитросоединениях один, а в первичных нитросоединениях один или два атома водорода на атомы галоида и получить таким образом соединения:
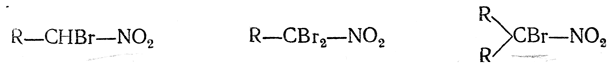
Такое строение образующихся галоиднитросоединений доказывается тем, что при действии на них цинкорганических соединений галоид замещается на алкил и получаются высшие гомологи нитросоединений (И. И. Бевад):
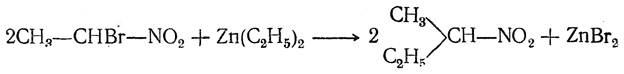
5. Восстановление. При восстановлении нитросоединений образуются первичные амины:

Эта реакция доказывает, что в нитросоединениях атом азота непосредственно связан с атомом углерода алкила. Напротив, при восстановлении изомерных нитросоединениям эфиров азотистой кислоты, в которых алкил связан с кислородом, получаются спирт и аммиак или гидроксиламин:
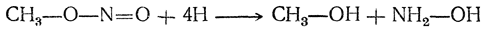
Впервые синтез первичных аминов восстановлением нитросоединений был осуществлен Н. Н. Зининым (1842) применительно к ароматическим соединениям (получение анилина и α-нафтиламина). В дальнейшем восстановление ароматических нитросоединений было широко изучено и сделалось основным способом получения ароматических аминов.
Восстановление жирных нитросоединений значительно менее изучено. Однако и здесь уже известны реакции, при которых получаются продукты неполного восстановления, например альдоксимы и кетоксимы. Вероятно, в этих случаях восстанавливаются изонитросоединения:

Оксимы в условиях восстановления оловом и соляной кислотой могут гидролизоваться, распадаясь на гидроксиламин и альдегиды или кетоны, или давать β-алкилгидроксиламины R—СН2—NH—ОН.
6. Конденсация с альдегидами. Первичные и вторичные нитросоединения под действием щелочей легко вступают в реакции конденсации с альдегидами за счет атомов водорода, находящихся в α-положении к нитрогруппе. При этом с формальдегидом реагируют все имеющиеся α-атомы водорода, а с другими альдегидами только один такой атом. Соответственно, нитрометан с формальдегидом образует трехатомный спирт
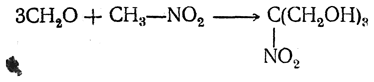
который, подобно глицерину, при этерификации азотной кислотой дает тринитрат C(NO2)(CH2ONO2)3, чрезвычайно мощное взрывчатое вещество.
С другими альдегидами получаются одноатомные спирты:
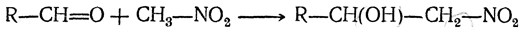
При известных условиях получившийся нитроспирт может терять элементы воды и превращаться в R—СН=СН—NO2.


