Нитрометан
НИТРОМЕТАН CH3NO2, мол.м. 61,042; бесцв. жидкость с запахом горького миндаля; т. пл. — 28,55 °С; т. кип. 100,8 °С; d420 1,1371; nD20 1,3817; m 11,67.10-30 Кл.м; л 0,646 мПа.с (20 °С); g 37,48 мН/м; DH0пл 9,7 кДж/моль, DH0исп 38,28 кДж/моль, DH0обр -113,1 кДж/моль, DH0сгор -708,4 кДж/моль; 6 35,87 (30 °С); рКа 10,2. Р-римость нитрометана в воде 9,5 мл в 100 мл, воды в нитрометане 2,2 мл в 100 мл, образует азеотропную смесь с водой (76,4% по массе нитрометана, т. кип. 83,6°С); хорошо раств. в орг. р-рителях (кроме алифатич. углеводородов).
По хим. св-вам нитрометан-типичный представитель алифатич. питросоединений. Специфич. св-ва нитрометана связаны с наличием трех реакционноспособных связей С—Н, а также с нестабильностью метаннитронатов - производных аци-фор-мы. На этом основано применение нитрометана в синтезе нитроцетатов:
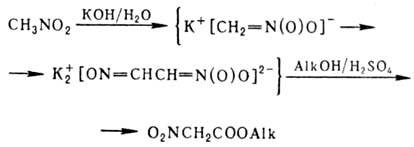
При взаимодействии нитрометана с пирилиевыми солями образуются ароматич. нитросоед.; с помощью нитрометана происходит расширение цикла в циклоалканонах, напр.:
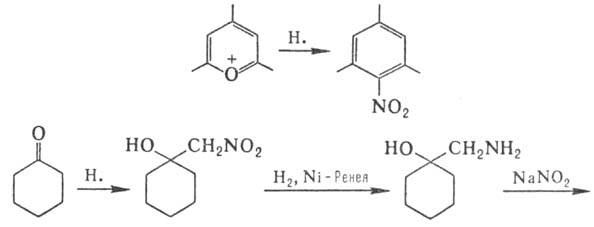
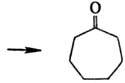
В пром-сти нитрометан получают деструктивным нитрованием низших алканов (напр., пропана) 50-70%-ной HNO3 при 400-700 °С в проточном реакторе (трубка Ni-Cr, время контакта до 2 с). Из реакц. смеси фракционированием выделяют нитрометан (~ 10%) и нитропарафины С2-С3; исходный пропан возвращают в реактор. В лаборатории нитрометан получают по р-циям:
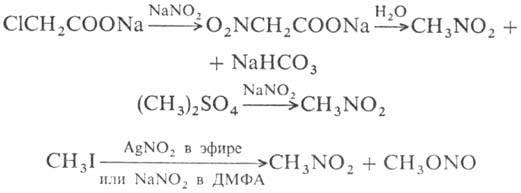
Нитрометан-р-ритель для эфироцеллюлозных лаков и смол, экстрагент ароматич. углеводородов из их смесей с парафинами, добавка к дизельным топливам, однокомпонентное ракетное топливо. В лаборатории нитрометан используют как р-ритель и полупродукт в синтезе разл. мононитро-, поли-нитросоед., а также соед. с др. функц. группами.
Для нитрометана т. воспл. 42-43 °С, т. самовоспл. 440 °С, ниж. КПВ 7,3%. При нагр. св. 100 °С под давлением, особенно в присут. окислителей, нитрометан взрывоопасен.
Нитрометан-сильный яд для центр. нервной системы. ПДК 30 мг/м3.
Произ-во нитрометана в США ок. 10 тыс. т/год.
Лит.: Лебедев Ю. А., Мирошниченко Е. А., Кнобель Ю. К., Термохимия нитросоединений, М., 1970, с. 29-32; Физер Л., Физер М., Реагенты для органического синтеза, т. 2, М., 1970, с. 459-62; Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 399-439. С. Л. Иоффе.
