Ингибиторы
ИНГИБИТОРЫ (от лат mhibeo - останавливаю, сдерживаю), в-ва, тормозящие хим. р-ции. Ингибирование характерно для каталитич и цепных р-ций, к-рые протекают с участием активных центров или активных частиц. Тормозящее действие обусловлено тем, что ингибитор блокирует активные центры катализатора или реагирует с активными частицами с образованием малоактивных радикалов, не способных продолжать цепь. Ингибитор вводится в систему в концентрации много меньшей, чем концентрации реагирующих в-в (10-2-10-5 моль%). Кинетика р-ций с участием ингибиторов принципиально различна для каталитических и цепных р-ций. В каталитич. р-ции число активных центров фиксировано и ингибитор, блокируя часть из них, не расходуется в ходе процесса. Поэтому при введении ингибитора скорость р-ции снижается, а затем процесс протекает длит. время с постоянной скоростью. В нек-рых случаях эта скорость может медленно возрастать из-за расходования ингибитора по к.-л. побочной р-ции. В цепной р-ции активные частицы непрерывно генерируются, что приводит к расходованию ингибитора и постепенному самоускорению р-ции (в случае цепной неразветвленной р-ции обычно восстанавливается исходная скорость).Ингибирование цепных реакций. Длительность t тормозящего действия ингибитора наз. периодом индукции; число цепей f, к-рые обрывает одна молекула ингибитора, последовательно вступая в р-ции обрыва, наз. стехиометрич. коэф. ингибирования. При исходной концентрации ингибитора [И]0 и скорости инициирования цепей vi период индукции равен: t = f [И]0/vi. Напр., хинон тормозит полимеризацию виниловых мономеров, вступая в след. р-ции:
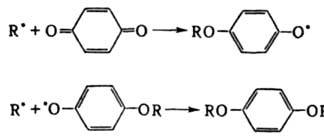
В этом случае f= 2 и t = 2[И]0/vi. В нек-рых системах происходит регенерация ингибитора в р-циях обрыва цепи, в результате чего одна молекула ингибитора и образующийся из нее радикал многократно участвуют в р-циях обрыва. Напр., при введении ионов меди в окисляющийся изопропиловый спирт цепи обрываются в результате протекания след. чередующихся р-ций:
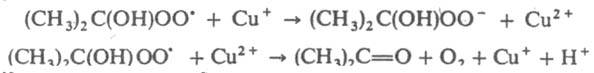
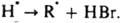 Образующийся НВr вызывает дополнит. обрыв цепей по р-циям:
Образующийся НВr вызывает дополнит. обрыв цепей по р-циям: 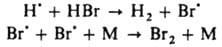
(М - любая третья частица). Для тушения горения применяют также огнегасящие порошки (напр.. NaHCO3, фосфорно-аммониевые соли), к-рые обладают комбинир. действием: снижают концентрацию радикалов из-за интенсивного обрыва цепей на пов-сти и вызывают повыш. теплоотвод (см. Горение). Различают слабые и сильные ингибиторы данной р-ции. Сильным считается такой ингибитор, к-рый, если его ввести в достаточно большой концентрации, сокращает длину цепи до единицы или уменьшает скорость р-ции в v0/vi раз, где v0 - исходная скорость р-ции. Слабый ингибитор, даже введенный в сравнительно высокой концентрации, снижает скорость р-ции от vi до нек-рого значения v > vi. Вызвано это тем, что из молекул слабого ингибитора образуются радикалы, способные продолжать цепь, в силу чего отношение v0/v уменьшается с увеличением [И]0, не достигнув значения v0/vi. Ингибитор, оказывающий сильное тормозящее действие в небольшой концентрации, наз. эффективным. Эффективность ингибитора характеризуют значением производной —dv/d[И]. Напр., окисление углеводорода RH в присут. инициатора, создающего скорость инициирования vi, определяется скоростью продолжения цепи с участием пероксильного радикала:
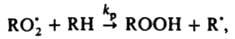
так что начальная скорость цепного окисления v = kp . [RH] [
 ]. В присут. ингибитора, напр., фенола, цепи обрываются по р-ции типа
]. В присут. ингибитора, напр., фенола, цепи обрываются по р-ции типа 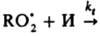 продукты. В квазистационарных условиях скорости инициирования и обрыва равны: vi = fkt[И][RO2], поэтому [
продукты. В квазистационарных условиях скорости инициирования и обрыва равны: vi = fkt[И][RO2], поэтому [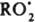 ] = vi/fkt [И] и v = kp[RH]vi/fkt [И]. Эффективность ингибирования характеризуется величиной отношения fkt/kp. Для ингибирования цепных разветвленных р-ций характерны критич. явления, сущность к-рых состоит в резком снижении скорости р-ции при очень незначит. увеличении концентрации ингибитора. Примером может служить ингибир. автоокисление углеводородов RH, в к-ром осн. источником радикалов является продукт окисления ROOH. При достаточно высокой т-ре или в присут. катализатора, интенсивно превращающего ROOH в радикалы, окисление RH может протекать в квазистационарном режиме, когда скорость образования ROOH практически равна скорости его расходования. Т.к. скорость образования ROOH зависит и от концентрации ингибитора, и от концентрации ROOH, существует нек-рая критич. концентрация ингибитора, при к-рой система переходит от нестационарного к квазистационарному режиму при очень незначительном (на 0,1-1%) изменении концентрации ингибитора. Это выражается в резком изменении скорости р-ции или периода индукции ингибитора. Два ингибитора, введенных в реагирующую систему, могут взаимно усилить ингибирующее действие друг друга (т. наз. синергизм ингибиторов) или ослабить его (антагонизм ингибиторов); нередко наблюдается и аддитивное действие двух ингибиторов. Если t1 и t2 - длительности тормозящего действия первого и второго ингибитора, введенных порознь, а t12 - длительность их совместного действия, то в случае синергизма t12 > (t1 + t2), в случае антагонизма t12 < (t1 + t2). На диаграмме t - концентрация ингибитора в случае синергизма наблюдается максимум. Синергизм ингибиторов может быть обусловлен либо разл. механизмами тормозящего действия ингибиторов (напр., при ингибир. окислении RH один ингибитор обрывает цепи, а другой разрушает ROOH), либо хим. взаимодействием между двумя ингибиторами или продуктами их превращения.
] = vi/fkt [И] и v = kp[RH]vi/fkt [И]. Эффективность ингибирования характеризуется величиной отношения fkt/kp. Для ингибирования цепных разветвленных р-ций характерны критич. явления, сущность к-рых состоит в резком снижении скорости р-ции при очень незначит. увеличении концентрации ингибитора. Примером может служить ингибир. автоокисление углеводородов RH, в к-ром осн. источником радикалов является продукт окисления ROOH. При достаточно высокой т-ре или в присут. катализатора, интенсивно превращающего ROOH в радикалы, окисление RH может протекать в квазистационарном режиме, когда скорость образования ROOH практически равна скорости его расходования. Т.к. скорость образования ROOH зависит и от концентрации ингибитора, и от концентрации ROOH, существует нек-рая критич. концентрация ингибитора, при к-рой система переходит от нестационарного к квазистационарному режиму при очень незначительном (на 0,1-1%) изменении концентрации ингибитора. Это выражается в резком изменении скорости р-ции или периода индукции ингибитора. Два ингибитора, введенных в реагирующую систему, могут взаимно усилить ингибирующее действие друг друга (т. наз. синергизм ингибиторов) или ослабить его (антагонизм ингибиторов); нередко наблюдается и аддитивное действие двух ингибиторов. Если t1 и t2 - длительности тормозящего действия первого и второго ингибитора, введенных порознь, а t12 - длительность их совместного действия, то в случае синергизма t12 > (t1 + t2), в случае антагонизма t12 < (t1 + t2). На диаграмме t - концентрация ингибитора в случае синергизма наблюдается максимум. Синергизм ингибиторов может быть обусловлен либо разл. механизмами тормозящего действия ингибиторов (напр., при ингибир. окислении RH один ингибитор обрывает цепи, а другой разрушает ROOH), либо хим. взаимодействием между двумя ингибиторами или продуктами их превращения. Ингибирование гетерогенно-каталитических реакций осуществляется в-вами, к-рые наз. ядами каталитическими. Торможение р-ции обусловлено снижением активности катализатора вследствие адсорбции ингибитора на его пов-сти.
Ингибирование ферментативных реакций м. б. обратимым и необратимым. В обоих случаях ингибитор способен к образованию комплекса с ферментом, но не м. б. подвергнут каталитич. превращению и препятствует образованию комплекса фермент - субстрат. Напр., бутанол ингибирует гидролиз сложных эфиров, катализированный карбоксипептидазой. Различают след. случаи обратимого ингибирования. Прямое конкурентное ингибирование, при к-ром молекулы ингибитора I и субстрата S конкурируют за присоединение к активному центру фермента Е. Процесс описывается соотношениями (Р - продукт превращения):
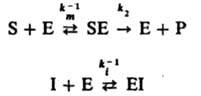
При таком механизме торможения, если [Е] << [S]0 и Е << [I]0, начальная скорость превращ. субстрата S равна:
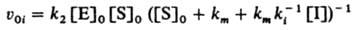
Неконкурентное ингибирование, при к-ром ингибитор присоединяется к активному ферменту или комплексу фермента с субстратом с образованием каталитически неактивной формы:
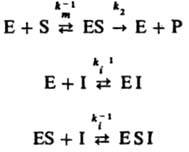
В этом случае начальная скорость р-ции равна:
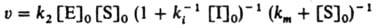
Внеконкурентное ингибирование, при к-ром ингибитор образует каталитически неактивный комплекс с субстратом:
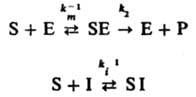
Начальная скорость р-ции равна:
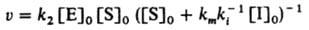
Отмечены случаи ингибирования фермента субстратом, когда неактивный комплекс с ферментом образует вторая молекула субстрата (субстратное ингибирование). Необратимо реагирующие ингибиторы реагируют с ферментом, дезактивируя его; в отличие от обратимого ингибирования активность фермента уменьшается во времени.
Применение. Ингибирование широко используется для регулирования скорости радикальной полимеризации, в частности при получении изделий большого объема. Ингибиторы окисления используют для стабилизации полиолефинов и каучуков при их переработке и в условиях эксплуатации (см. Деструкция полимеров), для стабилизации смазочных материалов и углеводородных топлив, сохранения пищ. жиров и лек. препаратов; в технологии получения мономеров они используются для предотвращения окислит. полимеризации. В исследовательских работах ингибиторы применяются для изучения механизма цепных р-ций, в частности определения скорости инициирования.
Литература
Ашмор П., Катализ и ингибирование химических реакций, пер. с англ., М., 1966; Уэбб Л., Ингибиторы ферментов и метаболизма, пер. с англ., М., 1966; Кулиев А. М., Химия и технология присадок к маслам и топливам, М., 1972; Денисов Е.Т., Ковалев Г. И., Окисление и стабилизация реактивных топлив, М., 1983. Е. Т. Денисов.
Ещё по теме
Ингибиторы ферментов — типы и механизмы действия
Ингибиторы химические — применение и виды
Механизмы активации и ингибирования ферментов — роль металлов в биохимии
Ингибиторы синтеза белка — механизмы действия и применение в медицине
Ингибиторы роста растений — виды и применение
Катализаторы и их роль в химических реакциях
Ингибиторы коррозии — защита материалов
Механизмы регуляции активности ферментов
Антиокислители — механизмы действия и применение
Яды каталитические — влияние на катализаторы и методы регенерации
Радикальные реакции в химии — механизмы и примеры
Регуляция активности ферментов
Неницеску реакция — механизмы и применение
