Хиноны
ХИНОНЫ, циклич. дикетоны, в молекулах к-рых кетогруппы входят в систему сопряженных двойных связей.
Наиб. практич. значение имеют бензохиноны, нафтохиноны, 9,10-антрахинон (см. Антрахинон), а также 1,2- и 1,4-антрахиноны (ф-лы I и II), 1,2-, 1,4- и 3,4-фенантрахиноны (ф-лы III-V, т. пл. 216, 153 и 133 °С, соотв.) и нек-рые дихиноны, напр. 1,4,5,8-нафтодихинон (VI).
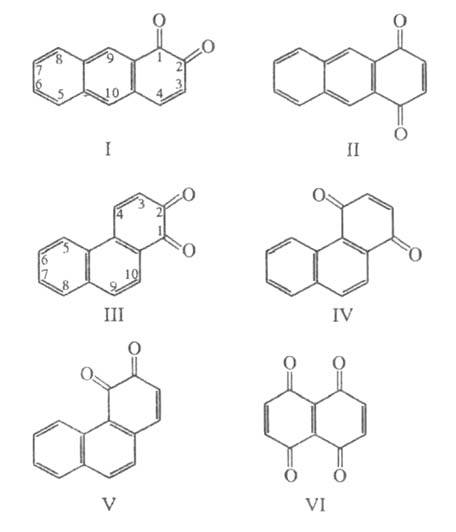
Хиноны- окрашенные кристаллы (табл.). Окраска хинонов во многом зависит от взаимного расположения карбонильных групп в молекуле: 1,2-хиноны окрашены, как правило, в красный или оранжево-красный цвет, 1,4-хиноны окрашены менее интенсивно - в желтый или светло-желтый цвет. 1,4-Хиноны обладают большей летучестью и более резким запахом, чем 1,2-хиноны.
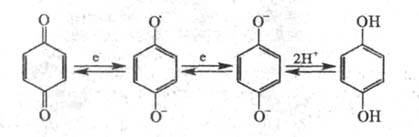
Хиноны весьма склонны к переходу в ароматич. соед.; присоединение одного электрона приводит к образованию сёмихиненового анион-радикала, к-рый при присоединении еще одного электрона дает дианион, в кислой среде превращающийся в двухатомный фенол, напр. в случае 1,4-бензохинона:
СВОЙСТВА НЕКОТОРЫХ ХИНОНОВ
| Соединение | Цвет | Т. пл., oС | Окислит. -восстановит. потенциал, В (CH3OH, 25 °С)* |
| 1,2-Бензохинон | Ярко-красный | 60-70 | 0,795 (H2O) |
| 1,4-Бензохинон | Светло-желтый | 116 | 0,711(C6H6) |
| Тетраметил- 1 ,4-бензо-хинон (дурохинон) | Желтый | 111-112 | 0,466 |
| Тетрахлор-1,4-бензохинон | Желтый | 290 | 0,742 (C6H6) |
| 1,2-Нафтохинон | Красный | 145-147 | 0,576 |
| 1,4-Нафтохинон | Желтый | 128,5 | 0,484 |
| 1,2-Антрахинон | Красный | 185-190 | 0,490 |
| 1,4-Антрахинон | Желтый | 218 | 0,401 |
| 9,10-Антрахинон | Желтый | 287 | 0,154 |
| 9,10-Фенантрахинон | Желтый | 206-208 | 0,460 |
| 1,4,5,8-Нафтодихинон | Желтый | 220 | 0,972 (H2O) |
*B скобках указан растворитель, отличный от СН3ОН.
Склонность хинонов к участию в окислит.-восстановит, р-циях характеризуется окислит.-восстановит, потенциалом. В общем случае 1,2-хиноны имеют более высокие потенциалы, чем 1,4-хиноны. Электроноакцепторные группы в молекуле хинонов обычно повышают его окислит.-восстановит. способность, электронодонорные - понижают.
По хим. св-вам хинонов аналогичны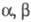 -ненасыщенным кетонам. Под действием мягких восстановителей хиноны легко превращаются в гидрохиноны, причем легче всего восстанавливаются бензохиноны, труднее - 9,10-антрахинон. Хиноны легко образуют комплексы с донорами электронов, напр. 1,4-бензохинон с гидрохиноном дает черно-зеленый кристаллич. комплекс хингидрона, с пиреном (1:1) в петролейном эфире - красный кристаллич. комплекс.
-ненасыщенным кетонам. Под действием мягких восстановителей хиноны легко превращаются в гидрохиноны, причем легче всего восстанавливаются бензохиноны, труднее - 9,10-антрахинон. Хиноны легко образуют комплексы с донорами электронов, напр. 1,4-бензохинон с гидрохиноном дает черно-зеленый кристаллич. комплекс хингидрона, с пиреном (1:1) в петролейном эфире - красный кристаллич. комплекс.
Для хинонов характерны р-ции присоединения, напр.:
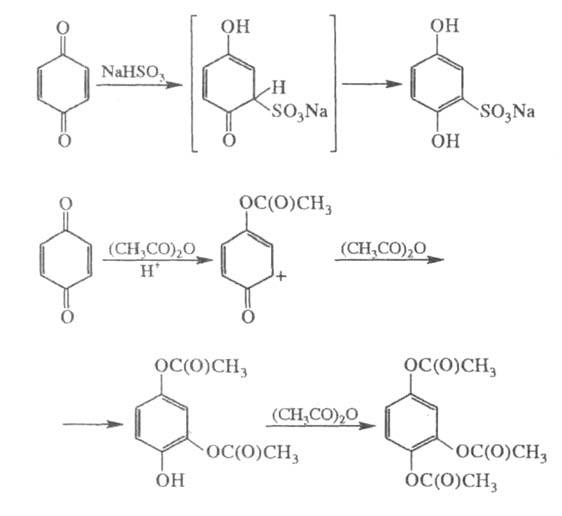
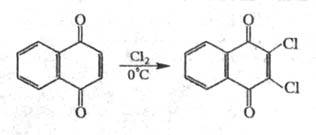
Взаимод. с С12 при низкой т-ре протекает с сохранением хиноидной структуры, напр.:
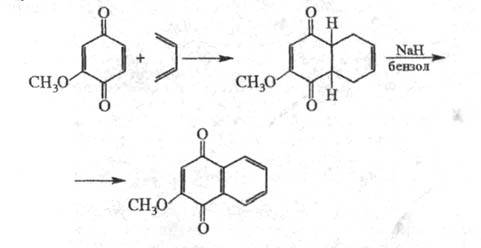
Хиноны легко вступают в диеновый синтез, причем 1,2-хиноны могут выступать как диены и диенофилы, а 1,4-хиноны- как диенофилы, напр.:
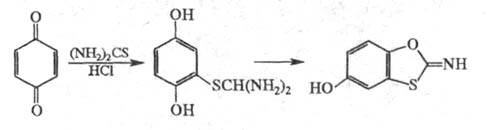
С тиомочевиной в НС1 хиноны дают продукты, способные к дальнейшей циклизации с образованием гетероциклов, напр.:
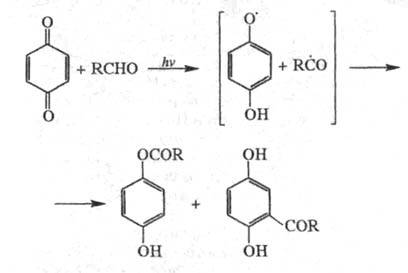
Облучение хинонов УФ светом в присут. альдегидов приводит к продуктам С- и О-ацилирования, напр.:
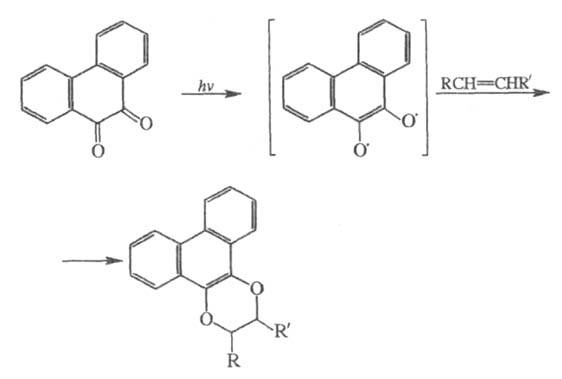
В условиях фотохим. р-ций хиноны могут присоединять по кетогруппе олефины, напр.:
Получают хиноны, как правило, окислением соответствующих фенолов, аминов или диаминов действием AgCO3, соли Фреми (KO3S)2NO, (C6H5SeO)2O (гл.обр. для синтеза 1,2-хинонов), хромовой к-ты и др. окислителей.
Хиноны- структурные фрагменты прир. в-в (напр., витаминов K1 и К3, см. Витамин К), антрахиноновых красителей, фталоилкарбазолов, орг. пигментов (см. Пигменты): 1,4-бензохинон - окислитель в фотографии, дубящее ср-во при крашении. Нек-рые хиноны и их производные - катализаторы в произ-ве синтетич. каучука и полиакрилатов (1,4-нафтохинон), окислит. дегидрирования (полинафтохинон) и окислит.-восстановит. процессов (алкилантрахиноны); полупродукты в синтезе полициклических кубовых красителей (2,3-дихлор-1,4-нафтохинон), бензантрона (9,10-антрахинон).
Лит.: Кэсон Д., в сб.: Органические реакции, пер. с англ., сб. 4, М., 1951, с. 270-336; Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов, Л., 1980; Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 830-47. См. также лит. при ст. Антрахиноновые красители.
Г. И. Пуца.
