1,4-бензохинон
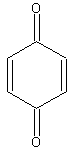
Синонимы:
2,5-циклогексадиен-1,4-дионпара-бензохинон
пара-хинон
хинон
Внешний вид:
желт. моноклинные кристаллы (растворитель перекристаллизации - вода)Брутто-формула (система Хилла): C6H4O2
Молекулярная масса (в а.е.м.): 108,1
Температура плавления (в °C): 115,7
Растворимость (в г/100 г или характеристика):
вода: 0,7 (5°C)вода: 1,5 (30°C)
вода: растворим (100°C)
вода: мало растворим
диэтиловый эфир: растворим
лигроин: растворим (100°C)
петролейный эфир: мало растворим
этанол: растворим
Вкус, запах, гигроскопичность:
запах: резкийМетод получения 1.
(лабораторный синтез)Источник информации: Гаттерман Л., Виланд Г. "Практические работы по органической химии" 5-е изд., М.-Л.: ГНТИХЛ, 1948 стр. 348-349
К раствору 23 г (0,25 моля) анилина в смеси 100 мл чистой концентрированной серной кислоты и 500 мл воды, находящемуся в толстостенном стакане, постепенно приливают из капельной воронки (прн охлаждении снаружи льдом, и перемешивании) раствор 30 г бихромата натрия в 75 мл воды. Температура при этом не должна подниматься выше 10°. Реакционную смесь оставляют стоять в течение ночи в холодном месте, а на следующее утро таким же способом к ней приливают по каплям раствор 40 г бихромата натрия в 120 мл воды. Снова оставляют стоять в течение 6 час, после чего раствор (окрашенный в темнокоричневый цвет) фильтруют на большой воронке Бюхнера и промывают осадок на фильтре небольшим количеством воды. Фильтрат 2 раза экстрагируют эфиром (применяя каждый раз по 0,5 л последнего).
Эфир отгоняют из перегонной колбы (из которой затем производят перегонку хинона с водяным паром); отогнанным эфиром (разделив его на две порции) снова извлекают хинон из уже обработанного фильтрата и снова отгоняют его из той же перегонной колбы.
К сырому хинону, оставшемуся в колбе после отгонки эфира, присоединяют остаток на фильтре (вместе с фильтром) и отгоняют хинон с водяным паром.
Хинон выделяется из погона в виде красивых золотистожелтых кристаллов; его сушат сначала между листами фильтровальной бумаги, а затем в обыкновенном эксикаторе над хлористым кальцием.
Температура плавления чистого хинона 116°.
Выход 14—16 г.
Хинон легко возгоняется; пары его имеют едкий запах и вызывают слезоточение. Ввиду большой летучести хинон нельзя долгое время оставлять на воздухе.
Для перекристаллизации хинона можно применять спирт или петролейный эфир. Чистый сухой препарат сохраняется без разложения длительное время.
Метод получения 2.
(лабораторный синтез)Источник информации: Гаттерман Л., Виланд Г. "Практические работы по органической химии" 5-е изд., М.-Л.: ГНТИХЛ, 1948 стр. 349
Растворяют (при нагревании до 50°) 10 г гидрохинона в 200 мл воды; раствор охлаждают до 20°, затем медленно приливают к нему 10 г концентрированной серной кислоты и снова охлаждают до 20°. Перемешивая и охлаждая (температура не выше 30°), прибавляют раствор 28 г бихромата натрия в 13 мл воды до тех пор, пока окраска осадка (хингидрон) из темно-зеленой не перейдет в желтовато-зеленую. После этого реакционную смесь охлаждают до 10°, отсасывают кристаллы иа воронке Бюхнера и промывают их небольшим количеством холодной воды. Фильтрат 3 раза извлекают бензолом, беря каждый раз по 20 мл.
Соединенные бензольные вытяжки переносят в коническую колбу, прибавляют хинон, ранее собранный на фильтре, и нагревают при перемешивании на водяной бане до полного растворения хинона. Бензольный раствор сушат еще в горячем состоянии небольшим количеством хлористого кальция и через короткое время фильтруют.
Бензол отгоняют до тех пор, пока не начнется перегонка хинона. При охлаждении остатка в перегонной колбе хиной выкристаллизовывается. Бензол нужно отгонять медленно во избежание уменьшения выхода хинона (унос с парами бензола).
Выход 8—9 г (80—90% от теоретического).
Перегонка хинона с водяным паром всегда сопровождается его заметным разложением.
Метод получения 3.
(лабораторный синтез)Источник информации: Храмкина М.Н. "Практикум по органическому синтезу" Л.: Химия, 1977 стр. 200-201
В круглодонную колбу вносят 10 г гидрохинона и 100 мл воды, нагретой до 50 °С. После растворения гидрохинона раствор охлаждают до 20 °С и медленно, небольшими порциями прибавляют 5 мл серной кислоты, выполняющей роль катализатора.
В случае применения не совсем чистого гидрохинона сразу же после внесения серной кислоты образуется черный клейкий осадок. Для освобождения от этого осадка жидкость фильтруют череа складчатый фильтр еще до внесения окислителя, в данном случае бромноватокислого калия
В реакционную смесь осторожно вносят 5,5 г бромноватокислого калия, нагревая колбу на водяной бане до 60°С. Сразу же начинается реакция с образованием зеленовато-черного осадка — хингидрона.
Подогревание прекращают, так как температура самопроизвольно повышается до 75°С. Реакция окисления считается законченной, как только черный цвет реакционной массы изменится до ярко-желтого цвета бензохинона. Реакционную смесь нагревают при 80 °С до полного растворения бензохинона, затем охлаждают до 0°С. Выпавший пара-бензохинон отфильтровывают на воронке Бюхнера, промывают небольшим количеством ледяной воды и сушат.
Выход п-бензохинона (т. пл. 116 °С) около 8 г.
Плотность:
1,318 (20°C, г/см3)Диэлектрическая проницаемость:
3,12 (17°C)Стандартная энтропия образования S (298 К, Дж/моль·K):
-187,5 (т)Энтальпия плавления ΔHпл (кДж/моль):
20,95Энтальпия кипения ΔHкип (кДж/моль):
47,76Дополнительная информация:
Летуч с водяным паром.
Легко и обратимо восстанавливается водородом (катализатор диоксид платины), диоксидом серы, гидразином - до гидрохинона (через анион-радикал - семихинон). Образует прочные комплексы с переносом заряда с бензолом, толуолом, нафталином, антраценом, гидрохиноном (хингидрон) - в соотношении 1:1, с фенолом - в соотношении 1:1 и 1:2 (фенохинон). Действием порошка цинка в уксусном ангидриде превращается в диацетоксибензол.
С первичными аминами образует замещенные монохинонимины, с гидроксиламином - п-хинонмоноокисм (таутомер п-нитрозофенола) и п-хинондиоксим. При взаимодействии с реактивами Гриньяра превращается в хинолы, перегруппировывающиеся в алкилгидрохиноны.
Подобно ненасыщенным кетонам способен к присоединению по кратным связям. Продукты присоединения окисляются избытком исходного хинона, если их окислительно-восстановительный потенциал ниже, чем у хинона. С метанолом образует 2,5-диметокси-1,4-бензохинон (катализатор хлорид цинка), с анилином - 2,5-дианилино-1,4-бензохинон. С тиомочевиной в соляной кислоте образует 2-(1,1-диаминометилтио)-1,4-бензохинон, который превращается либо в 2-оксо-5-гидрокси-1,3-бензоксатиолан или, избытком бензохинона - в 2-амино-6-гидрокси-1,3-бензтиазол. Специфической реакцией для хинонов является ацетоксилирование по Тиле-Винтеру, где из бензохинона под действием уксусного ангидрида образуется 1,2,4-триацетоксибензол.
В реакции Дильса-Альдера выступает как диенофил.
Реагирует с фенилдиазонийхлоридом давая 2-фенил-1,4-бензохинон.
С перекисью водорода в щелочной среде образует эпоксигидрохинон, превращающийся в кислой среде в гидроксихинон. Устойчив к действию окислителей.
Облучение 1,4-бензохинона в растворе дает с низким выходом димер. Облучение 1,4-бензохинона в присутствии альдегидов приводит с умеренными выходами или к моноэирам гидрохинона (ароматические альдегиды, альфа, бета-ненасыщенные альдегиды) или к к 2-ацилгидрохинону (алифатические и ароматические альдегиды).
- "Общая органическая химия" т.2 под ред. Бартона Д. и Оллиса В.Д., М.: Химия, 1982 стр. 840-846
- "Химическая энциклопедия" т.1 М.: Советская энциклопедия, 1988 стр. 278-279
- Рабинович В.А., Хавин З.Я. "Краткий химический справочник" Л.: Химия, 1977 стр. 131
