Бензол
БЕНЗОЛ, мол. м. 78,11; бесцв. жидкость с характерным запахом; у. пл. 5,53°С, т. кип. 80,1°С; d420 0,879, nD20 1,5011; 0,6468 мПа*с (20 С);
0,6468 мПа*с (20 С);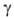 28,18 мН/м (25°С);
28,18 мН/м (25°С);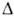 Hoпл 9,843 кДж/моль,
Hoпл 9,843 кДж/моль,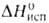 30,77 кДж/моль,
30,77 кДж/моль,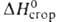 - 3303,72 кДж/моль,
- 3303,72 кДж/моль,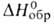 - 82,98 кДж/моль; Sо298 269,38 Дж/(моль*К); ркрит 4,91 МПа, tкрит 289,5 °С;
- 82,98 кДж/моль; Sо298 269,38 Дж/(моль*К); ркрит 4,91 МПа, tкрит 289,5 °С;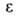 2,284 (20°С). Р-римость в воде 0,073% по массе (25 °С), воды в бензоле-0,05% (26 °С). Неограниченно раств. в углеводородах, эфирах, хуже - в метаноле, не раств. в этиленгликоле, глицерине; растворяет жиры, каучуки, гудрон, серу, фосфор, иод. Образует азеотропные смеси (см. табл.).
2,284 (20°С). Р-римость в воде 0,073% по массе (25 °С), воды в бензоле-0,05% (26 °С). Неограниченно раств. в углеводородах, эфирах, хуже - в метаноле, не раств. в этиленгликоле, глицерине; растворяет жиры, каучуки, гудрон, серу, фосфор, иод. Образует азеотропные смеси (см. табл.).

ХАРАКТЕРИСТИКА АЗЕОТРОПНЫХ СМЕСЕЙ БЕНЗОЛА
| Второй компонент смеси | Т. кип., °С | Содержание бензола, % по массе |
| Вода | 69,8 | 91,0 |
| Муравьиная к-та | 71,0 | 67,0 |
| Метанол | 58,0 | 62,0 |
| Этанол | 67,93 | 67,5 |
| Пропанол | 77,1 | 83,1 |
| Изопропанол | 71,9 | 66,2 |
Молекула бензола - плоский правильный шестиугольник с внутр. углами 120° и расстоянием между атомами углерода 0,139 нм. В УФ-спектре в этаноле максимумы при 184 нм (lg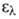 4,77), 203,5 нм (lg
4,77), 203,5 нм (lg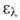 3,87), 254,5 нм (lg
3,87), 254,5 нм (lg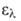 2,31).
2,31).
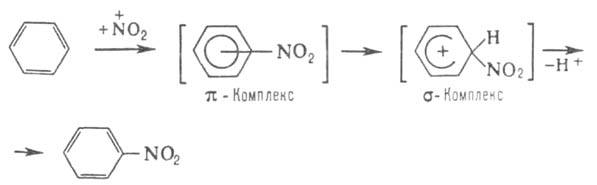
Бензол - родоначальник углеводородов ароматич. ряда. Хим. св-ва определяются наличием в молекуле стабильной замкнутой системы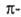 электронов (см. Ароматичность, Ароматические соединения). Он склонен к донорно-акцепторному взаимод. с соед., имеющими дефицит электронов; в результате образуются малостабильные и существующие только в р-рах
электронов (см. Ароматичность, Ароматические соединения). Он склонен к донорно-акцепторному взаимод. с соед., имеющими дефицит электронов; в результате образуются малостабильные и существующие только в р-рах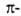 комплексы, к-рые могут превращ. в более прочные
комплексы, к-рые могут превращ. в более прочные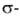 комплексы.
комплексы.
Катализаторы электроф. замещения - обычно к-ты Льюиса, облегчающие образование промежут. комплексов и ускоряющие основную р-цию, напр. хлорирование: 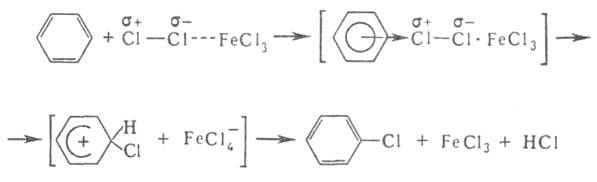
Бензол сульфируется до бензолсульфокислот, алкилируется олефинами с образованием алкилбензолов. В зависимости от природы первого введенного заместителя дальнейшее электроф. замещение направляется преим. в орто- и пара-положения или в мета-положение.
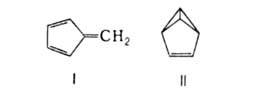
Для бензола характерна устойчивость к действию высоких т-р и окислителей. Лишь выше 650°С он частично превращ. в дифенил, выше 750°С разлагается на углерод и водород. Бензол не изменяется под действием Н2СrO4 и КМnО4, с О2 в присут. катализаторов (V, Мо) при 350^450°С образует малеиновый ангидрид. Гидрируется до циклогексана в присут. разл. катализаторов (напр., в присут. Ni при 120-200°С и 2,96-6,94 МПа). Щелочными металлами в жидком NH3 восстанавливается до 1,4-циклогексадиена. При фотохим. присоединении хлора превращ. в гексахлорциклогексан. При УФ-облучении способен к циклоприсоединению и изомеризации в фульвен (ф-ла I) и бензвален (II).
Наиб. старый метод пром. получения бензола: выделение его из предварительно охлажденных пирогазовых продуктов коксования каменных углей абсорбцией орг. поглотителями, напр. маслами кам.-уг. и нефтяного происхождения; для отделения поглотителя используют перегонку с водяным паром. От примесей (напр., тиофена) сырой бензол отделяют гидроочисткой. Осн. кол-во бензола получают риформингом (470-550°С) нефтяной фракции, выкипающей при 62-85 °С; извлекают экстракцией. Бензол высокой чистоты получают экстрактивной перегонкой с ДМФА. Бензол выделяют также из жидких продуктов пиролиза нефтепродуктов, образующихся в произ-ве этилена и пропилена. При избытке ресурсов толуола бензол производят деалкилированием последнего, к-рое проводят термич. способом при 600-820°С в присут Н2 и водяного пара или каталитически при 227-627°С в присут. цеолитов или оксидных катализаторов. наиб. экономически выгодно выделение бензола из продуктов пиролиза, но ресурсы этого источника недостаточны, поэтому б.ч. его производят риформингом. Доля коксохим. бензола в общем балансе невелика. В лабораториях особо чистый бензол синтезируют декарбоксилированием бензойной к-ты.
Специфич. р-ция обнаружения бензола в присут. гомологов: встряхивают смесь углеводородов с аммиачным р-ром Ni(CN)2; при наличии бензола выпадает осадок комплексного соед. Ni(CN)2NH3(C6H6).
Осн. области применения бензола (более 80%): произ-во этилбензола, кумола и циклогексана; остальное кол-во - для получения анилина, малеинового ангидрида, как компонент моторного топлива для повышения октанового числа, как р-ритель и экстрагент в произ-ве лаков, красок, ПАВ и др.
Для бензола т. всп. - 11 °С, т. самовоспл. 534°С, КПВ 1,5-8%. Сильно раздражает кожу; в высоких концентрациях бензол оказывает судорожное действие; при многократных воздействиях низких концентраций наблюдаются изменения в крови и кроветворных органах; ПДК 5 мг/м3.
Транспортируют в железнодорожных цистернах, снабженных оборудованием для разогрева продукта. Бензол открыт М. Фарадеем в 1825 при пиролизе китового жира; впервые синтезирован Э. Мичерлихом в 1833 декарбоксилированием бензойной к-ты.
Литература
Соколов В. 3., Харлампович Г. Д., Производство и использование ароматических углеводородов, М., 1980; Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов, Л., 1980; Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 314-455. Н.Н. Артамонова.
