Ацилирование
АЦИЛИРОВАНИЕ, введение ацильной группы (ацила) RCO в молекулу орг. соед. путем замещения атома Н. В широком смысле ацилированием называют замещение любого атома или группы атомов на ацильную группу. В зависимости от того, к какому атому присоединяется ацил, различают N-ацилирование, O-ацилирование, S-ацилирование и С-ацилирование. Р-ция, при к-рой вводится формильная группа (НСО), наз. формилированием, ацетильная (СН3СО) - ацетилированием, бензоильная (С6Н5СО)-бензоилированием.
Наиб. распространенные ацилирующие агенты - хлорангидриды карбоновых к-т. Они легко ацилируют амины и их соли. Процесс проводят в воде, инертных р-рителях, пиридине (метод Айнхорна). В последнем случае хлорангидрид не добавляется к реакц. смеси, а получается непосредственно в ходе р-ции из карбоновой к-ты и тионилхлорида: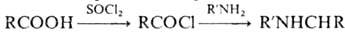 . Ацилирование спиртов и тиолов в пиридине проводят на холоду, фенолов -при нагревании. Ароматич., алициклич., ненасыщ. углеводороды, гетероциклы реагируют с хлорангидридом в присут. к-т Льюиса с образованием кетонов, напр.: RCH=CH2 + R'COCl -> RCH=CHCOR'. Бензоилирова-ние аминов, спиртов и тиолов ведут по Шоттену- Бауману в водно-щелочной среде (10%-ный р-р NaOH, р-ры NaHCO3, Na2CO3), напр.:
. Ацилирование спиртов и тиолов в пиридине проводят на холоду, фенолов -при нагревании. Ароматич., алициклич., ненасыщ. углеводороды, гетероциклы реагируют с хлорангидридом в присут. к-т Льюиса с образованием кетонов, напр.: RCH=CH2 + R'COCl -> RCH=CHCOR'. Бензоилирова-ние аминов, спиртов и тиолов ведут по Шоттену- Бауману в водно-щелочной среде (10%-ный р-р NaOH, р-ры NaHCO3, Na2CO3), напр.:
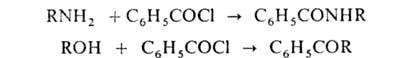
Ангидриды карбоновых к-т (чаще всего используют уксусный ангидрид) легко ацилируют амины в среде уксусной к-ты, эфире, бензоле, избытке уксусного ангидрида, ре-же-в пиридине: (RCO)2O + NHR2' -> RCONR2' + RCOOH. Ацилирование спиртов протекает труднее и облегчается при добавлении ангидрида трифторуксусной к-ты вследствие образования сильного ацилирующего агента - смешанного ангидрида CF3COOCOR; для ускорения р-ции используют также смешанные ангидриды кремниевой и карбоновой к-т, напр. (CH3COO)4Si. С-ацилирование ангидридами проводят по Фриделю — Крафтсу.
Карбоновые к-ты применяют преим. для ацилирования аминов. Первичные и вторичные амины ацилируются при сухой перегонке аммониевых солей карбоновых к-т или их нагревании в высококипящем р-рителе (нитробензоле, ксилоле) с удалением выделяющейся воды: RCOOH*HNR'2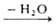 RCONR'2. В случае ароматич. аминов р-ция ускоряется в присут. А1С13, РС13, H2SO4. К-ты ацилируют амины практически количественно в присут. карбодиимидов, напр. N,N'-дициклогексилкарбодиимида (р-ция 1) или карбонилдиимидазола (р-ция 2), когда процесс идет через промежут. образование имидазолида к-ты:
RCONR'2. В случае ароматич. аминов р-ция ускоряется в присут. А1С13, РС13, H2SO4. К-ты ацилируют амины практически количественно в присут. карбодиимидов, напр. N,N'-дициклогексилкарбодиимида (р-ция 1) или карбонилдиимидазола (р-ция 2), когда процесс идет через промежут. образование имидазолида к-ты:
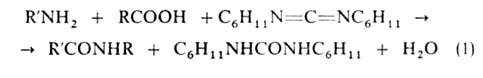
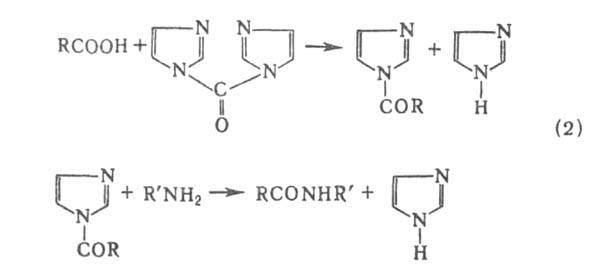
Формилирование аминов происходит при их кипячении с муравьиной к-той или формамидом, напр.: RNH2 + НСООН -> RNHCHO + Н2О
Ацилирование аминов кетенами идет по р-ции: RNH2 + СН2=С=О -> RNHCOCH3.
Каталитич. действие при ацилировании разл. классов соед. оказывают производные 4-аминопиридина. Так, бензоилирование м-хлоранилина ускоряется в 106 раз при добавлении 4-диметиламинопиридина.
Лит.: В е и г а н д К., Хильгетаг Г., Методы эксперимента в органической химии, пер. с нем., М., 1968; Гауптман 1, Грефе Ю., Ремане X., Органическая химия, пер. с нем., М., 1979; Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 115-19. Г. В. Гришина.
