Амины
Аминами называются соединения, которые могут быть произведены от аммиака замещением в нем атомов водорода на углеводородные радикалы.
В молекуле аммиака можно заместить на радикалы один, два или три атома водорода и таким образом получить амины следующих трех типов:
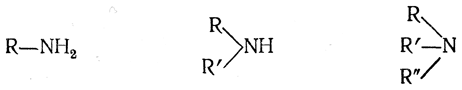
Эти типы аминов по числу атомов водорода, замещенных радикалами, называются первичными, вторичными и третичными аминами. Амины относят к соответствующему типу независимо от того, какие радикалы R (первичные, вторичные или третичные) входят в их состав. Следовательно, применительно к аминам терминам первичный, вторичный и третичный придается другое значение, чем в названиях радикалов.
Названия аминов обыкновенно производят от названий входящих в них радикалов с присоединением слова амин. Таким образом возникают названия: метиламин СН3—NH2, диметиламин (CH3)2NH, триметиламин (CH3)3N, пропиламин
СН3—СН2—СН2—NH2, втор-бутиламин
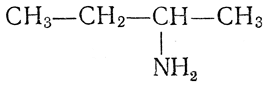
трет-бутиламин (СН3)3С—NH2 и т. д.
Изомерия аминов происходит как от изомерии радикалов (собственно изомерия), так и от того, что в молекуле амина может быть несколько различных радикалов (метамерия). Так, например, диметиламин (CH3)2NH изомерен (метамерен) этиламину СН3—СН2— NH2.
Аммиак, соединяясь с кислотами, образует соли аммония. Они не являются соединениями пятивалентного азота, как это полагали ранее. Реакцию образования солей аммония следует представлять себе таким образом: ион водорода (протон) присоединяется к атому азота, обладающему свободной парой электронов, причем образуется ковалентная связь между азотом и водородом. Атом азота приобретает положительный заряд, и вновь возникающее образование становится катионом, который связывается с анионом хлора ионной связью:
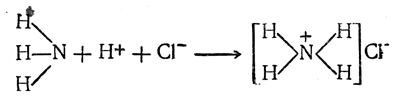
В солях аммония можно последовательно заместить от одного до четырех атомов водорода на углеводородные радикалы и получить таким образом соли органических замещенных аммониевых оснований, например:

Последняя соль называется хлористым тетраметиламмонием.
Действием натрийбензила на хлористый тетраметиламмоний удалось получить твердое вещество, в котором, казалось бы, у атома азота находятся пять углеводородных радикалов:
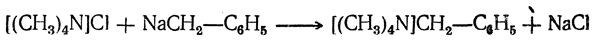
Однако все свойства этого вещества, начиная от глубокой окраски, доказывают, что этот продукт является аналогом исходного натрийбензила и что группировка [(CH3)4N) играет в нем роль металла. Растворы этого вещества проводят электрический ток, и при электролизе радикал бензил ведет себя как анион. Таким образом, азот и бензильный радикал связаны между собой не ковалентной, а ионной связью.


