Свойства
. Крахмал имеет вид белого аморфного порошка («картофельная мука»). Высушенный при 100—110° С крахмал очень гигроскопичен. При настаивании с водой (в определенных температурных интервалах, отличающихся для различных крахмалов) происходит клейстеризация крахмала, внешне выражающаяся в сильном набухании крахмальных зерен, их разрыве и образовании более или менее однородного раствора — крахмального клейстера. Растворы крахмала вращают плоскость поляризации вправо: [α]D=+201,5—205°.
Широко известна очень чувствительная цветная реакция крахмала с иодом. Характерно, что возникающее интенсивное синее окрашивание крахмала с иодом исчезает при кипячении раствора и вновь появляется при охлаждении. Крахмал не обнаруживает восстанавливающей способности при действии обычных реактивов в обычных условиях проведения реакций. Он не восстанавливает ни гидроокись меди, ни фелингову жидкость. Более чувствительные окисляющие реактивы дают возможность обнаружить в крахмале ничтожное количество свободных альдегидных групп: одну на сотни глюкозных остатков. Этим путем в последние годы стали определять молекулярные веса полисахаридов крахмала.
Методами метилирования и ацетилирования можно обнаружить в крахмале в среднем три свободные гидроксильные группы на каждый остаток глюкозы; так, например, можно получить «триметилкрахмал» и «триацетилкрахмал».
При быстром нагревании обычного крахмала, содержащего 10—20% воды, происходит расщепление гигантской молекулы крахмала на более мелкие молекулы — полисахариды того же состава, что и крахмал (C6H10O5)х, носящие название декстринов. Еще быстрее «декстринизация» протекает в присутствии кислот. По мере убывания величины молекулы декстрины дают с иодом окрашивание в сине-фиолетовый, красно-фиолетовый, красно-оранжевый, оранжевый и желтый цвет. Весь этот ряд декстринов можно легко получить при ферментативном расщеплении крахмала при помощи фермента слюны — птиалина, действуя им на крахмал в течение различных промежутков времени. Слабо декстринизованный крахмал, все еще окрашивающийся иодом в синий цвет, но лучше растворимый в воде, чем обычный крахмал, называется растворимым крахмалом.
Как при ферментативном, так и при достаточно продолжительном кислотном расщеплении крахмала гидролиз обычно не заканчивается образованием декстринов, хотя есть ферменты, которые расщепляют крахмал только до остаточных декстринов. Обычно ферменты пищеварительных соков при температуре около 40° С гидролизуют крахмал до глюкозы; так же действуют и минеральные кислоты при длительном кипячении
Схема постепенного гидролиза крахмала кислотным или ферментативным способом (действием карбогидраз) такова:
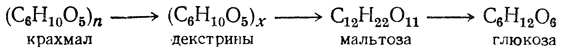
Карбогидразы, расщепляющие молекулы высших полиоз типа крахмала, носят общее название амилаз (от amylum — лат. крахмал). Наиболее известны два типа амилаз, обозначаемых буквами αиβ. В животном организме присутствуют лишь α-амилазы, в растениях — как α-, так и β-амилазы.
α-Амилазы расщепляют главным образом каждую пятую или шестую α-гликозидную связь цепи полиозы, причем места ветвлений не являются препятствием их действию (рис. 42).
Под действием α-амилазы молекула полиозы сначала очень быстро расщепляется на сравнительно высокомолекулярные декстрины, которые далее расщепляются до мальтозы. Небольшие количества мальтозы образуются наряду с декстринами уже с самого начала расщепления.
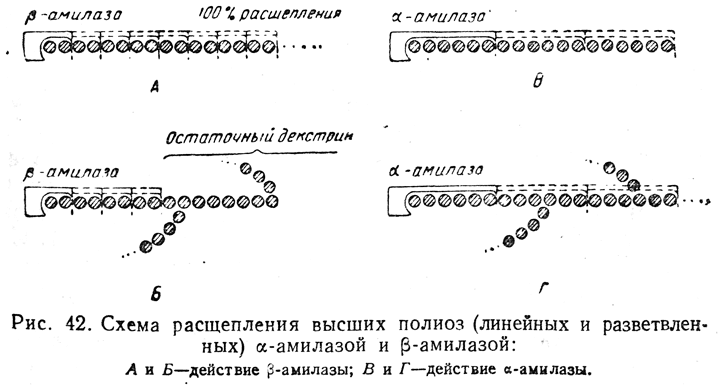
β-Амилазы расщепляют каждую вторую α-гликозидную связь, начиная от конца цепи, отщепляя по два глюкозных остатка в виде молекул мальтозы, причем места ветвлений цепи служат препятствием их действию (вблизи мест ветвлений расщепление останавливается). Таким образом, если цепь полиозы разветвлена, после действия р-амилазы образуются «остаточные декстрины».
Образующаяся при α- и β-амилолизе мальтоза далее расщепляется при действии фермента мальтозы.
В последние годы преимущественно из микроорганизмов получены γ-амилазы, последовательно отщепляющие от периферических концов полиглюкозидных цепей по одному остатку глюкозы.


