Диацетилен
ДИАЦЕТИЛЕН (1,3-бутандиин) , мол. м. 50,06; т. пл. - 36,4°С, т. кип. 10,3 °С; d40 0,736; nD20 1,4386:
, мол. м. 50,06; т. пл. - 36,4°С, т. кип. 10,3 °С; d40 0,736; nD20 1,4386: 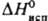 22,6 кДж/моль,
22,6 кДж/моль, 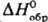 - 472,8 кДж/моль; Сp0 73,69 Дж/(моль.К);
- 472,8 кДж/моль; Сp0 73,69 Дж/(моль.К); 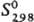 250,2 ДжДмоль.К); раств. в орг. р-рителях, воде (в 1 объеме 4,6 объема диацетилена). По хим. св-вам диацетилен близок ацетилену, однако значительно более взрывоопасен. Устойчив ниже 0°С, при комнатной т-ре самопроизвольно полимеризуется. При взаимод. с аммиачными р-рами солей Cu(I) образует легко взрывающиеся ацетилениды
250,2 ДжДмоль.К); раств. в орг. р-рителях, воде (в 1 объеме 4,6 объема диацетилена). По хим. св-вам диацетилен близок ацетилену, однако значительно более взрывоопасен. Устойчив ниже 0°С, при комнатной т-ре самопроизвольно полимеризуется. При взаимод. с аммиачными р-рами солей Cu(I) образует легко взрывающиеся ацетилениды 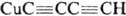 и
и 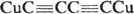 . Метиновые атомы Н в молекуле диацетилена могут замещаться: а) оба одновременно, напр., при получении реактива Иоцича
. Метиновые атомы Н в молекуле диацетилена могут замещаться: а) оба одновременно, напр., при получении реактива Иоцича 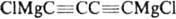 ; б) только один, как в р-ции Манниха:
; б) только один, как в р-ции Манниха: 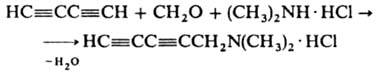
При взаимод. с ацетоном диацетилен превращается в "дииндиол"
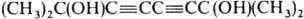 - реактив, используемый во мн. орг. синтезах (аналогично реактиву Гриньяра). Присоединение по тройным связям диацетилена происходит последовательно. При его гидрировании можно получить дивинил, при хлорировании - гексахлор-2-бутен, при взаимод. со спиртами -
- реактив, используемый во мн. орг. синтезах (аналогично реактиву Гриньяра). Присоединение по тройным связям диацетилена происходит последовательно. При его гидрировании можно получить дивинил, при хлорировании - гексахлор-2-бутен, при взаимод. со спиртами - 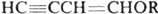 и
и 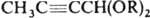 , при р-ции с Н2О - диацетил, при взаимод. с алкиламинами или тиолами - соответствующие замещенные винилацетилена. Диацетилен - побочный продукт при получении ацетилена электрокрекингом метана. Получают его димеризацией ацетилена (кат. - CuCl) дегидрохлорированием 1,4-дихлор-2-бутина или 1,2,3,4-тетрабромбутана, напр.:
, при р-ции с Н2О - диацетил, при взаимод. с алкиламинами или тиолами - соответствующие замещенные винилацетилена. Диацетилен - побочный продукт при получении ацетилена электрокрекингом метана. Получают его димеризацией ацетилена (кат. - CuCl) дегидрохлорированием 1,4-дихлор-2-бутина или 1,2,3,4-тетрабромбутана, напр.: 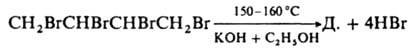
В высоких концентрациях диацетилен вызывает паралич дыхания.
Литература
Физер Л., Физер М., Реагенты для органического синтеза, т. 1, М., 1970, с. 252.- 53. Г. В. Дроздов.
Ещё по теме
Диацетилен — характеристики и методы получения
Диацетил — свойства и применение в химии
Дивинилацетилен — характеристики и применение
Дииодацетилен — характеристики и свойства
Дифенилацетилен — характеристики и растворимость
Ацетилен — свойства и применение
Ацетилен C2H2 — свойства и применение
Дибромацетилен — характеристики и растворимость
Диэтиленгликольдинитрат — характеристики и применение
Полигликоли — свойства и применение
Диэтиленгликольдинитрат — характеристики и применение
