Алюминия хлорид
АЛЮМИНИЯ ХЛОРИД А1С13, бесцв. дымящие на воздухе кристаллы с моноклинной решеткой (a = 0,591нм, b = = 1,024 нм, с = 0,616 нм,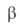 = 108,65°, z = 4, пространств. группа С2/m); т. возг. 180°С; тройная точка: т-ра 192,5°С, давл. 0,228 МПа, плотн. 2,44 г/см3;
= 108,65°, z = 4, пространств. группа С2/m); т. возг. 180°С; тройная точка: т-ра 192,5°С, давл. 0,228 МПа, плотн. 2,44 г/см3;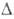 Н°пл 35,3 кДж/моль,
Н°пл 35,3 кДж/моль,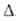 H0возг 115,7 кДж/моль (см. также табл.). В жидком состоянии и в парах до 440°С существует в виде димера, к-рый при 440-800°С сосуществует с мономером. При 800-1000°С стабилен только мономер.
H0возг 115,7 кДж/моль (см. также табл.). В жидком состоянии и в парах до 440°С существует в виде димера, к-рый при 440-800°С сосуществует с мономером. При 800-1000°С стабилен только мономер.
СВОЙСТВА ХЛОРИДА АЛЮМИНИЯ 
Алюминия хлорид раств. в воде (44 г в 100 г при 25°С), спирте (100 г в 100 г при 12,5 СС), ацетоне, СНС13, дихлорэтане, диэтиленгликоле, фосгене, нитробензоле, эфире, СС14, CS2 и др.; не раств. в бензоле, толуоле. Из водных р-ров кристаллизуется в виде желтовато-белого расплывающегося на воздухе гексагидрата. В воде постепенно гидролизуется. Алюминия хлорид-к-та Льюиса. Образует комплексные соед. с NH3, хлоридами и оксихлоридами (РС15, РОС13, NaCl и др.), а также с мн. орг. в-вами. Взаимод. с расплавом А1, давая монохлорид А1С1, существующий только в газовой фазе.
Получают алюминия хлорид действием С12 в присут. восстановителя (СО, углерод) на обезвоженный каолин или боксит. Лаб. способ - взаимод. С12 или НС1 с А1. Гексагидрат получают р-цией А1(ОН)3 с конц. соляной к-той с послед. высаливанием из р-ра действием НС1.
Алюминия хлорид-катализатор в орг. синтезе, напр. в р-циях Фриделя-Крафтса, промежут. продукт в произ-ве А1 методом электролиза, реагент для извлечения А1 из сплавов и получения А1 высокой чистоты. Гексагидрат и его р-ры используют для очистки сточных вод, обработки дерева и др.
Мировое произ-во алюминия хлорида более 140 тыс. т/год (1980).
Лит:. Фурман А. А., Неорганические хлориды, М., 1980, с. 143-79. В. П. Данилов.
