Трихлорэтилён
ТРИХЛОРЭТИЛЕН (трихлорэтен) ClCH = CCl2, мол.м. 131,39; бесцв. жидкость со сладковатым запахом; т. пл. -73 0C, т. кип. 86,7 0C;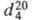 1,4642;
1,4642; 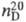 1,4773; ркрит5,02 МПа, tкрит 271 0C;
1,4773; ркрит5,02 МПа, tкрит 271 0C; 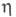 (мПа·с) жидкости 0,90 (-20 0C), 0,58 (20 0C), 0,37 (75 0C);
(мПа·с) жидкости 0,90 (-20 0C), 0,58 (20 0C), 0,37 (75 0C); 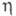 (мкПа·с) пара 9,28 (20 0C), 11,90 (100 0C);
(мкПа·с) пара 9,28 (20 0C), 11,90 (100 0C);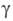 (мН/м) 29,28 (20 0C), 24,4 (60 0C);
(мН/м) 29,28 (20 0C), 24,4 (60 0C);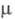 2,98 ·10-30 Кл·м; давление пара (кПа): 0,13 (-43,8 0C), 2,68 (0 0C), 8,0 (20 0C), 40,75 (6O0C); С°р [кДж/(кг·К)] жидкости 0,912 (-40 0C), 0,962 (20 0C), 0,996 (60 0C), пара 0,594 (О 0C), 0,657 (100 0C), 0,720 (300 0C);
2,98 ·10-30 Кл·м; давление пара (кПа): 0,13 (-43,8 0C), 2,68 (0 0C), 8,0 (20 0C), 40,75 (6O0C); С°р [кДж/(кг·К)] жидкости 0,912 (-40 0C), 0,962 (20 0C), 0,996 (60 0C), пара 0,594 (О 0C), 0,657 (100 0C), 0,720 (300 0C); 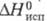 (кД/кг) 278,7 (-20 0C), 262,8 (20 0C), 231,0 (100 0C),
(кД/кг) 278,7 (-20 0C), 262,8 (20 0C), 231,0 (100 0C),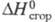 -962,32 кДж/моль,
-962,32 кДж/моль,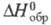 -7,53 кДж/моль; теплопроводность [Вт/(м·К)] жидкости 0,142 (-40 0C), 0,138 (20 0C), 0,099 (80 0C), пара 0,00833 (86,7 0C); e 3,42 (16 0C). Хорошо раств. в орг. р-рителях. Р-римость в воде (% по массе): 0,017 (10 0C), 0,027 (20 0C), 0,125 (60 0C), р-римость воды в трихлорэтилене 0,02 (20 0C), 0,08 (60 0C). Образует азеотропную смесь с водой (т. кип. 73 0C, 7% воды). Энергии связей (кДж/моль):
-7,53 кДж/моль; теплопроводность [Вт/(м·К)] жидкости 0,142 (-40 0C), 0,138 (20 0C), 0,099 (80 0C), пара 0,00833 (86,7 0C); e 3,42 (16 0C). Хорошо раств. в орг. р-рителях. Р-римость в воде (% по массе): 0,017 (10 0C), 0,027 (20 0C), 0,125 (60 0C), р-римость воды в трихлорэтилене 0,02 (20 0C), 0,08 (60 0C). Образует азеотропную смесь с водой (т. кип. 73 0C, 7% воды). Энергии связей (кДж/моль): 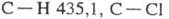 (для группы CHCl) 577,4.
(для группы CHCl) 577,4.
Трихлорэтилен реагирует с хлором: в жидкой фазе в присут. FeCl3 при 20-50 0C с образованием пентахлорэтана, в газовой фазе при 600 0C или в присут. катализаторов (песок и др.) при 450-550 0C с образованием смеси тетрахлорэтилена и гекса-хлорэтана. Трихлорэтилен присоединяет HCl в присут. AlCl3; при этом происходит конденсация, полимеризация и осмоление. При взаимод. со спиртовыми и конц. водными р-рами щелочей, а также при пиролизе образуется дихлорацетилен. Гидролиз трихлорэтилена водными р-рами щелочей при 150 0C приводит к гликолевой к-те, а гидролиз H2SO4 - к монохлоруксусной к-те; при восстановлении образуется 1,2-дихлорэтилен, в присут. катализаторов (Ni, Pd, Pt) - этилен; при окислении O2 воздуха -дихлорацетилхлорид, фосген, СО и HCl (р-ция ускоряется в присут. I2, к-т или УФ света). Для стабилизации трихлорэтилена используют алкиламины, эпоксиды и др.
Совр. метод получения трихлорэтилена совместно с тетрахлорэтиленом -высокотемпературное хлорирование смеси хлорэтанов и хлорэтиленов (обычно отходы от произ-ва винилхлорида, дихлорэтана) либо индивидуальных соед., напр, дихлор- или трихлорэтанов. Процесс проводят при 400-450 0C, как правило в кипящем слое катализатора (силикагель). Используют также окислит. хлорирование хлорэтанов и(или) хлорэтиленов в присут. катализатора (CuCl2 и KCl на носителях -корунде, силикагеле и др.) при 350-400 0C.
Применяют трихлорэтилен для обезжиривания металлов, для хим. чистки текстильных изделий, ранее применяли для произ-ва монохлоруксусной к-ты.
Трихлорэтилен- трудногорючий продукт, т. всп. 32 0C, т. самовоспл. 4160C; КПВ 10,5-41,0%. ПДК в воздухе рабочей зоны 10 мг/м3, в воздухе населенных мест 1 мг/м3 (среднесуточная), в водоемах хозяйственно-бытового пользования 0,06 мг/л.
Мировое произ-во 500 тыс. т/год (1990).
Лит. см. при ст. Тетрахлорэтаны. Ю. А. Трегер.
