Метиленхлорид
МЕТИЛЕНХЛОРИД (дихлорметан, хлористый метилен, хладон 30; фреон 30) СН2Сl2, мол.м. 84,93; бесцв. жидкость со сладковатым запахом; т.пл. -96,7°С, т.кип. 40,1 °С; d204 1,336; nD20 1,4244; С0р 1,213 кДж/(кг.К); длина связи С—Н 0,1068 нм, связи С—Сl 0,1772 нм; углы НСН 112°, СlССl 111,8°; m для пара 5,41•10-30 Кл.м; энергия связи С—Н 407,52 кДж/моль, С—Сl 330,12 кДж/молъ; DH0исп 336,4 кДж/кг (20 °С), DH0сгор -446,85 кДж/моль (для жидкости), DH0обр -87,86 кДж/моль; S0298 270,13 Дж/(моль.К); h 0,435 мПа.с; g 28,12 мН/м (20 °С); e 9,08 (для пара-1,0065), р 0,23.109 Ом.м; теплопроводность 0,1523 Вт/(м.К); давление пара 52,39 кПа (20 °С); tкрит 245 °С, pкрит 6,17 МПа, dкрит 472 г/см . Хорошо раств. в орг. р-рителях, плохо-в воде (2% при 20 °С); образует азеотропную смесь с водой (т.кип. 38,1 °С, 98,5% метиленхлорида).
Метиленхлорид реагирует с хлором с образованием СНСl3 и ССl4. С иодом при 200 °С дает СН2l2, с бромом при 25-30 °С в присут. Аl-бромхлорметан. При нагр. с водой гидроли-зуется до СН2О и НСl. В присут. металлов VIII гр. (Pd, Pt, Ni) гидрируется до метилхлорида и метана. При нагр. со спиртовым р-ром NH3 до 100-125 °С образует гексаме-тилентетрамин. Р-ция с водным р-ром NH3 при 200 °С приводит к метиламину, муравьиной к-те и НСl.
С ароматич. соед. в присут. АlСl3 метиленхлорид вступает в р-цию Фриделя - Крафтса, напр. с бензолом образует дифенил-метан. В газовой фазе реагирует при 270 °С с NO2 по схеме: СН2Сl2 + NO2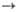 СО + NO + 2HCl. Метиленхлорид получают совместно с хлороформом хлорированием метана в паровой фазе при 510-520°С и соотношении метан:хлор, равном 5:1. Непрореагировавший метан и образовавшийся метилхлорид после отмывки НСl, осушки, нейтрализации и комлрими-рования реакционного газа возвращаются в реактор. Метиленхлорид, выделяемый ректификацией, имеет чистоту не менее 99,7%. Метиленхлорид получают также жидкофазным хлорированием метилхлорида при 80-90 °С в присут. N,N'-азо-бис-изобути-ронитрила.
СО + NO + 2HCl. Метиленхлорид получают совместно с хлороформом хлорированием метана в паровой фазе при 510-520°С и соотношении метан:хлор, равном 5:1. Непрореагировавший метан и образовавшийся метилхлорид после отмывки НСl, осушки, нейтрализации и комлрими-рования реакционного газа возвращаются в реактор. Метиленхлорид, выделяемый ректификацией, имеет чистоту не менее 99,7%. Метиленхлорид получают также жидкофазным хлорированием метилхлорида при 80-90 °С в присут. N,N'-азо-бис-изобути-ронитрила.
Метиленхлорид используют для обработки фото- и кинопленок, как р-ритель для снятия красок, обезжиривания металлич. пов-сти, в качестве хладагента и как добавку к аэрозолям.
Т. всп. 14 °С, т. самовоспл. 556 °С, КПВ 12-22%; ПДК 50 мг/м3 (в воде водоемов санитарно-бытового водопользования-7,5 мг/л).
Произ-во в США 309 тыс. т/год (1988).
Исп. литература для статьи «МЕТИЛЕНХЛОРИД»: Промышленные хлорорганические продукты, под ред. Л. А. Ошина, М., 1978; Трегер Ю. А., Карташов Л. М., Кришталь Н. Ф., Основные хло-рорганические растворители, М., 1984. Ю. А. Трегер.
