Молибдена галогениды
МОЛИБДЕНА ГАЛОГЕНИДЫ. Молибден образует простые, смешанные и комплексные галогениды, а также оксо-галогениды. Гексафторид MoF6-подвижная жидкость (см. табл.). Твердый MoF6 образует две полиморфные модификации: ниже — 9,76 °С-ромбическую и выше -9 76 °С-кубическую (а = 0,6221 нм при 266 К, z = 2); DH0 перехода 8,171 кДж/моль. Ур-ния температурной зависимости: плотн. жидкого в-ва d= 2,614-0,00416t г/см3 (17,0 <= t <= 76,7°С); давления пара lg p(Па) = 9,990- 1499,9/T (290,6 <= Т <=307 К), lg p (Па) = 9,670- 1432/T (308 <= Т <= <= 363 К). Раств. в безводном HF, ClF3, C2Cl2F4 и орг. р-рителях; дает с HF азеотропную смесь. Образует соед. типа MMoF7 и M2MoF8 (М - однозарядный катион). Получают взаимод. порошкообразных Мо или МоО3 (в присут. NaF) с F2 при 300-450 °С. Применяют для нанесения молибденовых покрытий на графит, Si, металлы и оксиды методом хим. осаждения из газовой фазы, как компонент катализатора гидрирования нефтепродуктов, при разделении изотопов Мо.
П е н т а ф т о р и д MoF5, т е т р а ф т о р и д MoF4 и т р и ф т о р и д MoF3 диспропорционируют при нагр. (3MoF5
 Mo2F9 + MoF6, 2Mo2F9
Mo2F9 + MoF6, 2Mo2F9 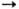 3MoF4 + MoF6, 2MoF4
3MoF4 + MoF6, 2MoF4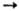
 MoF3 + MoF5, 2MoF3
MoF3 + MoF5, 2MoF3 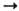 Mo + MoF6); MoF5 образует фторомолибдаты (V), MoF4 - фторомолибдаты (IV). Пентафторид Mo и низшие фториды получают восстановлением MoF6 металлами или Si, взаимод. раскаленной молибденовой проволоки с WF6, SF6 и др., как побочные продукты фторирования Мо.
Mo + MoF6); MoF5 образует фторомолибдаты (V), MoF4 - фторомолибдаты (IV). Пентафторид Mo и низшие фториды получают восстановлением MoF6 металлами или Si, взаимод. раскаленной молибденовой проволоки с WF6, SF6 и др., как побочные продукты фторирования Мо.
О к с о ф т о р и д ы MoOF4 и MoO2F2 получают взаимод. МоО3 с F2 или MoF6, а также МоОСl4 или МоО2Сl2 с HF. При растворении МоО3 или оксофторидов во фтористоводородной к-те образуются фторомолибденовые к-ты H2MoO3F2•H2O и H2MoO2F4•1,5H2O, дающие соли-оксо-фторомолибдаты (VI). Известны также и др. безводные или гидратированные оксофториды Мо и соед. МоО3_хРх со св-вами бронз оксидных.
П е н т а х л о р и д МоСl5-кристаллы с моноклинной решеткой (а =1,731 нм, b = 1,781 нм, с = 0,6079 нм, b = 95,7°, z=12, пространств. группа С2/т). Ур-ния температурной зависимости: плотн. жидкого в-ва d= 2,196-2,11 • 10 -8 х х (t - 194,4) г/см3 (194,4 <= t <= 400 °С); давления пара 1g р(Па)= 12,748-3391/T (343 <= Т <= 435 К). В парах разлагается до МоСl4 и Сl2. Раств. в ССl4, СНСl3, С2Н4Сl2; образует аддукты с РСl5, РОСl3, (CH3)3N, N4S4 и др. Получают взаимод. Мо или MoS2 с Сl2 при 400-500 °С либо МоО3 с ССl4, СОСl2 или SOCl2. Пентахлорид-промежут. продукт при получении Мо из ферромолибдена и отходов Мо, при синтезе Мо(СО)6. Применяют его для получения порошков Мо и нанесения молибденовых покрытий на металлы и керамику методом хим. осаждения из газовой фазы.
Т е т р а х л о р и д МоСl4, трихлорид МоСl3 и дихлорид МоСl2 получают взаимод. МоСl5, напр., с С6Н6, Мо, р-цией Мо с ССl4, при диспропорционировании и разложении хлоридов Мо. Дихлорид раств. в галогеноводородных к-тах с образованием Н2 [(Мо6Сl8) Х6].
О к с о т е т р а х л о р и д МоОСl4 получают взаимод. МоО3 либо МоО2Сl2 с МоСl5, SOCl2, смесью Сl2 с S2Cl2, д и о к с о д и х л о р и д МоО2Сl2-взаимод. МоО, с НСl, NaCl, ССl4 либо со смесью О2 с Сl2, ССl4 или S2Cl2. Известны также и др. безводные или гидратир. оксохлориды, хлоро- и оксохлоромолибдаты: М2[(Мо6Сl8)Сl6], М3МоСl6, ММоОСl4, М2МоСl5 и др.
Т е т р а б р о м и д МоВr4 легко окисляется и диспропорцио-нирует; получают взаимод. Мо или Мо(СО)6 с Вr2. Т р и-б р о м и д МоВr3 синтезируют взаимод. Мо с Вr2 или Hg2Br2, восстановлением МоВr4. Д и б р о м и д МоВr2 раств. в галогеноводородных к-тах с образованием Н2 [Мо6Вr8Х8], где Х-галоген; получают из элементов при 600-650°С, по р-ции МоСl2 с LiBr, при разложении МоВr3.
Д и о к с о д и б р о м и д МоО2Вr2 получают взаимод. Мо с Вr2 и О2 или МоО3 с Вr2. Известны также МоОВr3, МоОВr, бромомолибдаты(IV и III) и оксобромомолибдаты(V).
Т р и и о д и д МоI3 и дииодид МоI2 получают из простых в-в при т-рах выше 300 °С. Известен МоО2I2.
Синтезированы также молибдена галогениды типа МоСlnР6-n, МоСlnР5_n, Мо3Вr2Сl4.
Исп. литература для статьи «МОЛИБДЕНА ГАЛОГЕНИДЫ»: Галогениды молибдена, Новосиб., 1972; Буслаев Ю. А., Коку-иов Ю. В., "Координационная химия", 1983, т. 9, № 6, с. 723-51. См. также лит. при ст. Молибден. Э. Г. Раков.
