Липопротеины плазмы крови
Липопротеины – это высокомолекулярные водорастворимые частицы, представляющие собой комплекс белков и липидов. В этом комплексе белки вместе с полярными липидами формируют поверхностный гидрофильный слой, окружающий и защищающий внутреннюю гидрофобную липидную сферу от водной среды и обеспечивающий транспорт липидов в кровяном русле и их доставку в органы и ткани.
Плазменные липопротеины (ЛП) – это сложные комплексные соединения, имеющие характерное строение: внутри липопротеиновой частицы находится жировая капля (ядро), содержащая неполярные липиды (три-глицериды, эстерифицированный холестерин); жировая капля окружена оболочкой, в состав которой входят фосфолипиды, белок и свободный холестерин. Толщина наружной оболочки липопротеиновой частицы (ЛП-частица) составляет 2,1–2,2 нм, что соответствует половине толщины ли-пидного бислоя клеточных мембран. Это позволило сделать заключение, что в плазменных липопротеинах наружная оболочка в отличие от клеточных мембран содержит липидный монослой. Фосфолипиды, а также неэсте-рифицированный холестерин (НЭХС) расположены в наружной оболочке таким образом, что полярные группы фиксированы наружу, а гидрофобные жирно-кислотные «хвосты» – внутрь частицы, причем какая-то часть этих «хвостов» даже погружена в липидное ядро. По всей вероятности, наружная оболочка липопротеинов представляет собой не гомогенный слой, а мозаичную поверхность с выступающими участками белка. Существует много различных схем строения ЛП-частицы. Предполагают, что входящие в ее состав белки занимают только часть наружной оболочки. Допускается, что часть белковой молекулы погружена в ЛП-частицу глубже, чем толщина ее наружной оболочки (рис. 17.4). Итак, плазменные ЛП представляют собой сложные надмолекулярные комплексы, в которых химические связи между компонентами комплекса носят нековалентный характер. Поэтому применительно к ним вместо слова «молекула» употребляют выражение «частица».
Классификация липопротеинов. Существует несколько классификаций ЛП, основанных на различиях в их свойствах: гидратированной плотности, скорости флотации, электрофоретической подвижности, а также на различиях в апопротеиновом составе частиц.
Наибольшее распространение получила классификация, основанная на поведении отдельных ЛП в гравитационном поле в процессе ультрацентрифугирования. Применяя набор солевых плотностей, можно изолировать отдельные фракции ЛП: хиломикроны (ХМ) – самые легкие частицы, затем липопротеины очень низкой плотности (ЛПОНП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП).
Различная электрофоретическая подвижность по отношению к глобулинам плазмы крови положена в основу другой классификации ЛП, согласно которой различают ХМ (остаются на старте подобно γ-глобулинам), β-ЛП, пре-β-ЛП и α-ЛП, занимающие положение β-, α1- и α2-глобулинов соответственно. Электрофоретическая подвижность фракций ЛП, выделенных путем ультрацентрифугирования, соответствует подвижности отдельных глобулинов, поэтому иногда используют двойное их обозначение: ЛПОНП и пре-β-ЛП, ЛПНП и β-ЛП, ЛПВП и α-ЛП (рис. 17.5). Следует помнить, что изолированные различными методами ЛП не являются полностью идентичными, поэтому рекомендуется использовать терминологию, соответствующую методу выделения.
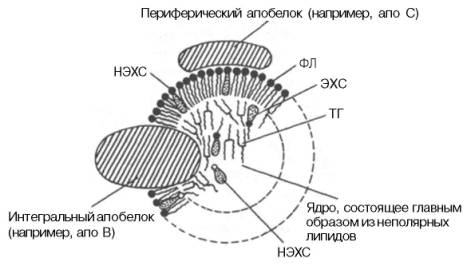
Рис. 17.4. Строение ЛП-частицы (схема). Имеется сходство со структурой плазматической мембраны. Некоторое количество эстерифицированного холестерина и триглицеридов (не показано) содержится в поверхностном слое, а в ядре частицы -небольшое количество неэстерифицированного холестерина (по А.Н. Климову и Н.Г. Никульчевой). Объяснение в тексте.
Аполипопротеины (апобелки, апо) входят в состав липопротеинов. Это один белок либо несколько белков, или полипептидов, которые называют апобелками (сокращенно апо). Эти белки обозначают буквами латинского алфавита (А, В, С). Так, два главных апобелка ЛПВП обозначаются A-I и А-II. Основным апобелком ЛПНП является апобелок В, он входит также в состав ЛПОНП и хиломикронов. Апобелки C-I, С-II и C-III представляют собой небольшие полипептиды, которые могут свободно переходить от одного липопротеина к другому. Помимо апобелков А, В и С, в липопро-теинах плазмы крови идентифицировано еще несколько апобелков. Одним из них является выделенный из ЛПОНП апобелок Е, на его долю приходится 5–10% от общего количества апобелков ЛПОНП.
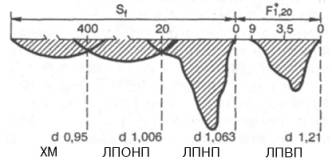
Рис. 17.5. Шлирен-профиль липопротеинов плазмы крови человека при аналитическом ультрацентрифугировании (по А.Н. Климову и Н.Г. Никульчевой, 1995).
Апобелки выполняют не только структурную функцию, но и обеспечивают активное участие комплексов ЛП в транспорте липидов в токе крови от мест их синтеза к клеткам периферических тканей, а также обратный транспорт холестерина в печень для дальнейших метаболических превращений. Апобелки выполняют функцию лигандов во взаимодействии ЛП со специфическими рецепторами на клеточных мембранах, регулируя тем самым гомеостаз холестерина в клетках и в организме в целом. Не меньшее значение имеет также регуляция апобелками активности ряда основных ферментов липидного обмена: лецитин-холестеролацилтрансферазы, липопротеинлипазы, печеночной триглицеридлипазы. Структура и концентрация в плазме крови каждого апобелка находится под генетическим контролем, в то время как содержание липидов в большей степени подвержено влиянию диетических и других факторов.
Дислипопротеинемией (ДЛП) называют изменения в содержании липопротеинов в плазме (сыворотке) крови: повышение, снижение или практически полное отсутствие. Сюда же относят случаи появления в крови необычных или патологических ЛП. Таким образом, понятие «дислипопро-теинемия» охватывает все разновидности изменения уровня ЛП в крови. Более узким является термин «гиперлипопротеинемия» (ГЛП), отражающий увеличение какого-то класса или классов ЛП в крови. Первой и весьма успешной попыткой систематизации отклонений от нормы в липопротеид-ном спектре крови явилась классификация типов ГЛП, разработанная D. Fredrickson и соавт. и одобренная экспертами ВОЗ. Согласно варианту ВОЗ, различают следующие типы ГЛП.
Тип I – гиперхиломикронемия. Основные изменения в липопротеи-нограмме следующие: высокое содержание ХМ, нормальное или слегка повышенное содержание ЛПОНП; резко повышенный уровень триглицери-дов в сыворотке крови. Клинически это состояние проявляется ксантома-тозом.
Тип II делят на два подтипа: тип IIа – гипер-β-липопротеинемия с характерным высоким содержанием в крови ЛПНП и тип IIб – гипер-β-липо-протеинемия с высоким содержанием одновременно двух классов липопро-теинов (ЛПНП, ЛПОНП). При типе II отмечается высокое, а в некоторых случаях очень высокое содержание холестерина в плазме крови. Уровень триглицеридов в крови может быть либо нормальным (типа IIа), либо повышенным (тип IIб). Клинически проявляется атеросклеротическими нарушениями, нередко развивается ишемическая болезнь сердца (ИБС).
Тип III – дис-β-липопротеинемия. В сыворотке крови появляются липопротеины с необычно высоким содержанием холестерина и высокой электрофоретической подвижностью («флотирующие» β-липопротеины). Они накапливаются в крови вследствие нарушения превращения ЛПОНП в ЛПНП. Этот тип ГЛП часто сочетается с различными проявлениями атеросклероза, в том числе с ИБС и поражением сосудов ног.
Тип IV – гиперпре-β-липопротеинемия. Характерны повышение уровня ЛПОНП, нормальное содержание ЛПНП, отсутствие ХМ; увеличение уровня триглицеридов при нормальном или слегка повышенном уровне холестерина. Клинически этот тип сочетается с диабетом, ожирением, ИБС.
Тип V – гиперпре-β-липопротеинемия и гиперхиломикронемия. Наблюдаются повышение уровня ЛПОНП, наличие ХМ. Клинически проявляется ксантоматозом, иногда сочетается со скрытым диабетом. Ишемической болезни сердца при данном типе ГЛП не наблюдается.
Несомненным достоинством данной классификации является то, что она выделила связь нарушений обмена ЛП с развитием атеросклероза, благодаря чему не утратила своего значения и в настоящее время. Однако эта классификация не охватывает все возможные варианты отклонений от нормы в содержании липидов и ЛП в плазме крови. В частности, она не учитывает изменения концентрации ЛПВП, пониженное содержание которых является независимым фактором риска развития атеросклероза и ИБС, а повышенное, наоборот, выполняет роль антириск-фактора.
Исследования, проведенные во многих странах мира, показали, что у больных ИБС содержание α-липопротеинового холестерина ниже, чем у лиц без признаков ИБС. Холестерин ЛПВП как «предсказатель» ИБС оказался в 8 раз чувствительнее, чем холестерин ЛПНП. Предложено в качестве «предсказателя» рассчитывать так называемый холестериновый коэффициент атерогенности (К), представляющий собой отношение уровня холестерина ЛПНП и ЛПОНП к содержанию холестерина ЛПВП:
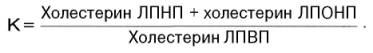
В клинике очень удобно рассчитывать этот коэффициент на основании определения уровня общего холестерина и холестерина ЛПВП:
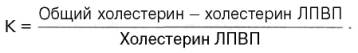
Чем выше этот коэффициент (у здоровых лиц он не превышает 3), тем выше опасность развития (и наличия) ИБС.


