Назарова реакция
НАЗАРОВА РЕАКЦИЯ, циклизация дивинилкетонов в замещенные циклопентеноны, напр.:
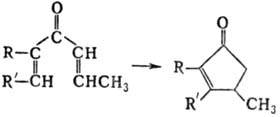
Р-цию осуществляют нагреванием (обычно при 50-100°С) дивинилкетонов (их получают гидратацией дивинилацетиле-новых углеводородов или др. способами) с Н3РО4, H2SO4, НСl или др. к-той. Получение циклопентенонов с геминаль-ными заместителями требует более жестких условий. Незамещенный циклопентенон этим методом получить нельзя. Выходы циклопентенонов достигают 70-80%.
Побочные продукты - 2-гидроксициклопентаноны, тетра-гидро-2-пираноны и в-ва, образующиеся в результате миграции кратной связи в цикле.
Назарова реакция-стереоселективная конротаторная электроциклич. р-ция. Она м.б. использована для лаб. синтеза структурных аналогов прир. соед. с азуленовой, стероидной или терпе-новой структурой.
Р-ция открыта И. Н. Назаровым в 1941.
Лит.: Назаров И. Н., "Успехи химии", 1951, т. 20, в. 1, с. 71-103; Елизарова А. Н., Химия циклопентенонов, М., 1966. В. Б. Мочалин.

Дополнения к описанию реакции Назарова: