Гелля-Фольгарда-Зелинского реакция
ГЕЛЛЯ -ФОЛЬГАРДА -ЗЕЛИНСКОГО РЕАКЦИЯ (р-ция Хелля-Фольхарда-Зелинского), получение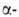 галоген-замещенных карбоновых к-т и их производных галогенированием к-т бромом (реже хлором) в присут. Р или его галогенидов:
галоген-замещенных карбоновых к-т и их производных галогенированием к-т бромом (реже хлором) в присут. Р или его галогенидов: 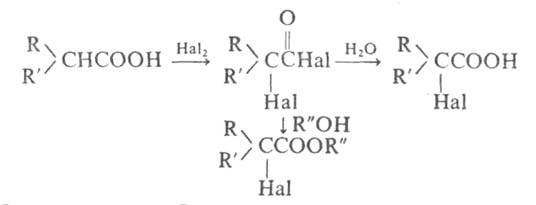
Обычно смесь карбоновой к-ты, Вr2 и красного Р или РНа13 нагревают при 80-100 °С без р-рителя. При использовании Р в стехиометрич. кол-вах образуются бромангидриды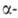 бромкарбоновых к-т, к-рые (часто без предварит. очистки) обрабатывают водой или спиртами для получения
бромкарбоновых к-т, к-рые (часто без предварит. очистки) обрабатывают водой или спиртами для получения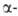 бромкарбоновых к-т или их эфиров. РВr5, образующийся в результате взаимод. Р с Вr2, превращает к-ту в бромангидрид, к-рый галогенируется легче, чем своб. к-та [вероятно, промежуточно образуется
бромкарбоновых к-т или их эфиров. РВr5, образующийся в результате взаимод. Р с Вr2, превращает к-ту в бромангидрид, к-рый галогенируется легче, чем своб. к-та [вероятно, промежуточно образуется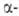 галогененол (ф-ла
галогененол (ф-ла 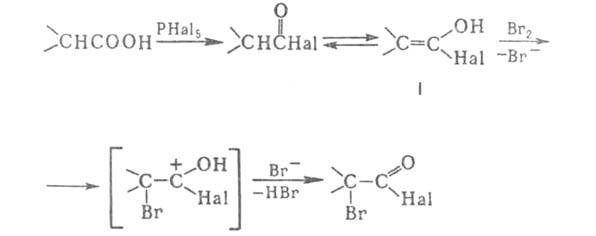
В случае применения лишь каталитич. кол-в Р образующийся галогенангидрид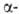 галогенкарбоновой к-ты взаимод. с непрореагировавшей исходной к-той, при этом регенерируется галогенангидрид незамещенной к-ты, к-рый далее снова подвергается галогенированию:
галогенкарбоновой к-ты взаимод. с непрореагировавшей исходной к-той, при этом регенерируется галогенангидрид незамещенной к-ты, к-рый далее снова подвергается галогенированию: 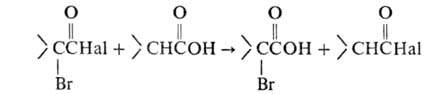
В результате галогенкарбоновую к-ту получают непосредственно (без обработки водой).
галогенкарбоновую к-ту получают непосредственно (без обработки водой).
Часто для получения эфиров галогенкарбоновых к-т из исходной к-ты получают хлорангидрид действием SOC12, хлорангидрид галогенируют Вr2 или SO2C12 (иногда в присут. следов I2); образующийся хлорангидрид
галогенкарбоновых к-т из исходной к-ты получают хлорангидрид действием SOC12, хлорангидрид галогенируют Вr2 или SO2C12 (иногда в присут. следов I2); образующийся хлорангидрид галогенкарбоновой к-ты обрабатывают спиртом, напр.:
галогенкарбоновой к-ты обрабатывают спиртом, напр.: 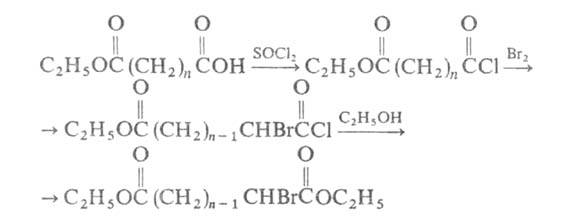
Выходы Гелля - Фольгарда - Зелинского реакции достигают 80-90%. Из образующихся к-т или эфиров обычно синтезируют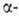 гидрокси-,
гидрокси-,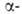 амино-и
амино-и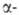 меркаптокарбоновые к-ты. Р-ция открыта К. М. Геллем в 1881 и усовершенствована Я. Фольгардом и Н. Д. Зелинским в 1887.
меркаптокарбоновые к-ты. Р-ция открыта К. М. Геллем в 1881 и усовершенствована Я. Фольгардом и Н. Д. Зелинским в 1887.
Литература
Бюлер К., Пирсон Д., Органические синтезы, пер. с англ., ч. 1, М., 1973, с. 439-41. f Е.М.Рохлин.
