Водородная связь
Помимо различных гетерополярных и го-меополярных связей, существует еще один особый вид связи, который в последние два десятилетия привлекает все большее внимание химиков. Это так называемая водородная связь. Оказалось, что атом водорода может образовывать связь между двумя электроотрицательными атомами (F, О, N, реже Сl и S). Известны случаи, когда эту связь образует водородный атом, связанный с атомом углерода в соединениях типа НСХ3, где X — электроотрицательный атом или группа (например, в HCN, фторуглеводородах). Хотя в настоящее время природа водородной связи еще до конца не выяснена, одна.ко определен-ное представление о ней уже можно составить.
Водородная связь образуется между электроотрицательными атомами, из которых хотя бы один имеет свободную электронную пару, например:
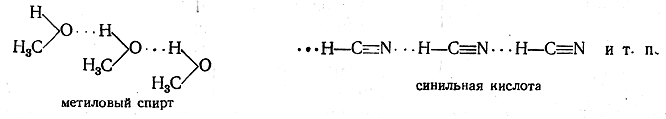
(водородная связь обозначается пунктиром из трех точек).
Таким образом, водородная связь по своему характеру является, по-видимому, электростатической; она образуется вследствие притяжения ковалентно связанного протона свободными электронами атома другой молекулы. При этом протон находится не посредине между связываемыми им атомами (даже если они одинаковы), а ближе к тому атому, с которым он связан ковалентно. Так, в случае воды
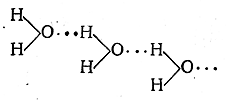
одно расстояние О—Н равно 0,99 А, а другое 1,76 А.
Вопрос о том, находится ли водород в фиксированном положении или он совершает колебания между двумя положениями равновесия, в общем случае еще неясен, хотя исследование хингидрона методом меченых атомов свидетельствует о фиксированном положении водорода водородной связи в этом соединении.
Энергия водородной связи мала; она имеет порядок 5—10 ккал/моль, в то время как, например, энергия нормальной связи О—Н равна 109 ккал/моль, а связи Н—F 148 ккал/моль. При плавлении льда рвется около 15% всех водородных связей, при нагревании воды до 40° С рвется около половины водородных связей. В парах воды водородных связей практически нет. При плавлении спиртов водородные связи почти не разрываются, однако они полностью рвутся при их испарении. В кар-боновых кислотах водородные связи не разрываются и при:
испарении, благодаря чему, например, муравьиная кислота и в паровой фазе существует в виде димера
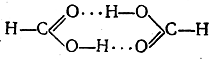
Однако и в этом случае энергия водородной связи составляет всего около 7 ккал/моль.
Наличие водородных связей оказывает существенное влияние на физические свойства соединений. Именно водородные связи обусловливают ассоциацию воды и спиртов, а следовательно, и аномально высокие точки их кипения сравнительно, например, с сероводородом и меркаптанами. Способность спиртов, аминов, карбоновых кислот, амидов растворяться в воде вызвана образованием водородных связей с молекулами воды.
Некоторые соединения, подобно енольной форме ацетоуксус-ного эфира, о-нитрофенолу и др., образуют внутримолекулярные водородные связи с замыканием цикла.
Изучение водородных связей должно пролить дополнительный свет на строение и свойства многих органических веществ.