Серебра азид
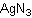
Внешний вид:
бел. ромбические кристаллыБрутто-формула (система Хилла): AgN3
Молекулярная масса (в а.е.м.): 149,89
Температура плавления (в °C): 250
Температура разложения (в °C): 297
Продукты термического разложения:
серебро, азотРастворимость (в г/100 г или характеристика):
ацетон: 0,015 (20°C)вода: не растворим (20°C)
вода: 0,01 (100°C)
этанол: 0,006 (20°C)
Вкус, запах, гигроскопичность:
не гигроскопиченМетод получения 1.
(лабораторный синтез)Источник информации: "Руководство по неорганическому синтезу" т.4 под ред. Брауэра Г. М.:Мир 1985 стр. 1094
Азид серебра (чистота 99,7-99,9%) в лабораторном масштабе получают из разбавленного водного раствора нитрата серебра путем постепенной добавки водного раствора азида натрия при интенсивном перемешивании и температуре 60-70 С. Осадок промывают водой, затем 95%-ным спиртом, в заключение - абсолютным эфиром, сушат и хранят в эксикаторе над концентрированной серной кислотой.
Способы получения:
1. Получают реакцией нитрата серебра с гидразингидратом и нитритом натрия. (выход 82%)Плотность:
4,81 (20°C, г/см3)Стандартный электродный потенциал:
AgN3 + e- → Ag + N3-, E = 0,292 В (вода, 25 C)Показатель диссоциации:
pПР (0) = 8,54 (20 C, вода)Стандартная энтальпия образования ΔH (298 К, кДж/моль):
279,5 (т)История:
Впервые получен Курциусом.
Дополнительная информация:
При температуре разложения взрывается. Детонирует при встряхивании и ударе. Под действием света темнеет. Менее чувствителен к удару чем гремучая ртуть и азид свинца: чувствительность мелкокристаллического = 777 мм (груз 0,5 кг), крупнокристаллического = 285 мм (груз 0,5 кг), аналогичные условия для гремучей трути дают значение 127 мм. Обладает большей бризантностью, чем гремучая ртуть (по песочной пробе). Предельные заряды для подрыва: тротила = 70 мг, тетрила = 20 мг, пикриновой кислоты = 35 мг.
Растворяется в азотной кислоте, растворим в растворе аммиака.
- "Руководство по неорганическому синтезу" т.4 под ред. Брауэра Г. М.:Мир 1985 стр. 1094
- "Справочник химика" т.2, Л.-М.: Химия, 1964 стр. 206-207
- "Справочник химика" т.3, Л.-М.: Химия, 1965 стр. 750
- Багал Л.И. "Химия и технология инициирующих взрывчатых веществ" М. 1975 стр. 238-241
