Деградация жирных кислот: β-окисление
А. Деградация жирных кислот: β-окисление
После попадания в клетки жирные кислоты активируются путем образования ацил-КоА Для этого нужны две богатые энергией ангидридные связи АТФ. В матрикс митохондрий активированные жирные кислоты попадают в виде ацилкарнитина, который является трансмембранным переносчиком.
Деградация жирных кислот происходит в митохондриальном матриксе путем окислительного цикла реакций, при котором последовательно отщепляются С2-звенья в виде ацетил-КоА (активированной уксусной кислоты). Последовательное отщепление ацетильных групп начинается с карбоксильного конца активированных жирных кислот каждый раз между С-2 (α-атомом) и С-3 (β-атомом). Поэтому цикл реакций деградации называется β-окислением. Пространственно и функционально β-окисление тесно связано с цитратным циклом и дыхательной цепью.
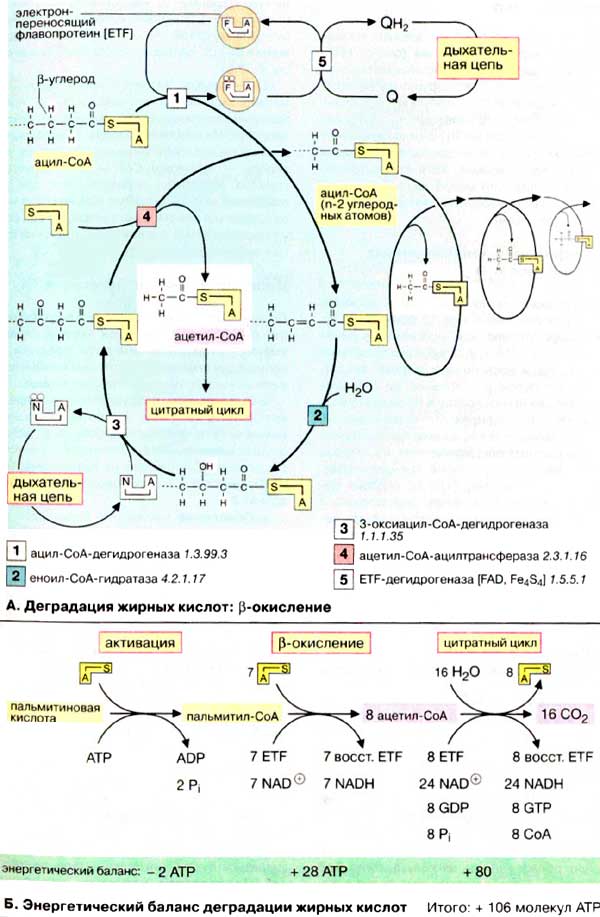
Первая стадия β-окисления — дегидрирование активированной жирной кислоты (ацил-КоА) с образованием β-ненасыщенной жирной кислоты с двойной связью в транс-конфигурации (реакция [1]: дегидрирование). При этом оба атома водорода с электронами переносятся от фермента [1] на электронпереносящий флавопротеин (ETF). ETF-дегидрогеназа (5) переносит восстановительные эквиваленты на убихинон (кофермент Q), который является составной частью дыхательной цепи. Вторая стадия деградации жирной кислоты состоит в присоединении молекулы воды к двойной связи ненасыщенной жирной кислоты (реакция [2]: гидратирование). На третьей стадии происходит окисление гидроксильной группы при С-3 в карбонильную группу (реакция [3]: дегидрирование). Акцептором для восстановительных эквивалентов является НАД+ который передает их в дыхательную цепь. На четвертой стадии активированная β-кетокислота расщепляется ацилтрансферазой (β-кетотиолазой) в присутствии кофермента А (реакция [4]: тиолитическое расщепление). Продуктами реакции являются ацетил-КоА и активированная жирная кислота, углеродная цепь которой короче на два углеродных атома по сравнению с длиной цепи исходной жирной кислоты.
Для полной деградации длинноцепочечной жирной кислоты цикл должен многократно повторяться; например, для стеарил-КоА (18:0) необходимы восемь циклов. Образующийся ацетил-КоА может переноситься на оксалоацетат с образованием цитрата, промежуточного метаболита цитратного цикла. При избытке ацетил-КоА в печени образуются кетоновые тела.
Б. Энергетический баланс деградации жирных кислот
Для расчета энергетического баланса деградации жирной кислоты в качестве примера рассмотрим молекулу пальмитиновой кислоты (16:0), которая окисляется полностью до 16 молекул СО2. На первой стадии жирная кислота активируется, потребляя две богатые энергией связи [АТФ (АТР)], с образованием пальмитоил-СоА состоящего из восьми C2-звеньев. Затем протекают семь циклов β-окисления. При этом образуются 7 молекул восстановленной формы флавопротеина (ETF) и 7 молекул НАДН + Н+. Оба соединения включаются в дыхательную цепь; окисление ETF через убихинон дает в итоге 1,5 молекулы АТФ, а НАДН + Н+ — 2,5 молекулы. Таким образом, β-окисление одного пальмитоильного остатка дает 28 молекул (7 х 4) АТФ. Окисление каждой молекулы ацетил-КоА приводит к образованию 10 молекул АТФ, что означает получение еще 80 молекул (8 x 10) АТФ. Из 28 + 80 молекул АТФ следует вычесть две молекулы АТФ, израсходованные при активации пальмитиновой кислоты. Итак, при утилизации одной молекулы пальмитиновой кислоты синтезируются 106 молекул АТФ, что соответствует свободной энергии 3300 кДж/моль (106 х 30,5 кДж/моль АТФ). Выигрыш в энергии при деградации жирных кислот существенно выше по сравнению с распадом углеводов (32 молекулы АТФ на 1 молекулу глюкозы) и белков даже с учетом больших размеров молекул. Поэтому жиры представляют собой очень выгодную форму сохранения энергии.


