Ионный обмен
Ионный обмен, обмен ионов в растворах электролитов (гомогенный ионный обмен). При смешении разбавленных растворов электролитов, например NaCl и KNO3 в смеси присутствуют ионы Na+, К+, NO3— и Cl—. Равновесное состояние выразится в этом случае уравнением: 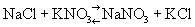 (реакция двойного обмена). Если одно из веществ, могущих получиться при взаимодействии, диссоциировано меньше других, равновесие сдвигается в сторону образования малодиссоциированного вещества. Равновесие сдвигается также в сторону образования летучего или малорастворимого продукта (если он выделяется из данной фазы) по реакциям:
(реакция двойного обмена). Если одно из веществ, могущих получиться при взаимодействии, диссоциировано меньше других, равновесие сдвигается в сторону образования малодиссоциированного вещества. Равновесие сдвигается также в сторону образования летучего или малорастворимого продукта (если он выделяется из данной фазы) по реакциям:
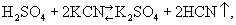
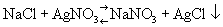
При выпаривании равновесного раствора прежде всего начинается кристаллизация соли (комбинации ионов), обладающей меньшей растворимостью. Избирательность кристаллизации может быть вызвана также добавлением органических растворителей (спирт, ацетон, диоксан и т. п.).
При гетерогенном ионном обмене (ионообменная сорбция) обмен происходит между ионами, находящимися в растворе, и ионами, присутствующими на поверхности твёрдой фазы — ионита. При соприкосновении ионита, насыщенного одним ионом, например Н+, с раствором, содержащим другие ионы, например Na+ и Ca2+, происходит обмен ионов между раствором и ионитом: в растворе уменьшаются концентрации Na+ и Ca2+ и появляется эквивалентное количество ионов Н+.
Гетерогенный ионный обмен имеет место при сорбции из растворов электролитов на некоторых минералах (алюмосиликатах, гидратах окисей металлов, цеолитах), в клетках и мембранах живых организмов и в синтетических ионообменных сорбентах. Гетерогенный ионный обмен широко применяется для обессоливания воды, идущей для питания котлов паром высоких параметров, в гидрометаллургии, в химической и фармацевтической промышленности (см. Иониты).
К. В. Чмутов.
